Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos Venezolanos de Puericultura y Pediatría
versión impresa ISSN 0004-0649
Arch Venez Puer Ped v.72 n.3 Caracas sep. 2009
Acidez titulable como control de calidad para la leche humana
Ameysa Torres De Freitas(*), Zandra Durán(**), Carmen Rodríguez(***)
(*) Médico Cirujano. Complejo Hospitalario Universitario Ruiz y Páez. Ciudad Bolivar. Edo. Bolivar. Correspondencia: ameysat@gmail.com. Cel.:(0414)102.5203
(**) Pediatra, coordinadora del Servicio de Banco de Leche Humana. Complejo Hospitalario Universitario Ruiz y Páez. Ciudad Bolivar. Edo. Bolivar. Correspondencia: zandraduranm@hotmail.com. Cel:(0414)854.75.69 y (0416)188.9235
(***) Licenciada en Bioanalisis. Jefa del Dpto. de Ciencias Fisiologicas. Profesora de Bioquimica. Universidad de Oriente. Núcleo Bolivar. Ciudad Bolivar. Estado Bolivar.
RESUMEN:
La determinación de la acidez titulable es una prueba fisicoquímica de control de calidad para leche humana que debe realizarse de rutina como parámetro clasificatorio en los Bancos de Leche Humana (BLH).
Objetivo: Analizar la acidez titulable como control de calidad para la leche humana en el Banco de Leche del Complejo Hospitalario Universitario Ruiz y Páez. Ciudad Bolívar, Estado Bolívar. Febrero-marzo 2007.
Métodos: Se analizaron 50 muestras por triplicado, obtenidas por extracción mecánica a donadoras de leche humana. Se determinaron acidez titulable por el método Dornic, recuento de bacterias aerobias mesófilas según Norma Venezolana COVENIN 902-87, y se relacionaron ambas variables. Para el análisis estadístico se utilizó la media aritmética, prueba de Chi cuadrado y coeficiente de correlación de Pearson.
Resultados: un 78% de las muestras (n=37) presentaron acidez titulable aceptable (1ºD a 8ºD), 22% restante (n=13) fueron no aceptables, (>8ºD a 20ºD). Hubo desarrollo microbiano en 100% de las muestras, con valores hasta 105 UFC/mL. Al relacionar acidez titulable con carga bacteriana total se obtuvo un coeficiente de correlación r =0,79; con tendencia positiva y relación lineal de las variables.
Conclusión: La acidez titulable en grados Dornic refleja de manera directa el grado de contaminación bacteriana que posee la leche humana, considerándose adecuada como prueba fisicoquímica de control de calidad.
Palabras clave: Acidez titulable, grados Dornic, carga microbiana, leche humana, Banco de Leche Humana.
SUMMARY:
Assessment of titratable acidity is a test of physical chemistry quality control for human milk that should be performed routinely as a qualifier parameter in human milk banks.
Objective: To analyze the titratable acidity as quality control for human milk in the Milk Bank of the University Hospital Complex "Ruiz y Páez" Ciudad Bolivar, Bolivar state, between February and March 2007.
Methods: 50 samples obtained by mechanical extraction of human milk donors were analyzed in triplicate. Titratable acidity by the Dornic method and bacterial aerobic mesophilic count according to Venezuelan Standard COVENIN 902-87 were assessed. Statistical analysis was performed by the arithmetic mean, Chi-square test and Pearson correlation coefficient.
Results: 78% of the samples (n = 37) presented acceptable acidity (1 º D-8 º D), and 22% (n = 13) were not acceptable (> 8 º to 20 º D). Microbial development was detected in all samples, with values up to 105 CFU / mL. A positive relation was found between titratable acidity and total bacterial load (r=0,79).
Conclusion: Titratable acidity reflects the degree of bacterial contamination of human milk and can be regarded as an adequate test for physical chemistry quality control.
Key words: Titratable acidity, Dornic degrees, microbial load, human milk, human milk banks.
INTRODUCCION:
La historia de la lactancia materna es tan antigua como la humanidad y se considera un componente fundamental en la alimentación infantil, en la que la supervivencia del niño depende exclusivamente de la aplicación de una adecuada lactancia. Se entiende por lactancia materna el proceso de alimentación de la madre a su hijo utilizando la secreción de sus mamas (1).
Hay circunstancias en las cuales la madre no puede suministrar a su hijo una lactancia materna exclusiva, entendida como la alimentación de un niño o niña lactante hasta los seis meses de edad exclusivamente con leche materna, sin el agregado de agua, jugos, té u otros líquidos o alimentos, tal como lo señala la Ley Nacional de Promoción y Protección de la Lactancia Materna (2). Cuando por alguna razón no se lleva a cabo el amamantamiento directo, existe la alternativa de acudir a los lactarios, que son sitios específicos destinados a la extracción mecánica o manual de leche materna no procesada, para distribución homóloga (3), o a los Bancos de Leche Humana (BLH), que son centros especializados responsables de la promoción, protección y apoyo de la lactancia materna, de la ejecución de actividades como extracción, procesamiento y controles de calidad de la leche humana; a su vez se encargan de entrenar, asesorar, capacitar recursos humanos y desarrollar investigaciones científicas (4).
A principios del siglo XX hubo un reconocimiento del aumento de la morbimortalidad relacionada con el consumo de preparados para lactantes. En respuesta a este problema se crearon los primeros BLH, sobre todo para la alimentación de los recién nacidos pre-término y enfermos. En 1909 se estableció en la ciudad de Viena, en Austria, el primer BLH. Por su parte, en EEUU el primer BLH fue establecido en Boston, Massachusset en 1910(5). En Latinoamérica, Brasil inició con los mismos en 1943, y posteriormente crearon la Red Nacional de Bancos de Leche FIOCRUZ, desde la cual se dictan las normas de funcionamiento para los Bancos de Leche de Venezuela.
En Venezuela, el primer BLH se fundó en el año 1986 en el Hospital Universitario de Caracas (6) y actualmente existen siete BLH vinculados a hospitales que cuentan con servicios de Obstetricia, Pediatría y Neonatología.
En estos BLH se realizan de rutina controles fisicoquímicos a la leche humana donada, los cuales evalúan ciertos parámetros como son: color, sabor, olor, crematócrito y acidez titulable método Dornic; éste último se define como el número de décimas de ml. de NaOH N/9 necesarios para neutralizar frente a la fenolftaleína 1 ml de leche (7).
La acidez de la leche humana en grados Dornic (°D) es determinada por el equilibrio entre los componentes ácidos de la leche como son fosfatos, citratos, carbonatos, hidroxilos y proteínas; y los componentes básicos que incluyen sodio, potasio, calcio, magnesio e hidrógeno. La Red de Bancos de Leche Humana de Brasil, sugirió un método de determinación de acidez titulable estandarizado según criterios de la Norma BLH-IFF/NT 29.04, la cual señala que la leche humana que presente acidez Dornic mayor a 8,0°D será considerada impropia para consumo (8).
La acidez de la leche humana puede ser clasificada como original y desarrollada. La original resulta de la presencia de sus constituyentes, y la desarrollada deriva del ácido láctico, producido a partir del crecimiento bacteriano. Dependiendo de la técnica utilizada para la determinación de la acidez, ésta puede ser denominada actual y titulable. La acidez actual es determinada con potenciómetros y sus valores son expresados en pH. En virtud del sistema tampón natural de la leche, para que ocurran cambios de pH de 0,1 unidades es necesario una elevación importante de la acidez; por esta razón se descalifica el pH como indicador eficaz de acidez por su baja sensibilidad. Se prefiere entonces la acidez titulable, que se determina por medio de una reacción estequiométrica entre un titulante alcalino y los constituyentes ácidos de la leche humana hasta que ocurre la neutralización (8).
En los BLH, además de las pruebas fisicoquímicas, se realizan determinaciones microbiológicas. El perfil microbiológico de los alimentos en general, incluye las determinaciones de Staphylococcus spp y coliformes totales fecales como indicadores de manipulación y sanitarios respectivamente; así como, el contaje total de aerobios mesófilos; estas pruebas constituyen parámetros clasificatorios de la leche (8,9).
La carga bacteriana total se determina mediante el contaje de bacterias aerobias mesófilas, todas las bacterias patógenas conocidas, transportadas por el agua y los alimentos son mesófilas; este grupo de microorganismos forma parte de la clasificación de bacterias según sus rangos de temperatura de crecimiento, pues se desarrollan en placa de agar a 30-37ºC, estando su temperatura óptima de crecimiento entre 30º y 45ºC (9).
Las condiciones de higiene del lugar en el cual se colecta la leche humana son importantes en la contaminación inicial que ésta pueda presentar (10). En una investigación realizada en el BLH de Ciudad Bolívar, Venezuela, se reportó la presencia de aerobios mesófilos, estafilococos y coliformes totales al analizar 30 muestras de leche humana antes de la pasteurización. Luego de efectuar el proceso de pasteurización, se determinó ausencia de microorganismos en todas las muestras procesadas (11).
En vista de la seguridad microbiológica que debe poseer la leche humana para garantizar su inocuidad y tomando en cuenta que la prueba de acidez titulable es un parámetro clasificatorio en los Bancos de Leche, el objetivo de este estudio fue analizar la acidez titulable como prueba de control de calidad para la leche humana correlacionándola con la carga microbiana total en muestras del Banco de Leche Humana del Complejo Hospitalario Universitario Ruiz y Páez de Ciudad Bolívar, Estado Bolívar.
METODOS
Se realizó un estudio prospectivo, descriptivo, con muestras de leche humana de madres que asistieron al Banco de Leche del Complejo Hospitalario Universitario Ruiz y Páez entre los meses de febrero a marzo del año 2007. Los criterios de inclusión fueron: madres sanas en periodo de lactancia, con edades comprendidas entre 15 y 35 años, embarazo controlado, seronegativas para el Virus de Inmunodeficiencia Humana (VIH) y prueba de VDRL con resultado no reactivo.
La toma de la muestra se llevó a cabo en las instalaciones del BLH, con todas las medidas de higiene del caso. Previo retiro de blusa, sujetador y prendas, se le indicó a la madre donante el uso de bata estéril con abertura hacia delante, gorro y tapaboca. Luego del lavado de manos con agua y jabón, lavado de mamas con agua y secado con gasa estéril, se procedió a la toma de muestra mediante la colocación de las copas de la bomba eléctrica extractora, marca Medela® previamente esterilizadas durante 15 minutos aproximadamente; siempre con la asistencia del personal del servicio.
La cantidad de leche extraída de cada madre varió desde 15 mL hasta 150 mL, según su producción individual. La misma fue depositada en un envase de vidrio estéril e inmediatamente se procedió a separar con pipeta estéril la alícuota (5 ml) para realizar las determinaciones de aerobios mesófilos y acidez Dornic, el resto de la leche fue conservada para cumplir la rutina propia del BLH.
De la alícuota de 5 ml de leche humana recién extraída, previa homogenización manual, se transfirió 1 ml a cada uno de tres tubos de ensayo de 10 x 100 mm para la determinación triplicada de acidez Dornic. La acidez titulable método Dornic se realizó según la técnica estandarizada utilizada en los BLH de Brasil, la cual establece que a cada tubo contentivo de 1 ml de leche humana se adicionan 2 gotas de solución indicadora de fenolftaleína hidroalcohólica al 1% p/v, posteriormente se titula con NaOH N/9 con ayuda de una microbureta o acidímetro con escala de 0,01 ml. Cada 0,01 ml de NaOH usado para neutralizar 1 ml de leche humana corresponde a 1 grado Dornic (°D) o acidez de la leche. La aparición de un color rosa pálido indica el punto final de la reacción.
Para el recuento de aerobios mesófilos o contaje total de microorganismos se utilizaron los 2 ml de leche humana restante de la alícuota. Con 1 ml de leche se realizaron tres diluciones decimales con agua peptonada (9 mL) al 0,1%, y se procedió a realizar siembra en profundidad, al igual que con el ml de la muestra pura en agar Plate Count por duplicado a 32+/- 1° C por 24 horas, según Norma Venezolana COVENIN 902-87. Los resultados se expresaron como recuento estándar por mililitro de muestra. El número de colonias obtenido se multiplicó por la dilución correspondiente y se expresó como UFC/ml.
Para el análisis estadístico se utilizó el programa Statistical Package for the Social Sciences (SPSS) versión Windows 2006. Los datos se presentaron en cuadros de distribución de frecuencias absolutas y porcentuales, usando Chi cuadrado para establecer la independencia de las muestras. Para el análisis de correlación de las variables acidez Dornic y recuentos de aerobios mesófilos se utilizó la prueba de correlación de Pearson con un nivel de significación estadística p < 0,05.
RESULTADOS:
En el cuadro 1 se observa la frecuencia de muestras aceptables o no, según la acidez titulable y se evidencia que de 50 muestras analizadas, en 78% de los casos (n=39) los títulos de acidez de la leche humana se catalogaron como aceptables. En el 22% restante (n=11), los valores de acidez titulable obtenidos fueron superiores a 8,0º D, llegando hasta valores de 20º D, considerados como no aceptables (Cuadro 1).
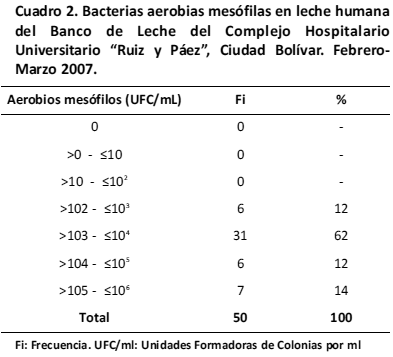
El cuadro 2 muestra la carga bacteriana total dividida en rangos con base a las diluciones decimales en las muestras de leche humana. En todas las muestras hubo crecimiento bacteriano y además, no se encontraron aerobios mesófilos en cantidad menor a 1,0x102 UFC/ml. El desarrollo de microorganismos aerobios mesófilos se cuantificó desde un mínimo de 1,1x102 UFC/ml hasta >105-≤106 UFC/ml como máximo. El rango de diluciones decimales donde se ubicó la mayor proporción de muestras fue el comprendido entre >103 - ≤104 UFC/ml, con 62% de las muestras analizadas (n=31); mientras que en el rango más alto se encontró un 14% de las muestras (n=7), es decir, entre >105 y ≤106 UFC/ml.
La correlación de la acidez Dornic y recuento de aerobios mesófilos, según el coeficiente de Pearson, muestra relación estadísticamente significativa (p<0,001), con tendencia positiva y relación lineal de las dos variables cuantitativas (Figura 1).
DISCUSION:
En esta investigación se evidenciaron valores de acidez titulable entre 1ºD y 8ºD (aceptables) en una alta proporción de las muestras de leche humana analizadas, y resultados entre 8 y hasta 20ºD (no aceptables) en el resto de los casos. Estudios de aspectos fisicoquímicos de la leche humana cruda y congelada, han registrado valores de acidez titulable menores o iguales a 7ºD (13), e investigaciones sobre la calidad de la leche humana han reportado valores aceptables en el 98,1% de los casos, entre 2ºD y 8ºD (14). Valores no aceptables de hasta 21ºD, han sido hallados al determinar la acidez titulable como control de calidad en leche humana (15).
Son admisibles las variaciones en la acidez titulable; luego de recolectar y almacenar muestras de leche humana en Bancos de Leche, se ha señalado que este parámetro varía en la leche de diversas donantes, así como en muestras del mismo donante; sugiriendo esta variación como parámetro de calidad higiénico-sanitaria, sin tomar en cuenta la oxidación lipídica que ocurre en el almacenamiento (16).
La carga microbiana total en las muestras de leche humana analizadas en esta investigación, evidenciaron contajes de aerobios mesófilos desde un mínimo de 1,1x102 UFC/ml hasta un máximo de >105 - ≤106 UFC/ml. Todos los valores incluidos en estos rangos se consideran dentro de los criterios microbiológicos para leche humana. Resultados similares y con recuentos menores de 105 UFC/ml han sido reportados en muestras de leche sin pasteurizar (11,17); así como, 100% de positividad para bacterias mesófilas con un 20% de los contajes en límites aceptables (18). Se han encontrado hallazgos superiores en diversas investigaciones. En evaluación de muestras de leche humana cruda se reportó que en todas existían bacterias mesófilas con variaciones en los contajes desde 10 hasta 108 UFC/mL (19); se ha señalado 40% de positividad de bacterias mesófilas con 23% de presencia de microorganismos patógenos y menor número de cultivos positivos entre las muestras extraídas manualmente y mantenidas en refrigeración (20). Otros autores han determinado contajes de bacterias aerobias mesófilas de hasta 106 UFC/ml y asumen como criterio microbiológico de referencia que una leche humana de calidad óptima debe tener menos de 2,5 x 103 UFC/ml (12,21).
En Venezuela no existe norma que estandarice los recuentos microbiológicos en leche humana, por lo cual se toman criterios de referencia de otros países. Reino Unido por ejemplo, establece que antes del proceso de la pasteurización no debe encontrarse crecimiento bacteriano superior a 105 UFC/ml (22); en Los Estados Unidos de Norteamérica, la asociación de bancos de leche humana de Norte América (Human Milk Banking Association of North America) señala que la leche extraída no debe tener bacterias patógenas, o no más de 104 UFC/ml de recuento total (5). En Brasil, se señala que las muestras de leche humana cruda se consideran apropiadas para el consumo si la cuenta de bacterias mesófilas es menor de 2,5 x 103 UFC/ml, y hacen énfasis en que la pasteurización mejora su calidad microbiológica (14). A menor grado de contaminación inicial la pasteurización es más efectiva para el control microbiológico (23).
Al relacionar la acidez titulable con la carga microbiana total de las mismas, se encontró que un incremento en el grado de acidez tiene relación directa y significativa con el aumento de carga bacteriana total en las muestras de leche humana estudiadas, la mayoría de muestras que presentaron ºD superiores a 8, fueron las que mostraron mayor número de colonias, excepto 5 muestras con acidez mayor de 8ºD con contajes de colonias menor de 2,5 x 103 UFC/ml Esto se pudiera explicar por variaciones individuales con relación a los recuentos de bacterias acidolácticas (productoras de ácido) que posee naturalmente la leche extraída de cada donante. La Red de Bancos de Leche de Brasil señala que la leche humana recién ordeñada que se titula inmediatamente, se presenta prácticamente libre de ácido láctico y su acidez total puede ser considerada original, con valores oscilando entre 1ºD y 4ºD. A medida que su microbiota encuentra condiciones favorables para el crecimiento, como puede ser el almacenamiento, ocurre producción de ácido láctico y la consecuente elevación de la acidez. Cuando estos valores superan los 8ºD, la leche es descalificada para pasar a la etapa de pasteurización y por supuesto, descalificada para el consumo (8). En vista de que los valores elevados de acidez titulable se relacionan de manera directa con el número de bacterias presentes en ella, la determinación de este parámetro como prueba fisicoquímica de control de calidad, adquiere especial interés en los Bancos de Leche Humana.
En conclusión, la acidez titulable en grados Dornic, refleja de manera directa el grado de contaminación bacteriana que posee la leche humana del Banco de Leche del Complejo Hospitalario Universitario Ruiz y Páez, por lo cual se considera adecuada como prueba fisicoquímica de control de calidad.
REFERENCIAS:
1. Stuart-Macadam P, Dettwyler KA. Breastfeeding, Biocultural Perspectives. New York. Aldine de Gruyter; 1995. [ Links ]
2. Ley de Promoción y Protección de la Lactancia Materna de 2007. Nº 38.763. Gaceta Oficial de la República Bolivariana de Venezuela. (Sep. 6, 2007). [ Links ]
3. Secretaría de Salud de México. Centro Nacional de Equidad de Género y Salud Reproductiva. Clínicas de Lactancia en Hospitales Infantiles y Generales Lineamiento. 2006. [Serie en línea] Disponible: www.mujerysalud.gob.mx/contenido/cnegsr.htmL-15k. [consultado: enero2006]. [ Links ]
4. Ley 2102 Banco de Leche Argentina. Sanción: 05/10/2006. Promulgación: Decreto Nº 1.868/006 del 1º/11/2006 Argentina. 2006. [Serie en línea] Disponible: www.ciudadyderechos.org.ar/derechosbasicos_l.php?id=14 & id2=64 & id3=1427-29k [consultado: enero 2006]. [ Links ]
5. HMBANA. Human Milk Banking Association of North America. Human milk banks history. 2005. [Serie en línea] Disponible: http://www.hmbana.org [consultado: enero 2007]. [ Links ]
6. Hernández M. Manual técnico para Bancos de Leche Humana. Hospital Universitario de Caracas. 1999:12-14. [ Links ]
7. Guerra de Almeida J A, Guimarães V, Novak F R. Selección y Clasificación de la Leche humana Ordeñada Cruda, Red Nacional de Bancos de Leche Humana. 2005. [Serie en línea]. Disponible: www.redeblh.fiocrudaz.br. [consultado: enero2007]. [ Links ]
8. Rede Bancos de Leite Humana, REDEBLH. Normas técnicas para bancos de leite humana. 2005. [Serie en línea]. Disponible: www.redeblh.fiocrudaz.br. [consultado: diciembre 2006]. [ Links ]
9. ICMSF. International Commission on Microbiological Specifications for Foods. Ecolog Microbiana Aliments. España. Edit. Acribia; 1980. [ Links ]
10. Novak FR, De Almeida JA, Santos MJ, Wanke B. Contamination of expressed human milk by mycelial fungi. J Pediatr Rio J. 2002; 78(3):197-201. [ Links ]
11. Rosas V, Durán Z, Guevara A, Rodriguez C, Carreño L. Calidad microbiológica de la leche humana procesada en el Banco de Leche, Complejo Hospitalario Universitario Ruiz y Páez. Arch Venez Puer Ped 2008; 71(1): 5-12. [ Links ]
12. Baquero A, Torres M. y Méndez H. Lactarios amigos de la mujer y la infancia. Hospital Occidente de Kennedy, Bogotá; 1998. [ Links ]
13. Cavalcante JL. Aspectos físico-químicos do leite humano ordenhado crude e congelado. Fortaleza; 2001. [ Links ]
14. Almeida SG, Dorea J. Quality Control of Banked Milk in Brasília. Brazil. J of Hum Lact. 2006; 22(3):335-339. [ Links ]
15. Cavalcante, JL, Siquiera F, Lopes M, De Barros R. Uso da acidez titulável no controle de qualidade do leite humano ordenhado. Ciênc Tecnol Aliment. 2005; 25(1):103-108. [ Links ]
16. Galhardo AL, Marques S, Araújo WM, Coelho LA. Acidez Dornic como parâmetro de qualidade, em bancos de leite humano. Hig Aliment. 2002; 16(100): 16-27. [ Links ]
17. De Assis A, Chaves A, Gomes M, Pereira T, Santos M. Perfil Microbiológico do leite materno do Banco da Maternidade Evangelina Rosa, Teresina (Piauí). Bol Centro Pesqui Process Aliment. 2001; 19(1): 75-84. [ Links ]
18. Costa A, Coelho S, Paiva C, Filho S. Caracterização microbiológica do leite humano procesado em banco de leite de João Pessoa - Paraíba/ Brazil. Rev Bras Anal Clin. 2004; 36(4): 225-229. [ Links ]
19. Carvalho C. Avaliação microbiológica de leite humano coletado em banco de leite na cidade de Goiânia/GO. Goiania. 2000. [Serie en línea]. 76 p. Disponible: www.fiocruz.br/redeblh. [consultado: mayo 2007]. [ Links ]
20. Rivera LL, Andonie N, Viril F, Max Dubón JM. Crecimiento bacteriano en leche humana. Rev Med Hond. 1992; 60(1):35-38. [ Links ]
21. Trombino V, Hernández M., De Slgrad M. Efectos de los procesos de higienización sobre la calidad microbiológica de la leche humana extraída en el Banco de Leche del Hospital Universitario de Caracas. Rev Inst Nac Hig Rafael Rangel. 2003; 34(1):10-16. [ Links ]
22. UKAMB, United Kingdom Association for Milk Banking. 2003. [Serie en línea] Disponible: http://www.ukamb.org. [consultado: noviembre 2006]. [ Links ]
23. Serafini AB, Andre MC, Rodrigues MA, Kipnis A, Carvalho CO, Campos MR. Microbiological quality of human milk from a Brazilian milk bank. Rev Saude Pub. 2003; 37(6):775-779. [ Links ]