Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos Venezolanos de Puericultura y Pediatría
versión impresa ISSN 0004-0649
Arch Venez Puer Ped vol.79 no.3 Caracas set. 2016
Hallazgos clínicos y citogenéticos en niñas con Sindrome Turner. Reporte de 6 casos.
Ruth Salas (1), Minijay López Calderón (2), Carmen Rojas (3)
(1) Pediatra. Endocrinólogo. Adjunto del servicio de Pediatría del Hospital Dr. Ángel Larralde. Docente contratada de la Universidad de Carabobo. Valencia- Edo. Carabobo.
(2) Pediatra. Adjunto del servicio de Pediatría del Hospital Dr. Ángel Larralde. Docente de la Universidad de Carabobo. Valencia-Edo. Carabobo.
(3) Pediatra. Endocrinólogo Pediatra. Clínica Ávila. Caracas.
Autor corresponsal: Dra. Ruth Salas, Telf.: 04141155449. Correo: ruthmsalas@hotmail.com
RESUMEN
Introducción: El síndrome de Turner es una disgenesia gonadal. Frecuencia: 1/2500 nacidas vivas. El patrón genético es, 45,XO (mayoría). El diagnóstico es tardío por la variedad del fenotipo. Objetivo: Conocer las manifestaciones clínicas y de laboratorio, en niñas con diagnostico de síndrome de Turner, en la consulta de Endocrinología Infantil del Hospital Universitario Dr. Ángel Larralde, 2009- 2014. Métodos: Estudio descriptivo, no experimental, de corte transversal. Resultados: De 6 niñas con diagnostico de Síndrome de Turner, 3 fueron escolares, 2 adolescentes y 1 preescolar. Entre los cariotipos involucrados: 45,XO (33%), isocromas X (33%), 45,X/46,XX (17%) y 45,X/46,XY (17%). Único motivo de consulta fue talla baja. Todas presentaron cuello corto, micrognatia y tronco ancho. Frecuencia de malformaciones: 4 niñas presentaron cardiopatías congénitas y 2 malformaciones renales. Un caso de gonadoblastoma asociado a 45,X/46,XY. Conclusión: El retardo en el diagnóstico es un factor que eleva la morbi-mortalidad. El tratamiento debe ser multidisciplinario.
Palabras clave: Síndrome de Turner, talla baja, gonadoblastoma.
Clinical findings and cytogenetic in girls with Turner Syndrome. Report 6 cases.
ABSTRACT
Introduction: Turner syndrome is a gonadal dysgenesis. Frequency: 1/2500 live female births. The genetic pattern is 45,XO. Late diagnosis is probably due to the variety of the phenotype. Objective: To describe the clinical presentation and laboratory findings in girls referred to the endocrinology outpatient clinic of the Hospital Dr. Ángel Larralde, 2009-2014. Methods: Descriptive, non experimental and cross-section study. Results: 6 girls had the cytogenetic diagnosis. 3 were school children, 2 teens and 1 preschool. The karyotypes were: 45,XO (33%), isocromes (33%) 45,X/46,XX (17%) and 45,X/46,XY (17%). Short stature was the reason for consultation in all cases. Clinical findings: short neck, micrognathia and wide trunk (100%); malformations: cardiac (67%), renal (34%). One of the girls presented a gonadoblastoma with karyoype 45,X/46,XY Conclusion: Delay in diagnosis is a factor that raises morbi-mortality. Treatment should be multi-disciplinary.
Key words: Turner Syndrome, short tall, gonadoblastoma.
Recibido: 21-4-16
Aceptado: 23-8-16
INTRODUCCIÓN
El Síndrome de Turner, se define como una disgenesia gonadal. Cuya frecuencia es de 1 caso por cada 2500 recién nacidas vivas (1,2).
En el año 1902, se reportó el primer caso comprobable del síndrome. Algunos anatomopatólogos durante los años 1923 y 1925 describieron la presencia de cintillas ováricas en algunos pacientes. En 1930, el pediatra alemán Otto Ullrich observó en varios pacientes síntomas característicos del Síndrome, al que en 1938 Henry Turner en EEUU dio el nombre. En Europa se conoce también como el Síndrome de Ullrich-Turner (1-3). El patrón genético del síndrome es, 45,XO. Se considera que un 50 a 60% de las pacientes exhiben esta fórmula cromosómica (2,4,5).
En el resto de las pacientes se han descrito otras anomalías citogenéticas, como el mosaicismo de una línea celular 45,X con otra línea celular, lo cual puede ser 46,XX, 46,XY o tener alteraciones estructurales de los cromosomas sexuales. Si en una línea celular se encuentra el cromosoma Y, se incrementa el riesgo de desarrollar tumores gonadales (5,6).
Entre las manifestaciones clínicas se encuentran: talla baja, siendo un hallazgo clínico universal, causada por haploinsuficiencia del gen SHOX, localizado en la región pseudoautosómica del cromosoma X (7,8).
Adicionalmente, estas pacientes presentan desproporción de los segmentos corporales como tronco ancho, con manos y pies largos, cubitus valgus, genus valgum y acortamiento del cuarto metacarpiano. En el desarrollo facial: paladar ojival y micrognatia. Tienen mayor riesgo de presentar subluxación coxofemoral, dislocación patelar, escoliosis y cifosis (7,8).
Entre las malformaciones destacan:
1) Cardiacas congénitas con espectro variable desde defectos triviales a desórdenes severos altamente complejos y resaltando que muchas lesiones son asintomáticas. Entre las más comunes se encuentran la hipoplasia aortica y coartación de la aorta (2,9,10).
2) Renales: riñón en herradura, hidronefrosis, doble sistema excretor, obstrucción de la unión pieloureteral e incluso agenesia renal (2,11).
En algunos casos pueden presentar, neoplasias de células germinales, especialmente en individuos con gónadas disgenéticas que contienen material del cromosoma Y. Entre estas neoplasias, el gonadoblastoma es el más frecuente. La importancia clínica de este hallazgo es que progrese a disgerminoma y a otras neoplasias de mayor malignidad (2,12).
Como puede apreciarse, el síndrome de Turner constituye una disgenesia gonadal poco frecuente, pero con múltiples anormalidades.
La mayoría de los autores coinciden en que el diagnóstico del síndrome de Turner, suele ser tardío, en una proporción importante de casos. A pesar de las características clínicas, el diagnóstico se plantea mucho después del nacimiento. En, aproximadamente el 30% de las niñas con síndrome de Turner no se realiza un diagnóstico correcto (1).
La falla en el diagnóstico es un evento desafortunado porque la morbilidad y mortalidad son más altas en estas niñas que en la población general (1,13).
Sin embargo, la medicina ofrece hoy en día, soluciones suficientemente buenas como para mejorar el pronóstico funcional y por ende, la integración social de estas pacientes. Queda pues de parte del equipo médico realizar los diagnósticos adecuados y tener en cuenta el manejo multidisciplinario, en beneficio del paciente.
Por lo antes expuesto se realizó este estudio cuyo objetivo fue conocer las características clínicas en pacientes con diagnóstico citogenético de Síndrome de Turner que acudieron a la consulta de Endocrinología Infantil del Hospital Universitario Dr. Ángel Larralde, en el periodo 2009- 2014.
MÉTODOS
En la consulta de Endocrinología Pediátrica, que funciona en el Hospital Universitario Dr. Ángel Larralde fueron diagnosticados 6 casos de niñas con Síndrome de Turner entre 2009 y 2014. A todas las pacientes se les realizo historia clínica que incluyó en la exploración física lo relacionado a peso, talla y su comparación con tablas de referencia nacional (14,15). Adicionalmente se solicitaron exámenes complementarios, entre los que se incluyó el estudio citogenetico, y la evaluación por cardiología y nefrología.
El estudio citogenético se realizó en cultivo de 72 horas de sangre periférica según una modificación del método de Moorhead y cols (16). Se colorearon 2 láminas de cada paciente con coloración de bandas G Wright según la técnica de Sánchez (17). En cada caso se analizaron 20 metafases. En dos casos se analizaron 60 metafases y 32 metafases, en vista de que no se detectó alteración con 20 metafases y estas pacientes tenían manifestaciones clínicas sugestivas del síndrome.
El presente trabajo fue un estudio descriptivo, no experimental, de corte transversal.
Los datos recolectados se procesaron con el programa Microsoft Office Excel 2007 y se presentan en cuadros y gráficos de distribución de frecuencias absolutas y relativas. Se corroboró el ajuste de las variables cuantitativas a la distribución normal, mediante la prueba de Kolmogorov-Smirnov y se resumieron con las medidas de tendencia central y de dispersión adecuada, es decir, media y desviación típica. Se hicieron comparaciones de proporciones con la prueba Z, asumiendo un nivel de significancia de p < 0,05.
RESULTADOS
Seis niñas fueron incluidas en el estudio, con diagnóstico genético de Síndrome de Turner, durante el periodo 2009- 2014. La distribución según grupo etario fue: 3 Escolares (50%), 2 adolescentes (33%) y 1 preescolar (17%). La edad mínima fue 5 años, la máxima 15, con promedio de 9,67 y desviación típica de 3,44 años.
Entre los resultados de los estudios cito genéticos, los resultados fueron los siguientes: 2 con cariotipo 45XO (33%), 2 con 46,Xi(X) (33%), 1 caso con 45,X/46,XX (17%) y 1 caso con 45,X/46,XY (17%).
Con respecto al motivo de consulta, fue: Talla baja en todos los casos.
Como parte de la evaluación de medidas antropométricas se determinó la relación peso y talla ajustándose a la edad utilizando las gráficas de la población venezolana. En el 83% de los casos, la relación peso/edad estuvo por debajo del percentil 10 para la curva de referencia nacional Fundacredesa (15).
En cuanto a la talla, para el grupo de escolares, la mínima fue 115 cm, máxima 120,8 cm, media 118,3 cm y desviación estándar de 2,9 cm. En las adolescentes, la talla mínima 123 cm y la máxima de 142 cm, con una media de 132,5 cm y desviación estándar de 13,4 cm. Se reportó un caso en edad preescolar con una talla de 92 cm. Encontrándose todas las pacientes por debajo del percentil 3 para la curva de referencia nacional (15).
Cinco niñas presentaron retardo en la edad ósea de 2 años, con predominio estadísticamente significativo (Z = 1,73; P = 0,04).
De 6 niñas, 4 presentaron cardiopatías congénitas:
.- Prolapso de la válvula mitral: 1 caso (17%) con cariotipo 46,Xi(X).
.- Coartación de la Aorta: 1 caso (17%) con cariotipo 45,XO, cuya manifestación clínica fue hipertensión arterial.
.- Estenosis aortica leve con dilatación aorta ascendente leve: 1 caso (17%) con cariotipo 45,XO.
.- Válvula aortica bicúspide: 1 caso (17%) con cariotipo 45,X/46,XY.
Entre las malformaciones renales, se encontró:
.- Riñón en herradura: 1 caso (17%) con cariotipo 46,Xi(X)
.- Riñón único: 1 caso (17%) con cariotipo 45,X/46,XX.
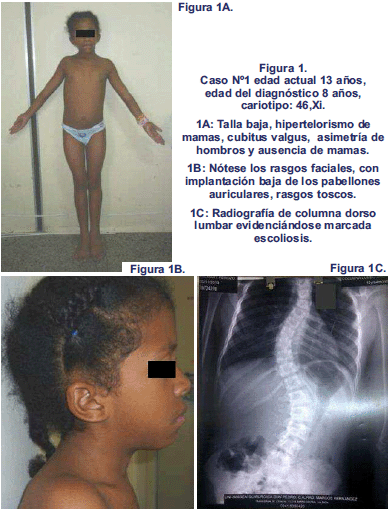
En el presente estudio, el caso identificado con el número 1, presento escoliosis y subluxación coxofemoral, por lo que fue intervenida en 2 oportunidades por el servicio de Ortopedia, persiste con dificultad para la marcha, pendiente otra intervención quirúrgica.
El hallazgo de Gonadoblastoma se evidencio en 1 solo caso, el cual se identificó como caso número 6, con cariotipo 45,X/46,XY. Fue intervenida quirúrgicamente y referida al servicio de oncología pediátrica de la institución. En vista del diagnostico oportuno y la conducta quirúrgica, no amerito tratamiento con quimioterapia hasta la actualidad. Su evolución clínica fue satisfactoria.
En la Tabla 1 se muestran las características clínicas de las 6 pacientes del presente estudio. Figuras 1, 2 y 3


DISCUSIÓN
El Síndrome de Turner (ST) representa uno de los desórdenes cromosómicos más comunes, sin embargo, es considerado por Stochholm y cols., como la única monosomia compatible con la vida. El diagnostico se puede retrasar hasta la adultez en un porcentaje de los casos (1,2).
En el presente estudio, la edad del diagnóstico fue entre 7 y 17 años, coincidiendo con la información nacional reportada por Vera y cols (18). La primera evaluación endocrinológica fue realizada en la adolescencia (18,19). Entre las observaciones realizadas por Schoemaker y cols., resalta la distribución de la edad en la que se hace el diagnóstico, presentando, pues, un comportamiento bimodal, con un pico en la edad neonatal y otro pico en la pubertad (1,20).
La expresión clínica de las niñas con ST, es variada. Mortensen KH y cols., Granger A y cols. consideran que el fenotipo se debe al cariotipo, por lo tanto las niñas con cariotipo 45,XO presentan estigmas más evidentes. El único punto en común fue la talla baja. El inadecuado crecimiento comienza en la vida fetal y se expresa con retardo de crecimiento intrauterino, pudiéndose manifestar durante toda la infancia (2,7,8,14,15,22-24, 26, 27).
La talla baja fue el único motivo de consulta en el presente estudio. Coincide con los resultados obtenidos por Román y cols., con la evaluación de 83 niñas chilenas, quienes presentaron talla baja (100%) y cariotipo 45,XO en el 60% de los casos. Sin embargo aunque la talla baja es considerada como el hallazgo clínico universal, existe la publicación realizada por Ríos Orbañanos y cols., quienes reportaron en un estudio de 45 pacientes con ST, solo el 54% presentaron talla baja, pero con la presencia de mosaicismo en el 63% de los casos. (25,27)
Las manifestaciones clínicas como cuello corto, implantación baja de los pabellones auriculares, micrognatia, tronco ancho e hipertelorismo de mamas, fueron descritas en todos los casos, del presente estudio. Hallazgos similares fueron reportados por Granger y cols., Makishima y cols., en una serie de 91 pacientes con ST, donde el 90% presento uno o más anormalidades craneofaciales que incluyen implantación baja de los pabellones auriculares, micrognatia e implantación baja del cabello (26,28).
Alteraciones esqueléticas como escoliosis, subluxación coxofemoral fueron descritas en una paciente. Coincide con reportes realizados por Mortensen y cols y Davenport, sobre estos hallazgos e incluye además la presencia de cifosis (2,7).
Las pacientes con ST tienen riesgo de alteraciones médicas que requieren cuidado desde la infancia hasta la adultez, de hecho, las cardiopatías representan una causa de mortalidad en este grupo de pacientes. Así, Ríos OrbañanosI y cols., describen el fallecimiento en dos casos de pacientes con ST, por aorta disecante (27).
Asociaciones frecuentes entre Monosomia X y la presencia de cardiopatías fueron observadas por Mortensen y cols (2).
En la presente investigación se reportó cardiopatía en un 67% de los casos. Según Granger y cols., la prevalencia de cardiopatías ha variado a través del tiempo y se deben a la técnica de imagen empleada. Estudios más recientes, entre los que destacan Mortensen y cols., Lee y cols., han evidenciado de un 65 a 70% de al menos una anomalía estructural del corazón y grandes vasos (10,29).
Entre las cardiopatías congénitas encontradas en el estudio, la Coartación de la Aorta se presento en 1 caso (17%). La prevalencia oscila entre 12% y 14% según Ho y cols., Mortensen y cols., siendo esta malformación, la más temida, según Shoemaker y cols., Mortensen y cols., por su implicación de compromiso de la vida del paciente. Así, Turtle y cols., han reportado asociación entre Coartación de la Aorta y Aorta disecante (2,10,13,30,31).
La válvula aórtica anormal en ST, es frecuentemente silente y detectada solo durante la evaluación cardiaca. La presencia de válvula aórtica anormal la hace más propensa a desarrollar endocarditis, pudiéndose además deteriorar a través del tiempo y conllevar a la presencia de estenosis o regurgitación (9,13,18).
La presencia de válvula aortica bicúspide se presento en 1 caso (17%). Según Mortensen y cols., Olivieri y cols., esta lesión valvular es la más común asociada a ST y esta presente en un 13 a 27% de los casos (10,32).
Otras alteraciones fueron observadas en el estudio como: 1 caso con prolapso de la válvula mitral y 1 caso con estenosis aortica leve con dilatación de la aorta ascendente leve, lo cual coincide con estudios realizados por Mortensen y cols, quien la reporta como poco frecuente (10).
Las malformaciones genitourinarias están presentes en niñas con ST. En el presente estudio, 2 niñas (33%) presentaron esta anormalidad. Según Granger y cols., la prevalencia ha variado desde 73% en 1970 según reportes de Matthies y cols., hasta 29% a un 38% según Bilge y cols., Carvalho y cols (26,33-35).
Se presento 1 caso (17%) con riñon en herradura, siendo descrita esta anormalidad por Lippe y cols., Bilge y cols. Sin embargo la prevalencia varía de 7% a 20% de niñas con ST según estudios reportados por Matthies, Lippe y Flynns. Destaca la publicación reciente como la realizada por Je y cols., la cual demostró que el ST, es el síndrome mas común en pacientes con riñón en herradura y esta presente en 4% de niños y adultos jóvenes con esta malformación (33,34,36-38).
Otra alteración descrita como agenesia renal fue observada en el estudio, con 1 caso (17%). Coincide con hallazgos encontrados en la literatura, con igual proporción a la presencia de otras anormalidades como quiste renal, vasos aberrantes, doble sistema colector en aproximadamente el 10% de los casos, según reportes de Lippe, Flynn, Bilge y Carvalho (34-37).
Se reportó en este estudio, 1 caso (17%) de gonadoblastoma, en la paciente con cariotipo 45,X/4,XY. La incidencia de esta neoplasia con cariotipo donde existe cromosoma Y, según Canto y cols., representa un 10% a 30% (12). Sin embargo, en una publicación reciente como la de Ji y cols., se demostró en un estudio con 1409 mujeres, un riesgo total de cáncer para pacientes con ST de 1,34 siendo mayor para tumores sólidos y con la hipótesis de que el cromosoma X juega un rol en la incidencia de los mismos (39).
Lo anteriormente expuesto, son las consideraciones necesarias al estudiar pacientes con síndrome de Turner en la infancia porque conllevan a una serie de anormalidades en la adultez que representan una disminución de la expectativa de vida de dichas pacientes. Por lo tanto es nuestra responsabilidad estudiar este grupo de pacientes y darle el beneficio del manejo multidisciplinario de cada una de ellas con sus particularidades.
REFERENCIAS
1. Stochholm K, Juul S, Juel K, Weis NR, Gravholt CH. Prevalencia, incidencia, retardo en el diagnóstico y mortalidad en el Síndrome de Turner. J. Clin. Endocrinol Metab. 2006; 91:3897-3902. [ Links ]
2. Mortensen KH, Andersen NH, Gravholt CH. Fenotipo cardiovascular en Síndrome de Turner. Integrando genética, Cardiología y Endocrinología. Endocr Rev. 2012; 33(5):677- 714. [ Links ]
3. Carrasco W. Síndrome de Turner. Clínica al día, 1998; 7(2):76-90. [ Links ]
4. Moreno E. Síndrome de Turner: Historia, generalidades y clínica. Disponible:WWW.http://WWW.geocities.com/HotSprings/Villa/7158/inform.htm.11 Consulta: 12 marzo 2015. [ Links ]
5. Yang C, Chapman AG, Kelsey AD, Minks J, Cotton AM, Brown CJ. Inactivación del cromosoma X: mecanismos moleculares desde la perspectiva humana. Hum Genet. 2011; 130(2):175-185. [ Links ]
6. Cheng M. Compensación de la dosificación del cromosoma X y Síndrome de Turner. International Congress series 2006; 1298:3-8. [ Links ]
7. Davenport M. Crecimiento y tratamiento con Hormona de crecimiento en Síndrome de Turner. International Congress series 2006; 1298:33-41. [ Links ]
8. Brinder G. Talla baja debido a deficiencia del SHOX. Genotipo, fenotipo y terapia. Horm Res Paediatr 2011; 75:81- 89. [ Links ]
9. Völkl TM, Degenhardt K, Koch A, Simm D, Dörr HG, Singer H. Anormalidades cardiovasculares en niños y adultos jóvenes con síndrome de Ulrich-Turner. Clin Cardiol, 2005; 28(2):88-92. [ Links ]
10. Mortensen KH, Hjerrild BE, Andersen NH, Sørensen KE, Hørlyck A, Pedersen EM, et al. Anormalidades de la arteria intratorácica principal en síndrome de Turner por resonancia magnética. Cardiol Young 2010; 20(2):191-200. [ Links ]
11. Jones O. Bases genéticas. Medicina maternofetal. Principios y práctica. Philadelphia: Creasy R (eds) WB Saunders, Co; 1994: pp. 29-32. [ Links ]
12. Canto P, Kofman-Alfaro S, Jiménez AL, Söderlund D, Barrón C, Reyes E, et al. Gonadoblastoma en pacientes síndrome de Turner con cariotipo 45X y secuencias de cromosoma Y. Cancer Genet Cytogenet 2004; 150(1):70-72. [ Links ]
13. Schoemaker MJ, Swerdlow AJ, Higgins CD, Wright AF, Jacobs PA. Mortalidad en mujeres con síndrome de Turner en Gran Bretaña: un estudio nacional de cohorte. J Clin Endocrinol Metab 2008; 93(12):4735-4742. [ Links ]
14. Aguirre M, Reyes Y, Ramírez M, Lara M, Briceño Y, Paoli M. Enfoque diagnóstico inicial del paciente con talla baja. Rev Venez Endocrinol Metab. 2013; 11(3):168-179. [ Links ]
15. López-Blanco M, Landaeta-Jiménez M. Manual de crecimiento y desarrollo. Sociedad Venezolana de Pediatría y Puericultura. FUNDACREDESA, 1991, pp. 89-102. [ Links ]
16. Moorhead PS., Nowel PC, Mellmann WJ., Battips DM., Hungerford DA. Preparacion de los cromosomas de cultivos de leucocitos a partir de sangre periférica. Expcell Res. 1960; 20:613-616. [ Links ]
17. Sánchez O., Escobar JI, Yunis JJ. Una técnica de banda simple. Lancet 1971; 2:971-972. [ Links ]
18. Vera L. Síndrome de Turner clásico y sus variantes. Algo más que 45X. Archivos Venezolanos de Puericultura y Pediatría 2006; 69(Supl. 1):61. [ Links ]
19. Salas R. Síndrome de Turner en la infancia. Epidemiología. Presentado en IX Congreso Venezolano de Endocrinología y Metabolismo, 2004. [ Links ]
20. Schoemaker MJ, Swerdlow AJ, Higgins CD, Wright AF, Jacobs PA. Mortalidad en mujeres con síndrome de Turner en Gran Bretaña: un estudio nacional de cohorte. J Clin Endocrinol Metab 2008; 93(12):4735-4742. [ Links ]
21. Canto P, Kofman-Alfaro S, Jiménez AL, Söderlund D, Barrón C, Reyes E, et al. Gonadoblastoma en pacientes síndrome de Turner con cariotipo 45X y secuencias de cromosoma Y. Cancer Genet Cytogenet 2004; 150(1):70-72. [ Links ]
22. Alvarez-Nava F. Aspectos genéticos de la Talla baja. Revisión. Rev Venez Endocrinol Metab. 2008; 6(1):2-6. [ Links ]
23. Landaeta M, Macías C, Fossi M. Tendencia en el crecimiento físico y estado nutricional del niño venezolano. Arch Venez Puer Ped 2002; 65(1):13-20. [ Links ]
24. Méndez Castellano H. Estudio nacional de crecimiento y desarrollo humanos de la República de Venezuela. Ministerio de la Secretaría. FUNDACREDESA. Caracas. 1996, pp. 1226- 1291. [ Links ]
25. Román R. Síndrome de Turner: Crecimiento y descripción clínica en 83 niñas chilenas. Rev Med Chile 2002;130:977-984. [ Links ]
26. Granger A, Zurada A, Zurada-Zielinska A, Gielecki J, Loukas M. Anatomy of Turner Syndrome. Clinical Anatomy 2016;29:638-642. [ Links ]
27. Rios Orbañanos I. Sindrome de Turner: del nacimiento a la edad adulta. Endocrinologia y Nutricion. 2015;62(10):499- 506. [ Links ]
28. Makishima T, King K, Brewer CC, Zalewski CK, Butman J, Bakalov VK, et al. Otolaryngologic markers for the early diagnosis of Turner síndrome. Int J Pediatr Otorhinolaringol. 2009;73:1564-1567. [ Links ]
29. Lee SH, Jung JM, Song MS, Chung WY. Evaluation of cardiovascular anomalies in patients with Turner syndrome using multidetector computed tomography. J Korean Med Sci. 2013;28:1169-1173. [ Links ]
30. Ho VB, Bakalov VK, Cooley M, Van PL, Hood MN, Burklow TR, Bondy CA. Major vascular anomalies in Turner síndrome prevalence and magnetic resonance angiographic features. Circ J. 2004;110:1694-1700. [ Links ]
31. Turtle EJ, Sule AA, Webb DJ, Bath LE. Aortic dissection in children and adolescents with Turner syndrome: Risk factors and management recommendations. Arch Dis Child 2015;100:662– 666. [ Links ]
32. Olivieri LJ, Baba RY, Arai AE, Bandettini WP, Rosing DR, Bakalov V, et al. Spectrum of aortic dilation valve abnormalities associated with aortic dilation across age groups in Turner syndrome. Circ Cardiovasc Imaging. 2013;6:1018-1023. [ Links ]
33. Matthies F, Macdiarmid WD, Rallison ML, Tyler FH. Renal anomalies in Turners syndrome types and suggested embryogenesis. Clin Pediatr (Phila) 1971;10:561–565. [ Links ]
34. Bilge I, Kayserili H, Emre S, Nayir A, Sirin A, Tukel T, et al. Frequency of renal malformations in Turner syndrome: Analysis of 82 turkish children. Pediatr Nephrol 2000;14:1111-1114. [ Links ]
35. Carvalho AB, Guerra Junior G, Baptista MTM, Farria APMD, Marini SHVDL, Guerra ATM. Cardiovascular and renal anomalies in Turner syndrome. Rev Assoc Med Bras 2010;56:655-659. [ Links ]
36. Lippe B, Geffner ME, Dietrich RB, Boechat MI, Kangarloo H. Renal malformations in patients with Turner syndrome: Imaging in 141 patients. Pediatrics 1988;82:852–856. [ Links ]
37. Flynn MT, Ekstrom L, De Arce M, Costigan C, Hoey HM. Prevalence of renal malformation in Turner syndrome. Pediatr Nephrol 1996;10:498-500. [ Links ]
38. Je BK, Kim HK, Horn PS. Incidence and spectrum of renal complications and extrarenal diseases and syndromes in 380 children and young adults with horseshoe kidney. Am J Roengenol 2015;205:1306–1314. [ Links ]
39. Ji J, Zoller B, Sundquist J, Sundquist K. Risk of hematological and solid tumors in malignancy with st and Klinefelter: A national cohort study. Int J Can. 2016;139(4):754-8. [ Links ]