Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Obstetricia y Ginecología de Venezuela
versión impresa ISSN 0048-7732
Rev Obstet Ginecol Venez vol.74 no.1 Caracas mar. 2014
Abordaje del anestesiólogo en pacientes con hipertensión y embarazo
Drs. Mauricio Vasco1, Paulino Vigil-De Gracia2*
1 Especialista en Anestesiología, Cuidados Intensivos y Reanimación, Universidad Pontificia Bolivariana, Medellín, Colombia, Coordinador del comité de Anestesia Obstétrica, Sociedad Colombiana de Anestesia S.C.A.R.E., Anestesiólogo, Clínicas Colsanitas, Bogotá, Colombia.
2 Departamento de Ginecología y Obstetricia del Complejo Hospitalario Dr. Arnulfo Arias Madrid de la Caja de Seguro Social, Panamá, Panamá.
*Autor Correspondiente: Dirección: Unidad de Cuidados Especiales de Ginecología y Obstetricia (CEGO), Departamento de Obstetricia, Complejo Hospitalario Dr. Arnulfo Arias Madrid de la Caja de Seguro Social, Panamá, Panamá. Teléfono 0050766143240, E-mail: pvigild@hotmail.com
RESUMEN
Los aumentos de la presión arterial son una de las principales complicaciones durante el embarazo y se pone en riesgo la salud materna y fetal. El grado de la enfermedad puede variar desde una preeclampsia leve hasta una eclampsia con síndrome HELLP. El adecuado manejo de los trastornos hipertensivos durante el embarazo involucra varios profesionales médicos y entre ellos los anestesiólogos. Se requiere entonces de que los anestesiólogos tengan un conocimiento óptimo sobre el tema para dar el manejo aceptado. El manejo que involucra directamente al anestesiólogo incluye usualmente monitoria adecuada, control de la presión arterial, evitar las convulsiones, uso limitado y adecuado de fluidos, abordaje neuroaxial en labor de parto y cesárea, anestesia general para la cesárea, además del uso correcto de los agentes uterotónicos y cuidados posnacimiento. En esta revisión analizamos detalladamente lo que la evidencia actual sugiere sobre el manejo óptimo dado por el anestesiólogo en pacientes complicadas con preeclampsia/eclampsia.
SUMMARY
Increases in blood pressure are one of the major complications during pregnancy and threatening maternal and fetal health. The degree of the disease can vary from mild preeclampsia to eclampsia with HELLP syndrome. Opportune management of hypertensive disorders during pregnancy involves several medical professionals including anesthesiologists. It then requires that anesthesiologists have an excellent knowledge on the subject to give the management accepted. Management that directly involves the anesthesiologist usually includes adequate monitoring practice, control blood pressure, prevent seizures, limited and appropriate use of fluids, neuraxial approach in labor and cesarean, general anesthesia for caesarean section, the correct use of the uterotonic agents and post birth care. In this review we analyze in detail the current evidence suggested about the optimal management given by the anesthesiologist to patients complicated with preeclampsia/eclampsia.
INTRODUCCIÓN
Los trastornos o desórdenes hipertensivos del embarazo (THE) son un grupo de complicaciones asociadas al embarazo y puerperio, se dividen en cinco subgrupos dependiendo de características particulares. La preeclampsia y eclampsia se observa con una frecuencia que varía entre 2 % y 10 % de todos los embarazos (1,2); además es una de las tres principales causas de muerte materna a lo largo de todo el mundo y en Latino América es la principal causa de muerte materna (3). Se estima que a nivel mundial cada año mueren unas 50 000 mujeres por causas relacionadas con la hipertensión, lastimosamente entre el 95 % y 97 % se observan en países de bajo ingreso per-cápite (4), como los nuestros. También se asocia con alta morbilidad materna y con secuelas que pueden ser incapacitantes. Además la preeclampsia-eclampsia afecta tanto a la madre como a su hijo, de hecho la preeclampsia es una de las principales causas de prematuridad y mortalidad neonatal. La alta morbilidad y mortalidad materna y neonatal son las principales razones por la cual dicha complicación es sujeto de múltiples estudios y de educación médica continua.
Uno de los grandes retos para los médicos que atienden estas pacientes es su manejo correcto, de hecho se involucran muchos profesionales de la salud incluyendo especialistas diferentes a la ginecología y obstetricia como lo son entre otros los intensivistas y anestesiólogos. En esta revisión haremos énfasis en el manejo con que se debe involucrar el anestesiólogo, desde el diagnóstico hasta el manejo posnacimiento.
DIAGNÓSTICO DE HIPERTENSIÓN Y EMBARAZO
A continuación definiremos cada uno de los 5 grupos que integran los THE.
Preeclampsia: La definición de preeclampsia involucra tres variables (1,5): A- Embarazo ≥ de 20 semanas o durante el puerperio, B- Hipertensión, definida como una presión arterial sistólica ≥ a 140 mmHg y/o una presión arterial diastólica ≥ 90 mmHg, tomada al menos dos veces en un lapso entre 4 horas hasta 7 días y C- Proteinuria, definida de dos formas: proteínas en orina de 24 horas ≥ 300 mg o 1+ en tiras reactivas repetida en un lapso de 4 horas hasta 7 días; ≥ 2+ en tira reactiva no requiere repetición.
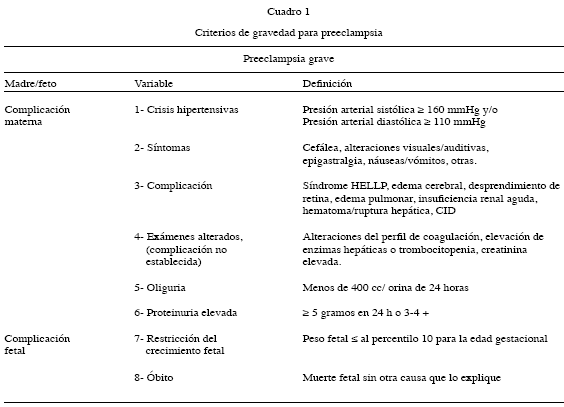
Una vez se cumple con el criterio de preeclampsia se debe considerar la existencia de gravedad o severidad. Se considera grave (severa) si existen uno o más de los siguientes criterios: Crisis hipertensivas, sintomatología, complicaciones con daño a órganos maternos, alteraciones de laboratorio, excesiva pérdida de proteínas y alteraciones fetales, ver Cuadro 1. Toda paciente con preeclampsia debe buscarse por la presencia de uno de esos criterios mencionados, por tanto la ausencia de los 8 criterios establece el diagnóstico de preeclampsia leve, es decir, el diagnóstico de preeclampsia leve es la exclusión de criterios de gravedad. Esta es la razón por la cual para algunos investigadores no debería existir esta sub-división y se debería hablar solo de preeclampsia.
Eclampsia: Cuando ocurren convulsiones asociadas a un trastorno hipertensivo del embarazo (preeclampsia, hipertensión gestacional, preeclampsia agregada) (1,5,6) y se descarta otro trastorno neurológico como por ejemplo epilepsia, malformaciones arteriovenosas, neuroinfección, hipoxia cerebral entre otros. Durante el posparto la gran mayoría de las convulsiones ocurren en las primeras 24 horas, sin embargo, se debe considerar eclampsia, hasta por 8 semanas posparto (4), aunque siempre es necesario descartar otra causa de la convulsión.
Hipertensión crónica: La hipertensión crónica asociada al embarazo se puede diagnosticar con la presencia de presiones arteriales ≥ 140/90 mmHg en 3 situaciones: (1,5) A- La hipertensión crónica conocida o con historia de tal complicación antes del embarazo, B- Hipertensión diagnosticada por primera vez durante las primeras 20 semanas del embarazo (solo si tiene atención prenatal en la primera mitad del embarazo) y C- Hipertensión que persiste luego del puerperio; algunas pacientes fueron clasificadas como preeclampsia o hipertensión gestacional durante el embarazo.
Preeclampsia agregada: (1,7) Es aquella paciente con diagnóstico de hipertensión crónica a la cual, luego de las 20 semanas, se le añade una preeclampsia. El diagnóstico se confirma si la proteinuria ≥ 300 mg/24 horas o en tiras reactivas con proteinuria persistente. Si la paciente tiene una proteinuria previa a las 20 semanas de embarazo superior a 300 mg en 24 horas, la proteinuria actual debe ser superior a ese valor. Usualmente se sospecha de preeclampsia agregada en hipertensas crónicas cuyas presiones arteriales no son controlables, aparecen síntomas o complicaciones, aparecen alteraciones de laboratorio o deterioro de la condición fetal.
Hipertensión gestacional: (1,5,7) Hipertensión que aparece luego de las 20 semanas o en el puerperio y la proteinuria es negativa. Al igual que la preeclampsia su definición involucra tres variables (1,5,6): A- Embarazo ≥ de 20 semanas o durante el puerperio, B- Hipertensión, definida como una presión arterial sistólica ≥ a 140 mmHg y/o una presión arterial diastólica ≥ 90 mmHg, tomada al menos dos veces en un lapso entre 4 horas hasta 7 días y C- Proteinuria, negativa: Proteínas en orina de 24 horas < 300 mg. Al igual que en la preeclampsia podemos tener hipertensión gestacional severa, que son aquellos casos donde se puede presentar una o más de las siguientes alteraciones: crisis hipertensivas, sintomatología, complicaciones con daño a órganos maternos, alteraciones de laboratorio y alteraciones fetales, similar a lo que aparece en el Cuadro 1 sin la proteinuria.
El síndrome HELLP es considerado como una complicación de los desórdenes hipertensivos del embarazo, principalmente observado en pacientes con preeclampsia severa y eclampsia; sin embargo, se puede diagnosticar en pacientes con preeclampsia agregada y en mujeres con hipertensión gestacional. Esta complicación de la preeclampsia-eclampsia se caracteriza por la presencia de anemia hemolítica microangiopática, la cual presenta hemólisis intravascular (H), elevación de las enzimas hepáticas (EL) y descenso del conteo plaquetario (LP). Entre un 4 % y 20 % de las pacientes con preeclampsiaeclampsia se complican con síndrome HELLP (8,9) y estas pacientes presentan alto riesgo de insuficiencia renal, coagulación intravascular diseminada, desprendimiento de placenta, edema pulmonar, edema cerebral, hematoma y ruptura hepática, desprendimiento de retina, choque hipovolémico (9,10).
MANEJO DE HIPERTENSIÓN SEVERA
Después del diagnóstico preeclampsia severa, el tratamiento subsiguiente dependerá de los resultados de la evaluación inicial materna y fetal, sin embargo, el tratamiento definitivo es el parto (nacimiento); el cual es lo más apropiado para la madre, pero para un feto prematuro puede ser la peor conducta.
El manejo de la paciente con preeclampsia severa lo podemos dividir en dos objetivos básicos; primero: el manejo de las crisis hipertensivas y segundo: evitar o tratar las convulsiones.
Antihipertensivos: Esencialmente, toda paciente con preeclampsia severa debe estar hospitalizada. Tratar la hipertensión leve no ha mostrado beneficios maternos ni fetales; en la hipertensión severa (tensión arterial sistólica >160 mmHg y/o diastólica >110 mmHg) no hay duda sobre la utilidad de los antihipertensivos (11,12). El objetivo es realizar una pequeña reducción en la presión sanguínea a niveles seguros para la madre y el feto, evitando caídas bruscas. Actualmente no hay evidencia de cual antihipertensivo es mejor (11,12).
Se decide iniciar los antihipertensivos cuando la presión sistólica es ≥ a 160 mmHg o cuando la diastólica es ≥ a 110 mmHg. El objetivo es mantener una presión diastólica entre 90 y 100 mmHg pues presiones más bajas representan riesgo fetal, por la posible disminución del flujo útero placentario y riesgos cerebrales maternos. Los antihipertensivos más usados en nuestro medio son: la hidralazina a razón de 5 mg intravenoso cada 15 minutos y se repite si es necesario por tres a cinco veces, en caso de no tener hidralazina o no haber respuesta se recomienda labetalol a razón de 20 mg intravenoso y si no hay disminución adecuada de la presión arterial se dobla la dosis a los 10-20 minutos luego y de ser necesario esta última dosis se dobla y de ser necesario se puede repetir tres veces esta última dosis. La otra opción es nifedipina por vía sublingual u oral a dosis de 10 mg cada 15 minutos hasta cinco dosis. Con nuestra experiencia podemos afirmar que el 100.% de las pacientes con preeclampsia-eclampsia y crisis hipertensivas responden a estos medicamentos (11), o a la interrupcción del embarazo. Existen una serie de medicamentos que se han usado como antihipertensivos, sin embargo, la evidencia actual sugiere no usarlos por sus efectos secundarios o por su poca utilidad, forman parte de este grupo el sulfato de magnesio, la nimodipina, ketanserine, diazóxido y clorpromazina.
PREVENCIÓN DE ECLAMPSIA
Como mencionamos previamente, además de evitar las crisis hipertensivas, debemos evitar las convulsiones.
Anticonvulsivante: En cuanto a la prevención y tratamiento de las convulsiones en la preeclampsia severa, definitivamente el sulfato de magnesio es el mejor medicamento existente y probado para evitar las convulsiones de una paciente con trastorno hipertensivo del embarazo (1,2). La dosis de impregnación debe ser de 4 a 6 gramos diluidos en solución salina, lactato ringer o dextrosa en agua y la dosis de mantenimiento debe oscilar entre 1 y 3 gramos intravenoso a dosis continua por 24 horas posparto o posúltima convulsión. Con el sulfato de magnesio se debe vigilar cada hora la diuresis, los signos vitales sobre todo la frecuencia respiratoria. Los efectos secundarios del sulfato de magnesio son pocos, sin embargo, el más temido es la intoxicación y es por eso que la vigilancia debe ser horaria. El antídoto del sulfato de magnesio es el gluconato de calcio al 10 %.
Si se presenta convulsión en vez de usar diazepan lo recomendado es usar 2-4 g de sulfato de magnesio intravenoso y los resultados son mejores (5).
Definitivamente toda paciente con preeclampsia severa debe ser tratada con sulfato de magnesio y antihipertensivos, sin embargo, este tratamiento debe ser más meticuloso si dicha paciente presenta un síndrome HELLP, ya que hemos observado en una revisión reciente que la posibilidad de muerte materna es mayor si la paciente que convulsiona tiene un síndrome de HELLP o trombocitopenia al momento de convulsionar (13).
MONITORÍA
Las pacientes con THE presentan dos perfiles hemodinámicos definidos por catéter de arteria pulmonar (CAP); el más frecuente (80 %) se caracteriza por un aumento en el gasto cardíaco, aumento de resistencias vasculares sistémicas y presiones de llenado normales o discretamente bajas; el resto de pacientes presenta un patrón de gasto cardíaco normal o bajo con aumento importante en las resistencias vasculares sistémicas y presiones de llenado altas (14). La ecocardiografía trastorácica muestra la mayoría de veces un patrón hiperdinámico, leve vasoconstricción y disfunción diastólica en preeclampsia no tratada (15). La evaluación en los gases arteriales de la base exceso al ingreso (Base exceso, EB > -8) puede definir un subgrupo con mayor riesgo de disfunción orgánica, síndrome HELLP y desenlaces adversos neonatales (16). El papel de biomarcadores como el péptido natriurético cerebral (BNP) para caracterización hemodinámica está por definirse, hasta el momento el BNP puede predecir complicaciones cardiovasculares y parto pretérmino (17).
Desde el año 1993 el Colegio Americano de Obstetras y Ginecólogos (ACOG) emitió recomendaciones para la monitoría invasiva de pacientes con THE (18):
Catéteres venosos centrales
La medición de la presión venosa central (PVC) es controversial porque si es mayor de 4 mmHg se correlaciona poco con las presiones de oclusión del capilar pulmonar (PCWP).
Indicado en pacientes con oliguria (< 30 mL / 3 horas) sin respuesta a expansión modesta de fluidos.
Utilización de fármacos vasoactivos parenterales. Catéter de arteria pulmonar (19,20).
No hay evidencia que soporte su uso rutinario en THE severo.
PVC que no se correlaciona con el grado de oliguria (mayor de 4 mmHg).
Compromiso cardiorrespiratorio (edema pulmonar, cianosis).
Enfermedad cardíaca preexistente o coexistente.
Definir el perfil hemodinámico para orientar terapia vasoactiva. Línea arterial:
Sería deseable utilizarla de rutina en preeclampsia severa.
Cuando se anticipa análisis frecuente de gases arteriales (edema pulmonar, necesidad de ventilación mecánica).
Uso de vasodilatadores parenterales arteriales potentes (nitroprusiato, nicardipina, nitroglicerina)
Enfermedad cardíaca preexistente o concomitante.
Anestesia general.
Obesidad.
PAPEL DE LA MONITORÍA MÍNIMAMENTE INVASIVA
La utilización CAP es una medida operador dependiente y con probabilidad de complicaciones graves por lesiones vasculares, arritmias o interpretación inadecuada de los datos derivados luego de su colocación. No existen actualmente estudios de buena calidad que soporten su uso rutinario en pacientes con preeclampsia (19,20); (disponemos actualmente de tecnologías de monitoría mínimamente invasivas del gasto cardíaco que obviarían el uso del CAP, las tecnologías que dependen del análisis de la onda de pulso) necesitarían la colocación de una línea arterial (VIGILEO®, LiDCOplus®, PiCCOplus®), otras tecnologías como la bioimpedancia (21) y la biorreactancia no requieren de la utilización de línea arterial. La biorreactancia (22), NICOM system®, es la menos afectada por artefactos e interferencia electromagnética. Existen múltiples reportes de estas tecnologías para evaluar el perfil hemodinámico asociado a técnicas analgésicas/anestésicas en embarazadas y algunas como el LiDCOplus® ya han sido validadas en el manejo periparto de pacientes con preeclampsia severa al compararlas con CAP (23).
MANEJO DE FLUIDOS
Luego de la hemorragia intracerebral, la causa más frecuente de mortalidad materna es el edema agudo de pulmón (13). La expansión de volumen con cristaloides o coloides de manera rutinaria no está indicada y puede incrementar el riesgo de edema pulmonar agudo y mortalidad sin mejorar desenlaces maternos o fetales (24-26). Adicionalmente y a diferencia de pacientes sanas en pacientes con THE no existe evidencia que respalde el uso de precarga o cocarga hídrica con el fin de atenuar la hipotensión asociada a técnicas neuroaxiales (27).
Como recomendación general las pacientes pueden recibir entre un máximo 80 mL/ hora, este aporte lo reciben con el sulfato de magnesio para profilaxis de eclampsia, si adicionalmente la paciente tiene otras infusiones por ejemplo: Oxitocina estas se deben concentrar (28); en caso de hemorragia obstétrica o falla renal el remplazo de fluidos ya es individualizado a la situación clínica y guiado por monitoría invasiva o mínimamente invasiva.
En las pacientes que desarrollan oliguria definida como un gasto urinario inferior a 30 mL en 3 horas, los retos de volumen deben ser modestos sin sobrepasar bolos de 250 mL de cristaloides (29), la mayoría de pacientes con 3 bolos de esta cantidad presentarán una respuesta favorable en la diuresis.
ABORDAJE NEUROAXIAL SEGURO
La incidencia de complicaciones mayores luego de abordajes neuroaxiales en población obstétrica es de 1 ⁄ 20 000 – 30 000 en anestesia espinal y de 1 ⁄ 25 000 en analgesia epidural. En la ausencia de contraindicaciones, las técnicas neuroaxiales de analgesia son de elección y deben ser instauradas lo más temprano posible anticipando la caída en el conteo plaquetario (30); la anestesia neuroaxial es el método ideal de anestesia para operación cesárea en pacientes con THE. La alteración de la coagulación más frecuente en los THE es la trombocitopenia. El conteo plaquetario para abordar el neuroeje de manera segura no está definido. Existen tres criterios para tomar la decisión; el conteo plaquetario, la velocidad de la caída en el conteo plaquetario y la presencia de coagulopatía por clínica o laboratorio. Pacientes con conteos plaquetarios por encima de 75 000 sin signos clínicos de coagulopatía y conteo plaquetario previo de las últimas 6 horas sin una caída abrupta (30 % del valor inicial) pueden recibir un abordaje neuroaxial. Si las plaquetas y la deshidrogenasa láctica (LDH) son normales en THE con criterios de severidad es poco probable que las pruebas de coagulación (PT, PTT, fibrinógeno) estén anormales por lo que no se deben indicar de rutina antes del abordaje neuroaxial (31-33). La utilización de tromboelastografía o PFA-100 de manera rutinaria para evaluar la función plaquetaria no está indicada en este grupo poblacional (34-36).
ANALGESIA NEUROAXIAL PARA EL TRABAJO DE PARTO
Las técnicas neuroaxiales de alivio del dolor para el trabajo de parto, técnicas móviles (combinada espinal epidural o concentraciones bajas de anestésico local más opioide vía epidural en volúmenes altos) disminuyen la respuesta presora durante las contracciones, permiten además en caso de cesárea de urgencia titular el anestésico local para obtener una epidural anestésica; se debe abordar de manera temprana o profiláctica el neuroeje siempre y cuando no exista contraindicación (37,38). Cuando existen contraindicaciones como la coagulopatía materna, infección sistémica severa o en el sitio de la punción, hipertensión endocraneana; la analgesia sistémica IV con opioides (remifentanil) por un sistema controlado por el paciente (PCA) y monitoría materna individualizada o la dexmedetomidina, son una buena opción (39,40).
ANESTESIA NEUROAXIAL PARA OPERACIÓN CESÁREA
Las técnicas neuroaxiales son de elección para operación cesárea; la espinal, la combinada espinal epidural (CSE) y la epidural son efectivas; la espinal al ser técnicamente más fácil, presentar bloqueo anestésico de rápida instauración y menor incidencia de hematoma espinal es la técnica más utilizada (41). La hipotensión asociada a técnicas neuroaxiales en pacientes con preeclampsia es menos frecuente que en gestantes sin esta entidad (42); Cuando se presenta hipotensión (disminución en la cifras de PAS < 30 % de la basal o PAM < 110 mmHg) se maneja con bolos de fenilefrina 50-100 μg IV o efedrina 3- 5 mg IV (43).
ANESTESIA GENERAL PARA OPERACIÓN CESÁREA
Puede estar indicada en pacientes con coagulopatía, edema pulmonar agudo y eclampsia; el objetivo primordial es evitar la respuesta presora a las maniobras de laringoscopia e intubación / extubación y evitar la broncoaspiración. El anestesiólogo debe tomarse el tiempo necesario para obtener estos objetivos debido a que la técnica de inducción de secuencia rápida puede tener consecuencias hemodinámicas adversas con hemorragia intracerebral asociada (44,45). Los inductores más utilizados son el tiopental sódico y el propofol, los coadyuvantes incluyen opioides (remifentanil, alfentanil, fentanilo), sulfato de magnesio, lidocaína y labetalol. Cuando se tome la decisión de utilizar opioides la literatura respalda con mejor evidencia la utilización de remifentanilo en dosis de 0,5 - 1 mck/kg IV (46,47). Es prudente aclarar que en situaciones de pérdida de bienestar fetal que requiera de cesárea de emergencia, las técnicas neuroaxiales sino existen contraindicaciones se asocian a mejores desenlaces maternos y neonatales (48). Se debe disponer de un algoritmo y los insumos para el manejo de la vía aérea difícil (49) y el recurso para la atención del neonato.
AGENTES UTEROTÓNICOS
La oxitocina es el agente de elección para la prevención de hemorragia posparto asociada a atonía uterina, estudios de monitoría hemodinámica han mostrado la vasodilatación y aumento del gasto cardíaco que puede producir este agente si se utiliza en bolo IV rápido; se recomienda la utilización de oxitocina 1 – 3 U IV en 60 segundos para evitar estos efectos hemodinámicos adversos (50), seguido por infusiones de oxitocina para 4 horas; el misoprostol es agente de segunda línea para prevención de atonía uterina en caso de no disponer de oxitocina o como coadyuvante a la oxitocina para el tratamiento de la HPP, la metilergonovina está contraindicada en pacientes con THE (51).
MANEJO POSPARTO
Las pacientes con criterios de severidad deben ser manejadas en un ambiente donde se pueda realizar monitoría y vigilancia adecuada (52). La analgesia luego de operación cesárea bajo anestesia espinal se basa en la utilización de morfina intratecal más acetaminofén VO o IV; en caso de coagulopatía que contraindique el uso de técnicas neuroaxiales se recomienda el manejo balanceado con acetaminofén VO o IV más opioides parenterales (morfina – hidromorfona).
Se debe individualizar el uso de antiinflamatorios no esteroideos (AINES) por el riesgo de disfunción renal y disfunción plaquetaria; el bloqueo del plano abdominal transverso (TAP block) está indicado en pacientes sin coagulopatía en los que no se usa morfina intratecal (53). El sulfato de magnesio en infusión parenteral debe mantenerse 24 horas luego de la terminación del embarazo o luego de la última convulsión si esta fue posparto, se debe individualizar su uso en pacientes en falla renal. Se debe realizar una estratificación de riesgo para detección de pacientes en alto riesgo de eventos tromboembólicos, como norma general pacientes con THE y criterios de severidad a las que se les realizó cesárea que no estén con coagulopatía necesitarán tromboprofilaxis farmacológica y/o mecánica (54). La utilización de un protocolo estandarizado y agresivo de manejo en pacientes con síndrome HELLP han mostrado disminución en la morbilidad y mortalidad de las gestantes (55,56).
El beneficio de los corticoesteroides como la dexametasona para mejorar los desenlaces maternos en síndrome HELLP no han mostrado disminución en la mortalidad de las gestantes; actualmente se están aleatorizando pacientes con HELLP tipo I para evaluar los desenlaces maternos y neonatales en este subgrupo de pacientes (57,58).
CONCLUSIONES
El anestesiólogo es integrante fundamental del grupo interdisciplinario de manejo en pacientes con THE y criterios de severidad. La estabilización inicial de estas pacientes incluye el manejo adecuado y racional de fluidos, la utilización de sulfato de magnesio para prevención y/o tratamiento de la eclampsia, el manejo de la crisis hipertensiva y la detección de coagulopatía. Se debe monitorizar adecuadamente las pacientes con el fin de definir su perfil hemodinámico y riesgo de complicaciones. Las intervenciones neuroaxiales analgésicas y/o anestésicas son las de elección cuando no están contraindicadas. La anestesia espinal es segura, se asocia a menor hipotensión que en pacientes sin THE y el uso de vasopresores para manejo de la hipotensión asociado a técnicas neuroaxiales es más indicado que la expansión de volumen rutinaria. El cuidado posparto es fundamental con el fin de la detección y/o tratamiento de complicaciones maternas, se debe disponer de recursos adecuados para el manejo del neonato.
REFERENCIAS
1. National High Blood Pressure Education Program Working Group Report on high blood pressure in pregnancy. Am J Obstet Gynecol. 2000;183(Suppl):1-23. [ Links ]
2. The Magpie Trial Collaborative Group. Do women with preeclampsia, and their babies, benefit from magnesium sulphate? The Magpie Trial: A randomized placebo controlled trial. Lancet. 2002;359:1877-1890.
3. Khan KS, Wojdyla D, Say L, Gülmezoglu AM, Van Look PFA. Who analysis of causes of maternal death: A systematic review. Lancet. 2006;367:1066-1074. [ Links ]
4. Villar J, Say L, Shennan A. Methodological and technical issues related to the diagnosis, screening, prevention, and treatment of preeclampsia and eclampsia. Int J Gynaecol Obstet. 2004;85(Suppl):28-41. [ Links ]
5. NHS. National institute for health and clinical excellence. Hipertension in pregnancy. The management of hypertensive disorders during pregnancy. Issue date: August 2010.
6. Steegers EA, von Dadelszen P, Duvekot JJ, Pijnenborg R. Preeclampsia. Lancet. 2010;376(9741):631-644. [ Links ]
7. Uzan J, Carbonnel M, Piconne O, Asmar R, Ayoubi JM. Preeclampsia: Pathophysiology, diagnosis, and management. Vasc Health Risk Manag. 2011;7:467- 474. [ Links ]
8. Sibai BM. Diagnosis, controversies, and management of the syndrome of hemolysis, elevated liver enzymes, and low platelet count. Obstet Gynecol. 2004;103:981-991. [ Links ]
9. Vigil-De Gracia P. Pregnancy complicated by preeclampsia-eclampsia with HELLP syndrome. Int J Obstet Gynecol. 2001;72:17-23. [ Links ]
10. Vigil-De Gracia P, Tenorio-Marañón RF, Cejudo- Caranza E, Helguera-Martinez A, García-Cáceres E. Diferencias entre preeclampsia, syndrome de HELLP y eclampsia: Evaluación materna. Gin Obstet Mex. 1996;64:337-382. [ Links ]
11. Vigil-De Gracia P, Lasso M, Ruiz E, Vega-Malek J, Tem de Mena F, López J. Severe hypertension in pregnancy: Hidralazine or labetalol. A randomised clinical trial. Eur J Obstet Gynecol. 2006;128:157- 162. [ Links ]
12. Duley L, Meher S, Jones L. Drugs for treatment of very high blood pressure during pregnancy. Cochrane Database of Systematic Reviews 2013, Issue 7. Art. No.: CD001449. DOI: 10.1002/14651858.CD001449. pub3.
13. Vigil-De Gracia P. Maternal deaths due to eclampsia and HELLP syndrome. Int J Obstet Gynecol. 2009;104:90-94. [ Links ]
14. Young P, Johanson R. Haemodynamic, Invasive and echocardiographic monitoring in the hypertensive parturient. Best Pract Res Clin Obstet Gynaecol. 2001;15(4):605-622. [ Links ]
15. Dennis AT, Castro J, Carr C, Simmons S, Permezel M. Haemodynamics in women with untreated preeclampsia. Anaesthesia. 2012;67(10):1105-1018. [ Links ]
16. Wheeler TC, Graves CR, Troiano NH, Reed GW. Base deficit and oxygen transport in severe preeclampsia. Obstet Gynecol. 1996;87(3):375-379. [ Links ]
17. Afshani N, Moustaqim-Barrette A, Biccard BM, Rodseth RN, Dyer RA. Utility of B-type natriuretic peptides in preeclampsia: A systematic review. Int J Obstet Anesth. 2013;22(2):96-103. [ Links ]
18. ACOG. Invasive hemodynamic monitoring in obstetrics and gynecology. ACOG Technical Bulletin Number 175--December 1992. Int J Gynaecol Obstet. 1993;42(2):199-205.
19. Li YH, Novikova N. Pulmonary artery flow catheters for directing management in preeclampsia. Cochrane Database Syst Rev. 2012; 6:CD008882.
20. Gilbert WM, Towner DR, Field NT, Anthony J. The safety and utility of pulmonary artery catheterization in severe preeclampsia and eclampsia. Am J Obstet Gynecol. 2000;182(6):1397-1403. [ Links ]
21. Da Silva EG, Carvalhaes MA, Hirakawa HS, da Silva EG, Peraçoli JC. Bioimpedance in pregnant women with preeclampsia. Hypertens Pregnancy. 2010;29(4):357-365. [ Links ]
22. Ohashi Y, Ibrahim H, Furtado L, Kingdom J, Carvalho JC. Non-invasive hemodynamic assessment of non-pregnant, healthy pregnant and preeclamptic women using bioreactance. Rev Bras Anestesiol. 2010;60(6):603-613, 335-340. [ Links ]
23. Dyer RA, Piercy JL, Reed AR, Strathie GW, Lombard CJ. Comparison between pulse waveform analysis and thermodilution cardiac output determination in patients with severe preeclampsia. Br J Anaesth. 2011;106(1):77-81. [ Links ]
24. Duley L, Williams J, Henderson-Smart DJ. Plasma volume expansion for treatment of women with preeclampsia. Cochrane Database Syst Rev. 2000;(2):CD001805. [ Links ]
25. Ganzevoort W, Rep A, Bonsel GJ, Fetter WP, van Sonderen L. A randomised controlled trial comparing two temporising management strategies, one with and one without plasma volume expansion, for severe and early onset preeclampsia. BJOG. 2005;112(10):1358- 1368. [ Links ]
26. Ganzevoort W, Rep A, Bonsel GJ, De Vries JI, Wolf H. A randomized trial of plasma volume expansion in hypertensive disorders of pregnancy: Influence on the pulsatility indices of the fetal umbilical artery and middle cerebral artery. Am J Obstet Gynecol. 2005;192(1):233-239. [ Links ]
27. Ramanathan J, Bennett K. Preeclampsia: Fluids, drugs, and anesthetic management. Anesthesiol Clin North Am. 2003;21(1):145-163. [ Links ]
28. CG107 Hypertension in pregnancy 2010: NICE guideline. consultado 15 Agosto 201]. Disponible en: http://www.nice.org.uk/nicemedia/live/13098/50418/50418.pdf.
29. Guidelines for the Management of Hypertensive Disorders of Pregnancy 2008. consultado 15 Agosto 2013. Disponible en: http://www.somanz.org/pdfs/somanz_guidelines_2008.pdf
30. American Society of Anesthesiologists Task Force on Obstetric Anesthesia. Practice guidelines for obstetric anesthesia: An updated report by the American Society of Anesthesiologists Task Force on Obstetric Anesthesia. Anesthesiology. 2007;106:843-863.
31. Leduc L, Wheeler JM, Kirshon B, Mitchell P, Cotton DB. Coagulation profile in severe preeclampsia. Obstet Gynecol. 1992;79:14-18. [ Links ]
32. Barron WM, Heckerling P, Hibbard JU, Fisher S. Reducing unnecessary coagulation testing in hypertensive disorders of pregnancy. Obstet Gynecol. 1999;94(3):364-370. [ Links ]
33. Sultan P, Butwick A. Platelet Counts and Coagulation Tests Prior to Neuraxial Anesthesia in Patients with Preeclampsia: A Retrospective Analysis. Clin Appl Thromb Hemost. 2012. (Epub ahead of print)
34. Sharma SK, Philip J, Whitten CW, Padakandla UB, Landers DF. Assessment of changes in coagulation in parturients with preeclampsia using thromboelastography. Anesthesiology. 1999;90:385- 390. [ Links ]
35. Marietta M, Castelli I, Piccinini F, Neri I, Bertesi M, Facchinetti F, et al. The PFA-100 system for the assessment of platelet function in normotensive and hypertensive pregnancies. Clin Lab Haematol. 2001;23:131-134. [ Links ]
36. Davies JR, Fernando R, Hallworth SP. Hemostatic function in healthy pregnant and preeclamptic women: An assesment using the platelet function analyzer (PFA-100) and thrombelastograph. Anesth Analg. 2007;104:416-420. [ Links ]
37. Dennis AT. Management of preeclampsia: Issues for anaesthetists. Anaesthesia. 2012;67(9):1009-1020. [ Links ]
38. Gogarten W. Preeclampsia and anaesthesia. Curr Opin Anaesthesiol. 2009;22(3):347-351. [ Links ]
39. El-Kerdawy H, Farouk A. Labor analgesia in preeclampsia: Remifentanil patient controlled intravenous analgesia versus epidural analgesia. Middle East J Anesthesiol. 2010;20(4):539-545. [ Links ]
40. Abu-Halaweh SA, Al Oweidi AK, Abu-Malooh H, Zabalawi M, Alkazaleh F. Intravenous dexmedetomidine infusion for labour analgesia in patient with preeclampsia. Eur J Anaesthesiol. 2009;26(1):86-87. [ Links ]
41. Henke VG, Bateman BT, Leffert LR. Spinal anesthesia in severe preeclampsia. Anesth Analg. 2013. [Epub ahead of print]
42. Aya AG, Mangin R, Vialles N, Ferrer JM, Robert C. Patients with severe preeclampsia experience less hypotension during spinal anesthesia for elective cesarean delivery than healthy parturients: a prospective cohort comparison. Anesth Analg. 2003;97(3):867-872. [ Links ]
43. Cooper DW, Sharma S, Orakkan P, Gurung S. Retrospective study of association between choice of vasopressor given during spinal anaesthesia for high-risk caesarean delivery and fetal pH. Int J Obstet Anesth. 2010;19(1):44-49. [ Links ]
44. Neilson J; on behalf of the Centre for Maternal and Child Enquiries. Chapter 3: Preeclampsia and eclampsia. En: Lewis G, editor. Saving Mothers Lives: Reviewing maternal deaths to make motherhood safer: 2006–2008. The Eighth Report of the Confidential Enquiries into Maternal Deaths in the United Kingdom. Br J Obstet Gynecol 2011;118(Suppl 1):1-203.
45. Huang CJ, Fan YC, Tsai PS. Differential impacts of modes of anaesthesia on the risk of stroke among preeclamptic women who undergo Caesarean delivery: A population-based study. Br J Anaesth. 2010;105(6):818-826. [ Links ]
46. Park BY, Jeong CW, Jang EA, Kim SJ, Jeong ST, Shin MH, Lee J, Yoo KY. Dose-related attenuation of cardiovascular responses to tracheal intubation by intravenous remifentanil bolus in severe pre-eclamptic patients undergoing Caesarean delivery. Br J Anaesth. 2011;106:82-87. [ Links ]
47. Yoo KY, Jeong CW, Park BY, Kim SJ, Jeong ST, Shin MH, et al. Effects of remifentanil on cardiovascular and bispectral index responses to endotracheal intubation in severe pre-eclamptic patients undergoing caesarean delivery under general anesthesia. Br J Anesth. 2009;102:812-819. [ Links ]
48. Dyer RA, Els I, Farbas J, Torr GJ, Schoeman LK, James MF. Prospective, randomized trial comparing general with spinal anesthesia for cesarean delivery in preeclamptic patients with a nonreassuring fetal heart trace. Anesthesiology. 2003;99:561-569. [ Links ]
49. Mhyre JM, Healy D. The unanticipated difficult intubation in obstetrics. Anesth Analg. 2011;112(3):648-652. [ Links ]
50. Dyer RA, Piercy JL, Reed AR, Lombard CJ, Schoeman LK. Hemodynamic changes associated with spinal anesthesia for cesarean delivery in severe preeclampsia. Anesthesiology. 2008;108(5):802-811. [ Links ]
51. Rojas-Suarez J, Vigil-De Gracia P. Preeclampsiaeclampsia admitted to critical care unit. J Matern Fetal Neonatal Med. 2012;25(10):2051-2054. [ Links ]
52. Kahn LH, Alderfer RJ, Graham DJ. Seizures Reported With Tramadol. JAMA. 1997;278(20):1661. [ Links ]
53. Abdallah FW, Halpern SH, Margarido CB. Transversus abdominis plane block for postoperative analgesia after Caesarean delivery performed under spinal anaesthesia? A systematic review and metaanalysis. Br J Anaesth. 2012;109(5):679-687. [ Links ]
54. Thrombosis and Embolism during Pregnancy and the Puerperium, Reducing the Risk 2009. consultado 15 Agosto 2013. Disponible en: http://www.rcog.org.uk/files/rcogcorp/GTG37aReducingRiskThrombosis.pdf
55. Haram K, Svendsen E, Abildgaard U. The HELLP syndrome: Clinical issues and management. A Review. BMC Pregnancy Childbirth. 2009;9:8.
56. Martin JN Jr, Brewer JM, Wallace K, Sunesara I, Canizaro A. Hellp syndrome and composite major maternal morbidity: Importance of Mississippi classification system. J Matern Fetal Neonatal Med. 2013;26(12):1201-1206.
57. Katz L, Amorim M, Souza JP, Haddad SM, Cecatti JG. COHELLP: Collaborative randomized controlled trial on corticosteroids in HELLP syndrome. Reprod Health. 2013;10:28.
58. Dexamethasone Efficacy in HELLP I Syndrome, a Multicentric, Double-blind, Placebo-controlled, Randomized Clinical Trial. consultado 15 Agosto 2013. Disponible en: http://clinicaltrials.gov/show/NCT01138839.