Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Obstetricia y Ginecología de Venezuela
versión impresa ISSN 0048-7732
Rev Obstet Ginecol Venez vol.75 no.3 Caracas set. 2015
Citología en base líquida: parámetros de eficacia
Dras. Silvia Emilcy Zambrano Araque*, Mireya González Blanco**
Correspondencia a: silemiz25@hotmail.com
* Especialista en Obstetricia y Ginecología.
** Jefa del Servicio de Ginecología y Directora del Programa de Especialización en Obstetricia y Ginecología de la Universidad Central de Venezuela, con sede en la Maternidad Concepción Palacios.
RESUMEN
Objetivo: Comparar la eficacia de la citología con la utilización de medio líquido en relación con la convencional, en pacientes que acudieron al Servicio de Ginecología de la Maternidad Concepción Palacios.
Métodos: Se llevó a cabo un estudio prospectivo y comparativo, que incluyó a 177 pacientes a las cuales se les realizó ambas citologías (convencional y líquida).
Resultados: Se obtuvieron 114 muestras con células metaplásicas y de la unión escamo- cilíndrica con la citología convencional y 60 con citología en base líquida (P=0,001). Con la citología en base líquida se encontraron menos casos sin exudado inflamatorio, más con exudado moderado, y se diagnosticaron más casos de infección por virus de papiloma humano. Con la técnica convencional se observaron más casos de vaginosis bacteriana. Los resultados citológicos, en relación con las células epiteliales, fueron similares con ambas técnicas: 171 y 157 negativos, 2 y 8 atipias de células escamosas de significado incierto y 4 y 12 lesiones intraepiteliales de bajo grado, para citología convencional y en base líquida, respectivamente. Hubo 23 falsos negativos y 1 falso positivo con la citología convencional mientras que con la citología en base líquida hubo 18 falsos negativos y 10 falsos positivos.
Conclusiones: La sensibilidad, el valor de predicción positivo y el valor de predicción negativo, de la citología procesada según ambas técnicas, fueron similares, la especificidad de la citología convencional fue más alta.
Palabras clave: Citología convencional. Citología en base líquida. Parámetros de eficacia.
SUMMARY
Objective: To compare the efficacy of cytology with the use of liquid medium in relation to the conventional, in patients who attended the gynecology service in Maternidad Concepción Palacios.
Methods: Carried out a comparative and prospective study that included 177 patients which underwent both PAP (conventional and liquid).
Results: 114 samples with metaplastic cells and from the union escamo-cylindrical were obtained with conventional cytology and 60 with liquid-based cytology (P = 0.001). With liquid-based cytology found fewer cases without inflammatory exudate, most with moderate exudate, and more cases of infection were diagnosed by human papillomavirus. With the conventional technique, there were more cases of bacterial vaginosis. The cytologic findings, in relation to the epithelial cells, were similar with both techniques: 171 and 157 negatives, 2 and 8 atypia of squamous cells of uncertain significance and 4 and 12 intraepithelial lesions of low grade, for conventional smear and liquid-based, respectively. There were 23 false negative and false positive 1 with conventional cytology while with liquid-based cytology had 18 false negative and false positive 10.
Conclusions: The sensitivity, the positive predictive value and the negative predictive value of Cytology processed according to both techniques were similar, the specificity of conventional cytology was higher.
Key words: Conventional cytology. Cytology liquid based. Parameters of efficiency.
INTRODUCCIÓN
La introducción del frotis de células recolectadas del cuello uterino para la detección del cáncer de cuello uterino se debe a Georges Nicolás Papanicolaou en 1940, desde entonces este método se ha usado hasta la actualidad, lo cual ha disminuido, en conjunto con otros métodos como la colposcopia y la biopsia dirigida por colposcopia, la incidencia de cáncer cervical en más de 50 % en los últimos 30 años, con una disminución similar de la mortalidad por la enfermedad. Sin embargo, la citología convencional presenta algunas desventajas que han motivado la búsqueda de nuevas técnicas que permitan mejorar el despistaje, con una mayor sensibilidad y especificidad, para aumentar la frecuencia de diagnósticos realizados en etapa preinvasiva, cuyo tratamiento adecuado constituye una de las herramientas más importante en la prevención del cáncer invasor, sobre todo en países como Venezuela, en el que no ha sido aprobada la administración de la vacuna contra el virus de papiloma humano. Dentro de estas técnicas de despistaje se encuentra la citología en base líquida, como un método que puede llevarse a cabo en forma automatizada, con la utilización de procesadores aprobados por la Food and Drug Administration (FDA), o en forma no automatizada, con la utilización de una citocentrífuga, que permite reducir los costos inherentes al procesamiento automatizado. En el presente estudio se hace una aproximación al valor de la técnica no automatizada de citología en base líquida, que en algunos países llaman procesamiento manual, para observar el impacto en la práctica diaria como gineco-obstetras.
La idea de realizar la presente investigación es establecer si el método de citología en base líquida realizado de acuerdo a un procesamiento no automatizado tiene mayor sensibilidad diagnóstica en relación con la citología convencional, mostrando con ello disminución del porcentaje de falsos negativos.
Lo significativo de la investigación es que hay escasa literatura disponible que hable de sensibilidad del método en base líquida no automatizado, la mayoría de los estudios utilizan un procesamiento automatizado a través de procesadores. La importancia de la utilización de un método citológico novedoso que sea eficaz es vital, sobre todo si supera la sensibilidad del método convencional de manera significativa, lo que llevaría a mejorar el porcentaje de diagnósticos en pacientes enfermas. Otro de los aspectos de importancia en la investigación es que las muestras tomadas con citología en base líquida son preservadas y pueden ser utilizadas posteriormente para determinación de serotipo de ácido desoxirribonucleico (ADN) de virus de papiloma humano (VPH).
La FDA aprobó dos pruebas de citología basadas en líquidos. Ambas permiten depositar el material en un preservativo líquido (Liquid-PREP) con el que se enjuaga el dispositivo de recolección y se fijan las células. Los sistemas de estudio por frotis basados en líquidos son Thin Prep Pap Test® (TPPT, Cytyc Corporation, Boxborough, MA), aprobado en 1996 y el AutoCyte Prep® (TriPap Imaging, Burlington, NC) aprobado en 1999 (1).
Para la realización de la citología líquida se requiere el Liquid-PREP el cual es el medio líquido de preservación donde se disolverá la muestra que se obtiene mediante un cepillo cervical (Cervex Brush ®) que puede remover células del exo y endocérvix simultáneamente, permite la rápida transferencia del material a una lámina en monocapa y disminuye el tiempo de examen (1,2). Sin embargo, este equipo es ligeramente más costoso, tiene algunas hebras plásticas pequeñas flexibles de varias longitudes, las mayores alcanzan el interior del canal cervical para tomar las muestra de células endocervicales, mientras que las más cortas recogen simultáneamente células del exocérvix; es decir, es un procedimiento de un solo paso que tiene la ventaja de la simplicidad y seguridad porque reduce el potencial del secamiento con el aire (1,3,4). El Cervex Brush® puede utilizarse también para la toma de la citología convencional procesada según la prueba de Papanicolaou.
Lee y col. (5) en 1997 ponen de manifiesto que comparando la técnica de Papanicolaou convencional con citología líquida (citología en monocapa) se encuentra una proporción de falsos negativos de 5,6 % y 2,2 % respectivamente. Otro estudio (6) realizado en 2005, concluyó que la citología en base líquida es un método asociado con pocas muestras insatisfactorias, y con significativamente más alta sensibilidad, cuando se compara con la técnica de citología convencional. Por otro lado, Pan y col. (7) siguiendo la metodología Thin Prep y la colposcopia seguida de biopsia cuando estaba indicado, estudiaron a 1997 mujeres en un área de alta incidencia de cáncer cervical en China. Todos los carcinomas de células escamosas y 87 % de las lesiones intraepiteliales de alto grado (LIE AG) en la histología fueron detectados por la citología en base líquida.
Abufala y col. (8) han obtenido una sensibilidad de 76 % con Thin Prep y 68 % con citología convencional y especificidad de 86 % y 79 % respectivamente. Sin embargo, Chatco y col. (9) no encontraron que el sistema en base líquida sea más efectivo que los extendidos convencionales para detectar carcinomas invasivos o lesiones intraepiteliales. Berstein y col. (10) en el 2001 publicaron un metaanálisis que recoge 25 trabajos publicados en la literatura inglesa entre los años 1999 y 2000. Entre sus conclusiones destacan que es mejor la calidad de la muestra de Thin Prep® en todos los estudios, sin embargo, no modifica significativamente el número de diagnósticos de células escamosas anormales como se evidencia por el estudio del intervalo de confianza pero tiene mayor sensibilidad para el diagnóstico de lesiones intraepiteliales de bajo grado (LIE BG) y LIE AG.
Los resultados indican un aumento de 59,7 % de detección de LIE AG o mayor con citología líquida; el cual no se puede atribuir a una elevación de falsos positivos puesto que los criterios citológicos que se emplean para el diagnóstico son similares a los de la citología convencional. Se encuentran tres posibles explicaciones para este aumento de la sensibilidad: 1) Incremento en la recogida del número de células representativas por mejora del muestreo, 2) Reducción de sangre y artefactos y 3) Mejor conservación de las células, lo que permite una mejor categorización de las lesiones. Es posible que el incremento de la sensibilidad se deba a la combinación de estos tres factores; lo cual intenta corregir las limitaciones de la citología tradicional (8). La comparación de las láminas de citología cervical según el método de procesamiento de la muestra permite evidenciar diferencias importantes, entre otras, la citología en base líquida proporciona mayor uniformidad en el espaciamiento de las células, una muestra homogénea, libre de sangre y moco y áreas concentradas para una rápida evaluación de la lámina (8).
Un metaanálisis (11) de ocho estudios en los que todas las pruebas estaban sometidas a la verificación con colposcopia y la prueba estándar que es la biopsia, cuando estaba indicada, señala que no hubo diferencias significativas entre sensibilidad y especificidad entre los dos métodos para lesiones tipo neoplasia intraepitelial 2 (NIC 2) histológicamente confirmadas o de grado mayor.
Uno de los aspectos importantes a considerar con respecto a la citología en base líquida es que se pueden utilizar los medios líquidos aprobados por la FDA con un procesamiento automatizado, mediante el uso de una máquina capaz de procesar una muestra cada vez, en citología líquida, tanto de citología exfoliativa ginecológica, como la no ginecológica, y también preparar muestras obtenidas mediante punción aspiración con aguja fina (PAAF). El procesador Thin Prep 3000® tiene el mismo sistema de trabajo pero es capaz de procesar 80 muestras a la vez (12).
El proceso automatizado de trabajo consta de tres fases:
Dispersión: homogeniza y randomiza el material dentro del vial, dispersando las células.
Selección del material: las células se adhieren en monocapa a un filtro. Los poros del filtro hacen una buena selección de las células, no deja pasar la sangre, el moco ni la mayor parte de leucocitos polimorfonucleares neutrófilos, deja el fondo de la preparación muy limpia.
Transferencia celular: el filtro se invierte y transporta las células que ha captado, del vial al portaobjeto colocado en la parte superior de la máquina.
Este proceso se puede repetir con el mismo vial y obtener varios portaobjetos, dependiendo del número y de la celularidad que hubiera en la muestra recibida, con la misma calidad citológica (13).
La evaluación de la citología en base líquida también puede realizarse en forma no automatizada, siguiendo manualmente cada uno de los pasos del procesador según el siguiente orden: 1.- Tomar la muestra del vial de preservación. 2.- Agregar en un tubo de ensayo, al que se le añadirá el líquido celular de limpieza de la muestra 3.- Centrifugar la muestra durante 10 minutos. 4.- Mediante micro pipeta obtener una gota del Pellet que se colocará en la lámina portaobjeto. 5.- Tinción de la lámina con hematoxilinaeosina. 6.- Secado a temperatura ambiente durante 24 horas. 7.- Visualización al microscopio tomando 10 campos de mayor aumento (40X) (13).
Un análisis de coste efectividad logra demostrar que la técnica de citología en base líquida mejora la sensibilidad, por tanto puede reducir la incidencia y mortalidad de cáncer de cérvix y disminuir los costos asociados a tratamientos de enfermedades avanzadas; así como reducir los costos indirectos mediante la aplicación de técnicas complementarias, como las destinadas al estudio del ADN del VPH. El coste efectividad debe ser valorado de manera global sumando los costos directos e indirectos y calculando los ahorros directos e indirectos que se derivan a corto y a largo plazo con la citología en base líquida (2, 13).
Una de las primeras causas de muerte por cáncer en la mujer venezolana lo representa el cáncer de cuello uterino, para el año 2012, produjo 1 321 muertes y ocupó la segunda causa de muerte por cáncer en la mujer, después del cáncer de mama (14).
Estas cifras elevadas, se deben en gran parte al diagnóstico frecuentemente tardío, determinado por una baja cobertura de los programas de detección y una escasa receptividad de la población de mayor riesgo.
El carcinoma de cuello uterino era la principal causa de muerte por neoplasia maligna en las mujeres de diversos lugares del mundo hasta 1940. Se ha demostrado a través del estudio de la patología que la mayoría de estos tumores tienen una historia natural de la enfermedad con un comienzo gradual, manifestado por la presencia de precursores preinvasores que pueden existir en el epitelio como etapas reversibles o como enfermedad in situ por varios años. Estas etapas tempranas suelen ser asintomáticas, y pueden ser detectadas por métodos comúnmente disponibles, como la citología y se corrobora mediante biopsia dirigida por colposcopia. El cáncer de cuello uterino es una enfermedad que tiene un tratamiento aceptable en la etapa pre-sintomática si se detecta con oportunidad, afectándose su curso y pronóstico (2,15,16).
La primera y más temprana alteración es la aparición de células atípicas en las capas basales del epitelio escamoso. Las células atípicas presentan alteraciones de la relación núcleo/ citoplasma, pérdida de la polaridad, aumento del número de mitosis y pleomorfismo, es decir, todas las características de las células malignas (17).
En 1967, Richard (18) propuso para las lesiones premalignas del cérvix el nombre de neoplasia cervical intraepitelial (NIC) definida como un espectro de epitelios escamosos en uno de cuyos extremos se hayan lesiones con perturbaciones en la estructura y en la maduración, pero bien diferenciadas (corresponderían con displasias leves) y en el otro extremo se hallan epitelios totalmente indiferenciados extendidos en la superficie y/o en las glándulas, sin invasión (correspondería con el carcinoma in situ).
Con respecto a la terminología neoplasia intraepitelial cervical y el sistema citológico de graduación de Papanicolaou, se ha propuesto abandonar estos términos y en su lugar emplear lesión escamosa intraepitelial (LIE) (18), y el Sistema Bethesda para la categorización de los hallazgos encontrados en los extendidos citológicos (19).
En la génesis del carcinoma de cuello uterino se encuentra la infección por VPH; la evidencia epidemiológica de los últimos años identifica al VPH como agente etiológico necesario del cáncer cervical. El ADN de VPH está presente en casi todos los casos (93 %) de cáncer cervical y lesiones precursoras. Si bien se considera que el VPH es un componente de la transformación neoplásica, es improbable que sea su única causa (1).
El carcinoma cervical de tipo escamoso, es la neoplasia cervical más frecuente; representa alrededor del 60 % a 70 % de todo el cáncer de cérvix; las lesiones se localizan en un 90 % a 98 % de los casos en la zona de transformación. El adenocarcinoma se origina a partir de las células cilíndricas o de las células de reservas y habitualmente tienen una localización endocervical. La historia natural del adenocarcinoma cervical se conoce menos que la evolución de la variedad escamosa, probablemente porque es poco frecuente y no es accesible a la visión directa. Se supone que se origina a partir del adenocarcinoma in situ y que puede localizarse en cualquier punto del canal cervical. En su génesis, como en la variedad escamosa, la infección por VPH interviene de forma importante. La iniciación del adenocarcinoma endocervical se ha triplicado en las últimas dos décadas. En consecuencia, se ha dirigido cada vez más atención a la morfología celular del endocérvix. El adenocarcinoma endocervical in situ y la displasia endocervical se están describiendo con más frecuencia, algunas veces asociados con lesión intraepitelial escamosa de alto grado (LIEAG) (1).
Los programas de citología cervical de pesquisa bien organizados han mostrado su efectividad especialmente en países desarrollados dado que actualmente existen suficientes datos que demuestren sus efectos protectores; pueden reducir la incidencia y la mortalidad hasta en 90 %; secundario al éxito del diagnóstico preclínico y del diagnóstico de lesiones cervicales pre-malignas, lo cual es posible por la accesibilidad del cuello uterino a la visualización directa así como al estudio celular y tisular y está relacionado directamente con la proporción de la población a la que se le ha practicado la detección (2,20).
El frotis de Papanicolaou es la prueba de despistaje de cáncer más ampliamente practicada. La frecuencia cada vez menor de muerte relacionada con el cáncer cervical en muchos países desarrollados ha sido atribuida al éxito de este despistaje (21). La citología de Papanicolaou es un método de gran valor para la detección temprana del cáncer cervicouterino, gracias a su alto grado de especificidad, aunado a su sencillez y bajo coste (13). El uso de la colposcopia con biopsia dirigida confirma histológicamente la presencia de la lesión.
La citología exo – endocervical tiene un porcentaje de falsos negativos que varía ampliamente en las diferentes investigaciones entre 0 % y 70 %; y las publicaciones indican que en laboratorios acreditados la proporción de falsos negativos es de 5 % al 10 %, pero que hay un 5 % de falsos negativos que parece imposible de reducir con la citología convencional. Cuando se hace el análisis retrospectivo en pacientes que desarrollan un cáncer de cuello uterino a pesar de haber estado sometidas a evaluación citológica, se observa que 5 % a 15 % tenían un diagnóstico falso negativo y que estos casos correspondían a lesiones epiteliales escamosas de significado indeterminado (ASCUS), lesiones epiteliales escamosas de bajo grado (LIEBG) y lesiones epiteliales escamosas de alto grado (LIEAG) (2,22).
Se ha invertido un esfuerzo considerable para desarrollar instrumentos para extraer células exfoliadas de cuello uterino desde el descubrimiento de que estas contienen rasgos citológicos que indican la presencia de lesiones premalignas o malignas, simultáneamente con la evaluación de las dificultades en el diagnóstico de cáncer cervicouterino, debidas a la toma de una buena muestra del canal endocervical y a las altas tasas de falsos negativos reportadas por la prueba de Papanicolaou; siendo esta última su más grave restricción (2,3).
Las características ideales del instrumento para la toma de muestras incluyen que debe ser capaz de remover células del endocérvix, exocérvix y unión escamocolumnar, las cuales tienen el mayor riesgo de transformación maligna, a su vez debe causar mínima incomodidad, producir poco trauma y ser económico en tiempo de examen y coste de adquisición (3). Se han desarrollado varias técnicas para la recolección de las células del canal endocervical, entre las que se destaca el uso de hisopo de algodón humedecido, el cepillo citológico y técnicas de aspiración endocervical (23).
Dentro de los resultados obtenidos al evaluar los diferentes dispositivos se ha demostrado ausencia de células endocervicales en 11,12 % usando el Citocep ®, en 9,74 % con el uso de Cytobrush® y cifras preocupantes como de 63,8 % con el uso del hisopo de algodón (24).
Lo adecuado de un frotis cervical ha sido un tema de discusión importante, se debe tomar en cuenta la presencia o ausencia de células endocervicales, debido a que este es un punto final común y fácilmente medible. La alta tasa de falsos negativos de la prueba de Papanicolaou es atribuible a los frotis inadecuados caracterizados por estar contaminados con sangre o células inflamatorias, estar extendidos en una capa muy gruesa o errores en la interpretación de la muestra, estar mal fijados y algunos tener insuficiente e incluso ausencia de células endocervicales. Esto trae como consecuencia una disminución de la sensibilidad de la prueba hasta 51 % y un 98 % de especificidad para detectar una neoplasia intraepitelial o un cáncer cervicouterino invasor; según indica un reciente metaanálisis que incluyó únicamente estudios no afectados por sesgos (2,16,25).
La confiabilidad de la citología cervical para detectar enfermedad premaligna y maligna depende de la toma apropiada de la muestra de la zona de transformación debido a que muchas anormalidades epiteliales se generan en o cerca de la unión escamocolumnar. Además, la tasa de detección de anormalidades epiteliales es menor en los frotis que carecen de células endocervicales. Se ha reportado un número estadísticamente significativo de frotis de Papanicolaou negativos en mujeres con cáncer cervical invasivo que carecían de células endocervicales (2,13). La obtención de células endocervicales en los frotis de Papanicolaou se ve influenciada por varios factores: uno lo representa las hormonas sobre el epitelio cervical (las mujeres embarazadas y menopáusicas a menudo producen frotis que carecen de células endocervicales); la ingestión de anticonceptivos orales (ACO) pueden influir adversamente en la obtención de células endocervicales, otro factor es la experiencia de quien toma la muestra, pues los entrenados obtienen mayor tasa de células endocervicales; y el instrumento usado para obtener la muestra también puede influir en la obtención (1,2). Uno de requisitos para reducir al mínimo la incidencia de falsos negativos es que el frotis se realice de preferencia en la fase estrogénica, este aspecto, sin embargo, no ha limitado el hecho de que las muestras se tomen en cualquier momento del ciclo de las pacientes (26).
En 1988, un grupo de expertos reunidos en Bethesda, Estados Unidos, acordaron que la ausencia de células endocervicales en pacientes premenopáusicas debe ser considerada insuficiente para el diagnóstico (2). El hecho de que la presencia de las células endocervicales refleja lo adecuado del frotis es anatómicamente factible, debido a que sugiere que se ha tomado una muestra de la zona de transformación, a partir de la cual surge el cambio premaligno. La presencia de células endocervicales garantiza la representatividad total del componente celular cervical indispensable para emitir un juicio diagnóstico de calidad satisfactoria, de acuerdo a la clasificación de Bethesda de 1991 (2,16,25). Posteriormente, la introducción del sistema 2001 de Bethesda para divulgar resultados de la citología cervical, realizó cambios sustanciales en terminología y en la clasificación de la suficiencia del especimen. El fondo y la discusión del sistema 2001 de Bethesda tiene 2 categorías de la suficiencia: satisfactorio para la evaluación e insatisfactorio para evaluación. El término satisfactorio pero limitado por... de la clasificación anterior fue eliminado. La presencia o la ausencia del componente de endocervical y zona de transformación y cualquier otro indicador de la calidad se proporcionan inmediatamente después del término satisfactorio para la evaluación, por lo que un frotis no se considerará inadecuado o insatisfactorio solo por la ausencia de estas. El informe insatisfactorio incluye las razones de la designación insatisfactoria. Cualquier especimen con células anormales es por definición satisfactorio para la evaluación (27).
El objetivo del presente estudio fue comparar la eficacia de la citología en base líquida con la convencional, en pacientes que acudieron al Servicio de Ginecología de la Maternidad Concepción Palacios.
MÉTODOS
Se llevó a cabo un estudio experimental prospectivo y comparativo, que incluyó 177 pacientes, que hubiesen iniciado actividad sexual, independientemente de la edad. Se excluyeron las que presentaron sangrado genital para el momento del examen, las que estaban embarazadas o usaban terapia hormonal, mujeres con antecedentes de histerectomía o cirugía previa sobre el cérvix y aquellas cuyas muestras resultaran insatisfactorias por alguna de las dos técnicas.
Todas las pacientes recibieron información detallada sobre el estudio y sus alcances, y se incluyeron solo aquellas que expresaron su deseo de participar mediante la firma del consentimiento informado. La toma de la citología se realizó con la paciente colocada en posición de litotomía. No se realizó tacto vaginal previo ni se utilizaron lubricantes sobre la superficie del espéculo; previa visualización del cérvix, se utilizó un cepillo cervical (Cervex Brush®) para la toma endo/exocervical simultáneamente; se realizó un giro de 360 grados para obtener una buena muestra. Posteriormente, se realizó el extendido en una lámina portaobjeto de vidrio rotando el instrumento a lo largo de la superficie de la lámina y se fijó con atomizador a base de alcohol. En un segundo tiempo, con el empleo del mismo cepillo cervical se realizó otra toma con la misma técnica; luego la cabeza del cepillo fue removida y se colocó dentro del vial de preservación que contiene el medio líquido.
Las muestras para citologías convencionales fueron evaluadas en el Servicio de Anatomía Patológica de la Maternidad Concepción Palacios. Las citologías en base líquida fueron revisadas en un laboratorio privado. Ambos patólogos evaluaron las muestras tomando 10 campos de mayor aumento; registraron el número de células endocervicales y sus características citológicas y reportaron los resultados según la clasificación de Bethesda 2001.
Se reportó la presencia o ausencia de células endocervicales, que se clasificaron como normales cuando se encontraron entre 2 y 5 mórulas en campo de 2,5 X, abundantes cuando se encuentraron más de 5 mórulas en un campo de 2,5 X y escasas en el caso de menos de 2 mórulas en un campo de 2,5 X.
La calidad de la muestra se clasificó como satisfactoria cuando la muestra era factible de interpretarse técnicamente (material suficiente, no contaminado) o cuando había presencia de células endocervicales (un mínimo de 2 mórulas) indicando una unión escamo-columnar adecuadamente muestreada; no obstante un frotis no se consideró inadecuado solo por la ausencia de estas, colocándose la respectiva nota en el reporte para consideración del clínico. Fueron consideradas insatisfactorias cuando más del 75 % de las células epiteliales estaban oscurecidas (no se pueden evaluar microscópicamente), el portaobjetos estaba roto o no identificado, se observaba desecación y/o mala fijación.
A todas las pacientes se les realizó colposcopia exo y endocervical y se llevó a cabo toma de muestra para biopsia dirigida en caso de algún hallazgo positivo. Una vez recibidos los diagnósticos definitivos estos fueron registrados para efectos de la investigación y las pacientes fueron derivadas a la consulta para su tratamiento adecuado según el caso.
Todos los datos fueron descritos mediante frecuencias absolutas, relativas o porcentajes, para la comparación se utilizó el paquete estadístico EPIDAT 3.1 y Chi cuadrado, para una P: < 0,05; se usó el test de Fisher para evaluar sensibilidad, especificidad, valor de predicción positivo y valor predicción negativo.
RESULTADOS
Se evaluó un total de 185 pacientes. En 8 casos la citología en base líquida resultó no satisfactoria. Este dato se consideró para el análisis de la calidad de los especímenes, pero luego las pacientes fueron excluidas, quedando como total de pacientes incluidas para el estudio 177.
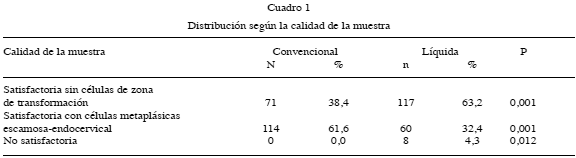
En el Cuadro 1 se muestran los resultados relacionados con la calidad de la muestra. La muestra obtenida con citología convencional fue satisfactoria con células de metaplasia escamosa y/o endocervicales en 114 casos y satisfactoria sin estas células en 71 casos; ningún caso fue reportado como muestra no satisfactoria. Con respecto a la citología en base líquida fue considerada como muestra satisfactoria con células de metaplasia escamosa y/o endocervicales en 60 casos, satisfactoria sin células de metaplasia escamosa y/o endocervicales en 117 y en 8 casos se consideró a la muestra de la citología base líquida como no satisfactoria. Las diferencias entre cada parámetro considerado con respecto a la calidad de la muestra fueron estadísticamente significativas.
En el Cuadro 2 aparece la distribución comparativa de los casos según la presencia de exudado inflamatorio. En 46 casos de citología convencional no hubo exudado mientras que en la citología en base líquida se describió ausencia de exudado en 13 casos (P = 0,001). Cuando hubo exudado la citología en base líquida detectó un mayor número de casos con exudado moderado (69), respecto a la citología convencional (28), esta diferencia fue estadísticamente significativa.
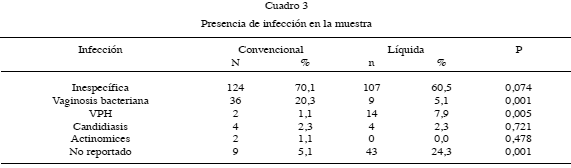
Al evaluar la presencia de infección en la muestra, se observa que la citología convencional diagnosticó 36 casos de vaginosis bacteriana y la citología en base líquida solo 9 (P = 0,001). Por otro lado la citología en base líquida puso en evidencia 14 casos de infección por VPH y la citología convencional solo dos casos (P < 0,005). Las otras infecciones fueron diagnosticadas por igual con ambos métodos (Cuadro 3). Con la citología en base líquida no se reportó infección en 43 casos y con la citología convencional solo 9 (P = 0,001).
Hubo 171 casos negativos como reporte de la citología convencional y 157 casos con la citología en base líquida (P = 0,008). La diferencia en la distribución de los casos positivos (ASCUS y LIE bg) no fue estadísticamente significativa (Cuadro 4).
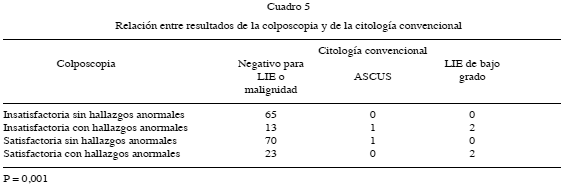
En el Cuadro 5 se observa la distribución de los casos según la relación entre los resultados de la citología convencional y los hallazgos colposcópicos. Hay un predominio de colposcopias sin hallazgos anormales en los casos negativos para LIE (135/171) y de los (6) seis casos con citologías con hallazgos anormales, en (5) cinco se observaron cambios colposcópicos. Esta correlación entre citología convencional y colposcopia fue altamente significativa (P: 0,001).
En el Cuadro 6 se observa que de 157 casos negativos para LIE, 122 tuvieron colposcopias normales pero de 20 casos con citologías alteradas hubo solo seis colposcopias anormales, sin embargo, esta relación también fue estadísticamente significativa (P: 0,003).
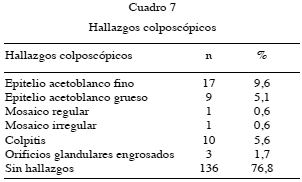
Se puede observar como el mayor porcentaje de pacientes no mostró ningún hallazgo en la colposcopia y de los hallazgos que se presentaron el más frecuente estuvo representado por el epitelio acetoblanco fino (9,6 %) (Cuadro 7).
La correlación citohistológica se representa en el Cuadro 8. Se observan 23 casos de falsos negativos para la citología convencional y 18 para la citología en base líquida. Además, 1 caso de falso positivo para la citología convencional y 10 para la citología en base líquida. Con estos datos se calcularon los índices de eficacia de cada prueba que se presentan en el Cuadro 9 entre los dos métodos. Las diferencias solo fueron estadísticamente significativas en el cálculo de la especificidad (P: 0,0140) que resultó mayor para la citología convencional.
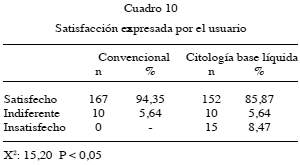
Respecto a la satisfacción del usuario, los resultados se observan en el Cuadro 10. El procedimiento fue considerado satisfactorio en el 85, 87 % de los casos de citología en base líquida y en el 94,35 % de las citologías convencionales. Esta diferencia fue estadísticamente significativa.
DISCUSIÓN
La citología en base líquida es un método que permite la evaluación de una muestra de cérvix que se toma mediante un cepillo cervical (Cervex Brush®) que puede remover células del exo y endocérvix simultáneamente y posteriormente disolverla en un medio líquido de preservación para luego realizar la transferencia del material a una lámina en monocapa. Este proceso disminuye el tiempo de examen (1,2).
En esta serie según la descripción de los patólogos, la muestra obtenida por la técnica convencional es de mejor calidad que la procesada en base líquida, con una mayor proporción de casos en los que se obtuvo células de la zona de transformación y ausencia de casos reportados como muestra no satisfactoria; dato que resulta ser estadísticamente significativo cuando se comparan ambos métodos. Stark (28) hace una comparación entre la calidad de la muestra usando citología convencional y citología en base líquida; en ese estudio la proporción de especímenes que fueron categorizados como insatisfactorios fue de 0,55 % con el uso de la citología convencional y 0,22 % con el uso de la citología en base líquida, dichos autores concluyen que con la implementación de la citología en base líquida hubo una declinación importante en la proporción de especímenes insatisfactorios (P < 0,001). Otros estudios como los de Weynand y col. (29) y Bergeron y col. (30), con la utilización de procesamiento no automatizado describen superioridad de la calidad de la muestra de citología en base líquida, cuando la comparan con la citología convencional, y cuando se compara la calidad de la muestra en dos sistemas no automatizados describen 0,7 % (29) y 0,14 % (30) de muestras inadecuadas. Alves y col. (31) en 2004, realizaron un estudio comparativo utilizando diferentes metodologías como lo fue el uso de Thinprep® y el Autocyt PREP® (procesamientos automatizados) y un procesamiento no automatizado (manual) llamado Mono PREP®. Concluyen que las tres metodologías, preservaron adecuadamente la estructura celular para la evaluación morfológica. Los hallazgos reportados por Stark (28), Weynand y col. (29) y Bergeron y col. (30) no se correlacionan con el presente estudio, en el que se obtuvo 4,3 % de muestras insatisfactorias. La posible explicación para este hecho pudiera estar determinada por el orden en la toma de las muestras, puesto que la primera muestra obtenida fue la destinada al extendido directo o citología convencional y posteriormente, utilizando el mismo cepillo citológico, se procedió a tomar la muestra para su disolución en medio líquido quedando probablemente menor cantidad de células a evaluar para la citología en base líquida.
Se obtuvo un pequeño número de casos sin exudado y una mayor cantidad de exudados moderados en los frotis de la citología en base líquida, contrario a lo que se esperaba puesto que con este método se tratan de separar los elementos inflamatorios y detritus para obtener frotis más limpios, tal como lo muestra Stark (28), quien observa que la excesiva inflamación es una de las razones para clasificar los especímenes como insatisfactorios para evaluación. Este autor señala una disminución de la proporción de los especímenes categorizados como insatisfactorios por exceso de inflamación de 11 % a 4,1 % cuando se cambia la técnica a citología en base líquida (P: 0,003). Las diferencias pudieran ser debidas al traumatismo que se produjo en el cérvix luego de un primer raspado para la toma de la muestra convencional, de hecho, se observó que, luego de la segunda toma, el cérvix quedaba más friable y en muchos casos con sangrado, lo que no ocurría con la primera toma de muestra. Otro aspecto que pudiera influir en las diferencias de los resultados entre el presente estudio y el de Stark (28), pudiera estar dado por las diferencias en la manera de procesar las muestras, dado que en la mencionada investigación se utilizó un procesamiento automatizado, con la utilización un procesador denominado Sure Path.
Respecto a los procesos infecciosos, se diagnosticaron más casos de vaginosis bacteriana con la citología convencional (P: 0,001) y de VPH con la citología en base líquida (P: 0,005). Se encontró un mayor número de casos en los que no se reportó infección con la citología en base líquida y esto pudiera interpretarse como falla de diagnóstico, sin embargo, como ya se señaló, con este método se separan los elementos inflamatorios y detritus para obtener frotis más limpios. Esto explica el número más elevado de casos de diagnóstico de vaginosis bacteriana con la citología convencional. En teoría, este procesamiento debe reducir los falsos negativos para cambios sospechosos, que en último caso es el objetivo de la detección citológica. Las diferencias observadas en ambos métodos con el número de casos no reportados de infección, el número de casos de infección por VPH y de vaginosis bacteriana resultaron significativas.
Con respecto a los diagnósticos obtenidos, llamó la atención el mayor número de casos considerados negativos por la citología convencional, este mayor porcentaje de casos negativos podrían ser interpretados como falsos negativos. La citología convencional como método de detección tiene una sensibilidad que varía entre 50 % y 70 % según la mayoría de las series, lo que se relaciona con su elevado número de falsos negativos. La citología en base líquida permitió, en términos absolutos, diagnosticar mayor número de casos con atipias en células escamosas de significado incierto (ASCUS) y LIEBG pero la diferencia no fue estadisticamente significativa.
Con respecto a los parámetros de eficacia evaluados, se puede establecer que, en general no existe superioridad de una prueba con respecto a la otra. Se observa una mejor sensibilidad para la citología en base líquida de 35,71 % aunque esta diferencia no fue estadísticamente significativa (P: 0,2274), sin embargo, la especificidad de la citología convencional si resultó significativamente mayor que la citología en base líquida (P: 0,0140). En un metaanálisis (11) que incluyó ocho estudios en los que todas las pruebas estaban sometidas a la verificación con colposcopia y la prueba estándar que es la biopsia, cuando estaba indicado, los resultados de señalan que no hubo diferencias significativas entre sensibilidad y especificidad entre los dos métodos para lesiones histológicamente confirmadas tipo NIC 2 o de grado mayor.
La citología en base líquida es una prueba frecuentemente preferida por patólogos o citotecnólogos dado que la interpretación se ve facilitada por el extendido uniforme de las células epiteliales en una capa delgada y con una reducción del tiempo promedio de interpretación microscópica de 30 %. Además se pueden realizar investigaciones en el líquido remanente, tales como determinación de VPH de alto riesgo en pacientes con resultados alterados (dudosos), sin embargo, el método es más costoso en términos de inversión de capital y costes.
A pesar de la popularidad de la citología en base líquida hay escasos estudios de alta calidad sobre su exactitud. La técnica ha demostrado aumentar el número de falsos positivos y no da lugar a una mayor detección de neoplasias intraepiteliales o de lesiones de alto grado (11). De acuerdo con esta afirmación, en esta serie se obtuvieron diez casos de falsos positivos para la citología en base líquida, mientras que solo hubo un falso positivo para la citología convencional. Sin embargo, la citología en base líquida permitió una mayor detección de casos positivos (LIEBG y ASCUS), proporcionando 10 diagnósticos de sospecha en 28 casos positivos, mientras que la citología convencional solo proporcionó 5 casos sospechosos de 28.
El medio líquido está siendo utilizado con frecuencia en la práctica de los gineco-obstetras (32), porque permite realizar otras pruebas en la solución residual, incluido ADN de VPH, sobre todo para las determinaciones en caso de ASCUS.
En una revisión hecha por Ronco y col. (32) la realización de la citología en base líquida en las mujeres jóvenes tuvo un impacto negativo porque se duplicó el número de ASCUS y los falsos positivos fueron diez veces más frecuentes en relación con la citología convencional, lo que se correlaciona con el presente estudio. Ronco y col. (32) señalan que la utilización de la determinación de VPH en pacientes con resultados positivos en la citología, hace que estas pacientes sean sometidas a la realización de una colposcopia sin determinar ningún hallazgo importante, por ello concluyen que la presencia de VPH cervical oncogénico en las adolescentes es común y que la presencia de cáncer cervical es muy rara (33). Las directrices de la Sociedad Americana de Patología Cervical (34) frente a este problema, recomiendan que las adolescentes y menores de 21 años con una citología alterada (dudoso), no debería ir a determinación de VPH sino realizarse un seguimiento con citología en 12 meses.
La precisión de la detección de cáncer cervical puede ser mejorada con la adición de la prueba de VPH junto con la citología en mujeres mayores de 30 años. La detección dual fue aprobada por la FDA en el año 2003 y está incluida en las directrices de numerosas organizaciones, incluyendo la Sociedad Americana del Cáncer y el Colegio Americano de Obstetras y Ginecólogos (35,36). La combinación de ambas pruebas de detección aumenta la precisión a más de 99 % y permite la estratificación del riesgo mediante la identificación de las mujeres con VPH de alto riesgo que requieren de un seguimiento activo, incluso en presencia de una citología negativa; además, en pacientes con citología y determinación de VPH negativos no es necesario repetir las pruebas durante tres a cinco años.
Aunque la evidencia acumulada muestra que la sensibilidad de la prueba de citología líquida no es tan elevada como se informó anteriormente, su popularidad no disminuirá debido a su capacidad para permitir la prueba de VPH, gonorrea, e infección por Chlamydia, junto con la opción para la detección automatizada. De hecho, esto se pone claramente de manifiesto cuando se observa que el usuario, es decir, la persona que practica el estudio, se consideró satisfecho con la técnica de la toma de la muestra en el 85,87 %. Los pocos casos de insatisfacción del usuario o de indiferencia estuvieron relacionados con sangrado del cérvix posterior a la primera toma, lo cual no afectó a la toma de la muestra convencional en vista que siempre se realizó en primer lugar. Otros aspectos que se señalaron para limitar la satisfacción fueron la presencia de orificio cervical externo estenótico o de lesiones endocervicales como pólipos que dificultaron la toma de las muestras, aspectos que afectaron por igual al procedimiento, independientemente del tipo de citología que se realizó.
Este es un momento de oportunidad para mejorar la prevención del cáncer cervicouterino con la aplicación de vacunas contra el VPH (prevención primaria) y las mejoras en la detección y tratamiento de lesiones preinvasoras (prevención secundaria). En esta era de las vacunas, los médicos deben continuar el control y seguimiento de las pacientes con el uso adecuado de todas estas pruebas. Se tienen que identificar los métodos más precisos y eficientes para detectar y prevenir el cáncer cervicouterino y mejorar el acceso a la detección en las mujeres que no están siendo atendidas.
De todo lo anterior se puede concluir que la citología en base líquida como prueba de detección de cáncer de cuello uterino y de sus lesiones premalignas, presentó igual sensibilidad, valor de predicción positivo, valor de predicción negativo pero menor especificidad que la citología convencional en este grupo de pacientes. La calidad de la muestra fue superior con la citología convencional. El usuario se expresó satisfecho con el método en el 85,87 % de los casos.
REFERENCIAS
1. Scott J, Gibbs R, Karlan B, Haney A. Tratado de Obstetricia y Ginecologia Danforth. 9ª edición. México: Mc Graw- Hill Interamericana; 2003:980- 998. [ Links ]
2. Parkin DM, Bray F, Devesa SS. Cancer burden in the year 2000. The global picture. Eur J Cancer. 2001;37: 4-66. [ Links ]
3. Malpica C, Somogyi L, Porta M. Citología endocervical entre muestras tomadas con hisopo y cytobrush. Rev Obst Ginecol de Venez. 1992;52:73- 75. [ Links ]
4. Chakrabarti S, Guijon FB, Paraskevas M. Brush vs spatula for cervical smears. Histologic correlation with concurrent biopsies. Acta Cytol. 1994;38:315- 318. [ Links ]
5. Lee KR, Ashfaq R, Birdsong GG, Corkill ME, McIntosh KM, Inhorn SL. Comparison of conventional Papanicolaou smears and a fluid- based, thin-layer system for cervical Cancer Screening. Obstet Gynecol. 1997;90:278-284. [ Links ]
6. Longatto A, Pereira S, Di Loreto C, Utagawa M, Makabe S, Sakamoto M, et al. DCS liquid based system is more effective than convencional smears to diagnosis of cervical lesions: Study in high-risk population with byopsy-based confirmation. Gynecol Oncol. 2005;97:497-500. [ Links ]
7. Pan Q, Belinson JL, Li L, Pretorius RG, Qiao YL, Zhang WH, et al. A thin layer, liquid based pap test for mass screening in an area of China with a high incidence of Cervical Carcinoma. A cross-sectional comparative study. Acta Cytol. 2003;47(1):45-50. [ Links ]
8. Abufala O, Pezzulo JC, Sherer DM. Perfomance of ThinPrep liquid based cervical cytology in comparison with conventionally prepared papanicolau smears: A quantitative survey. Ginecol Oncol. 2003;90:137-144. [ Links ]
9. Chatco MS, Mattie ME, Schwartz PE. Cytohistologic correlation rates between conventional Papanicolaou smears and ThinPrep cervical cytology: A comparison. Cancer Cytopathol. 2003;99:135-140. [ Links ]
10. Bernstein SJ, Sanchez L, Ndubisi B. Liquid based cervical cytologic smear study and conventional papanicolaou smears: A metaanalysis of prospective studies comparing cytologic diagnosis and sample adequacy. Am J Obstet Gynecol. 2001;185:308-317. [ Links ]
11. Arbyn M, Bergeron C, Klinkhamer P, Martin-Hirsch P, Siebers AG, Bulten J. Liquid compared with conventional cervical cytology: A systematic review and meta-analysis. Obstet Gynecol. 2008;111:167- 177. [ Links ]
12. García M. Utilización de la citología liquida - Procesador Thin Prep en el diagnóstico citológico. Sociedad Española de Anatomía Patológica. 2003. Disponible en http://www.conganat.org/seap/congresos/2003/mesacitologialiquida/. Revisado febrero 2008. [ Links ]
13. Celasun B. Presence of endocervical cells and number of slides in cericovaginal smears. Differences in performance between gynecologists. Acta Cytol. 2001;45:730-734. [ Links ]
14. Anuario de Mortalidad 2012. Ministerio del Poder Popular para la Salud. Dirección General de Epidemiología. Dirección de Información y Estadísticas de Salud. Venezuela. Sept 2014. [ Links ]
15. De Palo G. Neoplasias invasoras del aparato genital inferior. En: De Palo G, editor. Colposcopia y patología del tracto genital inferior. Buenos Aires/ Editorial Médica Panamericana; 2007. p.106. [ Links ]
16. De la Fuente P, Garzon A. Cáncer de Cervix. En: Usandizaga JA, De la Fuente P, editores. Tratado de Obstetricia y Ginecología. Madrid: McGraw-Hill Interamericana; 1999. p.335-371. [ Links ]
17. Alonso P, Lazcano EC, Hernández M. Cáncer cervicouterino. Diagnóstico, prevención y control. 2ª edición. Editorial Médica Panamericana; 2005. p.1- 188. [ Links ]
18. Richard RM. A modified terminology for cervical intraepithelial neoplasia. Obstet Ginecol. 1990;75:131-133. [ Links ]
19. Solomon D, Davey D, Kurman R. The 2001 Bethesda system: Terminology for reporting results of cervical cytology. JAMA. 2002;287:2114-2119. [ Links ]
20. Hempling RE. Cáncer cervical. En: Piver MS, editor. Oncología Ginecológica. 2ª edición. Madrid: Marban libros; 1996. p.111-140. [ Links ]
21. Koonings PP, Dickinson K, Schalaeth JB. A randomized clinical trial comparing the citobrush and cotton swap for papanicolaou smears. Obstet Gynecol. 1992;80:241-245. [ Links ]
22. Germain M, Heaton R, Erickson D, Henry M, Nash J, O Connor D. A comparison of the three most common papanicolaou smear collection techniques. Obstet Ginecol. 1994;84:168-173. [ Links ]
23. Rodríguez A, Torres K, González M. Biopsia endocervical: uso de cánulas endometriales conectadas a un sistema de aspiración. Rev Obstet Ginecol Venez. 2013;73(4):234-244. [ Links ]
24. Somogyi L, Garcia L, Mateo MG, Aldana J. El Citocep: un nuevo instrumento para la toma de muestra de citología cervical. Rev Obstet Ginecol Venez. 1994;54:93-95. [ Links ]
25. Di Saia P. Clinical Gynecologic oncology. 5ª edición. Missouri: Mosby Inc; 2002. [ Links ]
26. González-Merlo J, Abad ML, Salguero LL, Biete SA, Bosch SX, López GG. Cáncer de cervix. Documentos de la SEGO. Madrid: Medites; 1997:115-158. [ Links ]
27. Davey D, Marshall Ch, Birdsong G, Buck H, Cox T, Darragh T, et al. Pap test specimen adequacy and quality indicators. Am J Clin Path. 2002;118(5):714- 718. [ Links ]
28. Stark A. Rejected and Unsatisfactory Specimens: A Comparative Study of Liquid-Based (SurePath) Preparations and Conventional Pap Smears for Cervicovaginal Screening. Lab. Med. 2007;38(12):729-733. [ Links ]
29. Weynand B, Berlière M, Haumont E, Massart F, Pourvoyeur A, Bernard P, et al. A new liquid based cytology technique. Acta Cytol 2003;4:149-153. [ Links ]
30. Bergeron C, Fagnani F. Perfomance of a new liquid based cervical screening technique in the clinical setting of a large French laboratory. Acta Cytol 2003;47(5):753-761. [ Links ]
31. Alves VA, Bibbo M, Schmitt FC, Milanezi F, Longatto Filho A. Comparison of manual and automated methods of liquid based cytology. A morphologic study. Acta Cytol. 2004;48:187-193. [ Links ]
32. Ronco G, Cuzick J, Pierotti P, Cariaggi MP, Dalla Palma P, Naldoni C, et al. Accuracy of liquid based versus conventional cytology: Overall results of new technologies for cervical cancer screening randomised controlled trial. BMJ. 2007;335:28. [ Links ]
33. Cancer Institute. SEER Cancer Statistics Review 1973-1999. Disponible en: http://seer.cancer.gov/csr/1973_1999/. Revisado febrero 2008. [ Links ]
34. Wright TC Jr, Massad LS, Dunton CJ, Spitzer M, Wilkinson EJ, Solomon D; 2006 American Society for Colposcopy and Cervical Pathology-sponsored Consensus Conference. 2006 consensus guidelines for the management of women with cervical intraepithelial neoplasia or adenocarcinoma in situ. Am J Obstet Gynecol. 2007;197:340-345. [ Links ]
35. Saslow D, Runowicz CD, Solomon D, Moscicki AB, Smith RA, Eyre HJ, et al. American Cancer Society guidelines for the early detection of cervical neoplasia and cancer. CA Cancer J Clin. 2002;52:342-362. [ Links ]
36. Wright TC Jr, Schiffman M, Solomon D, Cox JT, Garcia F, Goldie S, et al. Interim guidance for the use of human papillomavirus DNA testing as an adjunct to cervical cytology for screening. Obstet Gynecol. 2004;103:304-309. [ Links ]