Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Técnica de la Facultad de Ingeniería Universidad del Zulia
versión impresa ISSN 0254-0770
Rev. Téc. Ing. Univ. Zulia v.32 n.3 Maracaibo dic. 2009
Oxidation of natural graphite in the laboratory and comparison with the synthetic graphite oxide, by means of thermal and spectroscopic techniques
Daniel Pisapia1, Carlos Barrios2, Manuel Martínez2, Katya Reategui 2, Williams Meléndez2, Santiago Marrero2 y Marcos Escobar3
1Fundación La Salle de Ciencias Naturales, Estación de Investigación Hidrobiológica de Guayana, Ciudad Guayana, Venezuela. danielpisapia@yahoo.com
2Centro de Geoquímica, Instituto de Ciencias de la Tierra, Facultad de Ciencias, Universidad Central de Venezuela. Caracas 1040, Venezuela.
3CARBOZULIA, S.A. y Postgrado en Geología Petrolera, Facultad de Ingeniería, Universidad del Zulia. Maracaibo, Venezuela.
Abstract
With the aim of establishing the probable natural formation of graphite oxide (GO) during the weathering and transport of this mineral, a highly crystalline graphite sample isolated from a Sierra Nevada Formation graphitic schist (Precambrian Age) collected at the State of Trujillo, was subject to controlled oxidation in an oven (T~90°C) with a wet oxygen atmosphere through 25, 50 and 75 days of oxidation. This experimental design simuling weathering is equivalent to the natural alteration for the period of 8, 16 and 24 years, approximately. In addition, graphite oxide (GO) was synthesized by treatment with acid KMnO4. All samples and GO were characterized by means of XRD, Raman spectroscopy, thermogravimetric analysis and Fourier Transformed infrared spectroscopy. Oxydized samples exhibit a decrease in the crystallinity index and in the crystal thickness, reduction of the Raman signals corresponding to the ordered structure, displacements in the highest temperature towards lower values in thermogravimetry, and appearance of C – O strenght vibration in infrared spectroscopy. Such results indicate that a modification takes place in the graphite crystallinity, due to the expansion and incorporation of oxygen. The extent of the alteration do not reached the stage of GO formation.
Key words: Graphite, weathering, graphite oxide, Venezuela, cristalinity.
Oxidación del grafito natural en el laboratorio y comparación con el óxido de grafito sintético, por medio de técnicas térmicas y espectroscópicas
Resumen
Con la finalidad de determinar la posible formación natural del óxido de grafito durante la meteorización y transporte de este mineral, una muestra de grafito altamente cristalizado, aislado de un esquisto grafitoso de la Formación Sierra Nevada (Precámbrico), Estado Trujillo, fue sometido a oxidación controlada (T = 90°C) en atmósfera de oxígeno saturado de agua, a tiempos variables (25, 50 y 75 días). Este diseño experimental de meteorización simulada corresponde a la alteración natural durante 8, 16 y 24 años, respectivamente. En adición, se sintetizó óxido de grafito (OG) por tratamiento con KMnO4 en medio ácido. Tanto las muestras y el OG fueron caracterizadas por medio de las técnicas de difracción de rayos X, espectroscopía Raman, análisis termogravimétrico y espectroscopía de infrarrojo con Transformadas de Fourier. Las muestras oxidadas presentaron disminución en el índice de cristalinidad y espesor del cristal, disminución de las señales Raman correspondientes al material ordenado, desplazamientos de la temperatura máxima en termogravimetría hacia valores más bajos, y aparición de señales C – O en el infrarrojo. Estos resultados indican un cambio en la cristalinidad del material, por la expansión e incorporación de oxígeno. La alteración del material grafitoso original no alcanzó la formación de OG.
Palabras clave: Grafito, meteorización, óxido de grafito, Venezuela, cristalinidad.
Recibido el 21 de Octubre de 2008
En forma revisada el 26 de Junio de 2009
Introducción
El grafito es común en distintas situaciones geológicas, generalmente como resultado del metamorfismo de material carbonáceo, asociado a vetas hidrotermales, o asociado a cuerpos ígneos [1]. El estudio del grafito resulta de importancia en el campo de la petrología metamórfica, ya que comúnmente el nivel de ordenamiento de su estructura está relacionado con las condiciones de metamorfismo que lo han producido, siendo utilizado como indicador de la temperatura del evento metamórfico [2-5]. El grafito experimenta ventajas respecto a otros geotermómetros: a) está presente, aún en pequeñas concentraciones, en numerosas rocas metamórficas; b) responde de forma lineal a los incrementos de temperatura, mediante reordenamiento de su estructura; c) es irreversible, lo que implica que el metamorfismo retrógrado no lo afecta.
Sin embargo, no existen estudios dirigidos a establecer el comportamiento geoquímico del grafito en el ambiente exógeno, siendo Venezuela un país tropical donde sus formaciones geológicas son afectadas en gran magnitud por los factores que inciden sobre el proceso de meteorización; por tanto se espera que ocurra algún tipo de cambio en este mineral. Además, es bien conocido que la estructura abierta, laminar, del grafito hace que muchas moléculas puedan penetrar entre las capas. Se conocen algunas sustancias de este tipo, a saber, fluoruro de grafito y óxido de grafito (OG), este último ha sido el más estudiado por su aplicación industrial. El OG se ha obtenido únicamente de forma experimental, tratando muestras naturales de grafito con agentes oxidantes. El óxido de grafito no se obtiene en forma de compuesto de composición definida, reproducible y estequiométrica, dependiendo de la naturaleza de los cristales de grafito y las condiciones de preparación [6-7]. Lo antes citado, plantea la posibilidad de que pudiese formarse el OG en el ambiente exógeno, producto de la interacción con los agentes meteóricos (H2O, O2, CO2, etc.). De allí, que en el presente trabajo se plantea el estudio de la oxidación experimental controlada del grafito simulando las condiciones naturales y su comparación con OG preparado en el laboratorio.
Materiales y Métodos
Se trabajó con una muestra de grafito aislado de un esquisto grafitoso de la Formación Sierra Nevada, colectado en las cabeceras del río Tafayés, al sur del Estado Trujillo. La muestra fue llevada a condiciones de oxidación controlada en una estufa (T = 90°C) con atmósfera de oxígeno, previamente burbujeado sobre una solución de ácido acético para asegurar condiciones de oxidación ácidas (pH < 6). Se tomaron alícuotas de la muestra a 25, 50 y 75 días de alteración. Se puede demostrar fácilmente que las condiciones empleadas equivalen, asumiendo cinética de primer orden para el proceso, a una aceleración de la meteorización natural de 128 veces. Por tanto las condiciones de tiempo empleadas en la experiencia equivalen a una meteorización del grafito durante su exposición a la pedogénesis, y transporte en medios fluviales, por 8, 16 y 24 años, aproximadamente.
El OG se obtuvo por oxidación del grafito con KMnO4 en medio ácido. Posteriormente fueron caracterizadas todas las fracciones obtenidas, así como el grafito original y el OG por medio de las técnicas de difracción de rayos X (DRX), espectroscopía Raman (ER), y análisis termogravimétrico (ATG-ATD), infrarrojo (FT-IR).
Resultados y Discusión
DRX
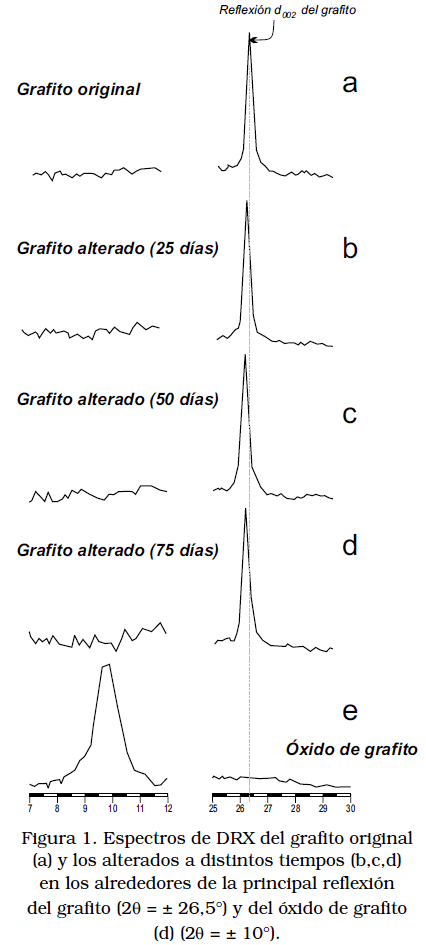
La señal correspondiente a la reflexión d002 (26,5°) mostró pocas variaciones, tanto en el grafito original como en las secuencias oxidadas a 25 y 50 días (Figura 1). A través de esta técnica se logró determinar una leve disminución en el ángulo correspondiente a la reflexión d002 conforme incrementa el tiempo de exposición del grafito a la alteración. La extensión de esta disminución es de apenas 0,2°, lo que corresponde a una variación en el plano de no más de 0,1 Å. Sin embargo, el cálculo de los parámetros cristalinos Ic (Índice de cristalinidad) y Lc (espesor del cristal) en la muestra a medida que aumenta el tiempo de exposición a las condiciones de oxidación controlada señalan cambios menores pero consistentes, a medida que la oxidación progresa (Tabla 1). En efecto, tanto el Ic como el Lc disminuyen en 11 y 6% respectivamente, al pasar del grafito original al oxidado durante 75 días. No se observa cambio alguno en la intensidad de la señal a los 10° (Figura 1), señal que corresponde al OG [7].
Índice de cristalinidad y espesor del cristal
| Muestras | Ic | Lc (A) |
| FMSN | 19,0 | 473,9 |
| FMSN25 (25 días) | 18,0 | 473,7 |
| FMSN50 (50 días) | 17,5 | 473,7 |
| FMSN75 (75 días) | 16,9 | 444,0 |
La serie de grafitos alterados en el laboratorio no alcanzan las características observables en el espectro del OG. Se puede inferir, a partir de los resultados de DRX, que la alteración del grafito mediante oxígeno atmosférico, simulando una oxidación natural acelerada, ocasiona cambios leves en el empaquetamiento cristalino del grafito, pero no se detecta la formación del OG.
Espectroscopía Raman
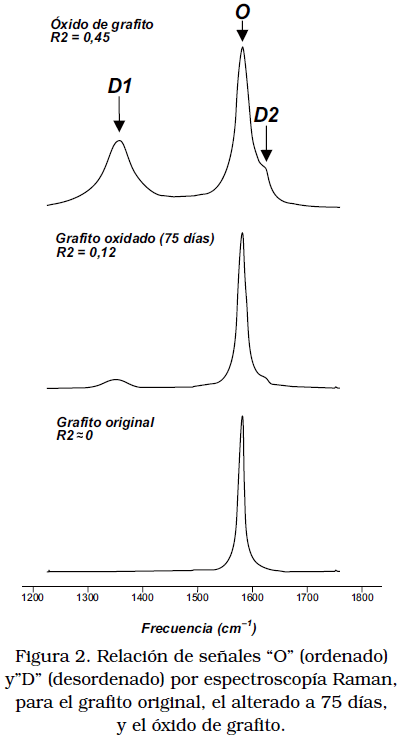
A partir de los espectros de Raman obtenidos (Figura 2), se pudo evidenciar una disminución en la banda de orden “O” (modo de vibración de observado a 1582 cm–1) y un aumento o aparición de las bandas de desorden (modos de vibración D1 y D2 observados a 1355 y 1625 cm–1 respectivamente) a medida que el material fue sometido a un mayor grado de exposición ante los agentes oxidantes, siendo el material menos ordenado el óxido de grafito sintetizado en el laboratorio. Este hecho se ve directamente reflejado en una disminución del parámetro R2 que no es más que la relación entre las áreas de las bandas D1 / O+ D1+D2, y que indica un decrecimiento en el grado de ordenamiento del material [8-10]. La disminución de la cristalinidad se debe posiblemente a la incorporación progresiva de moléculas de oxígeno entre las capas de grafeno que conforman la estructura cristalina del grafito. Se aprecia, al igual que en el caso de DRX, que aún el grafito alterado por más tiempo no alcanza el nivel de desorden propio del óxido de grafito.
Análisis termogravimétrico
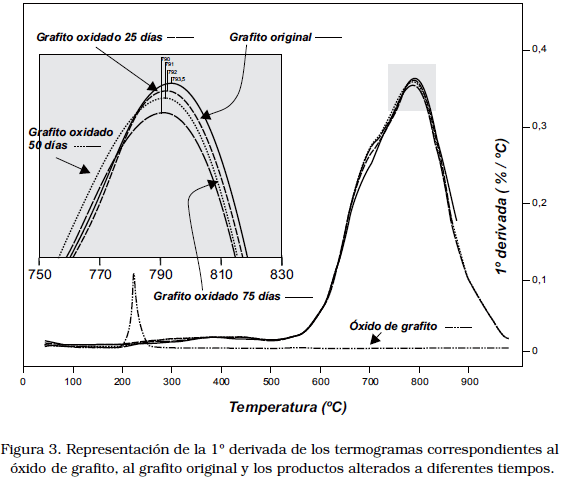
El análisis de los termogramas y en particular de las curvas correspondientes a la 1º derivada del análisis termogravimétrico permite apreciar una leve diferencia en las temperaturas máximas de esta curva, en los distintos productos alterados del grafito, en comparación con la muestra original y con el óxido de grafito (Figura 3). Para el grafito original, el máximo de la curva de la 1ª derivada se alcanza a los 793,5°C, disminuyendo este valor en forma progresiva para las muestras con diferente grado de oxidación hasta llegar a 790°C para la muestra oxidada durante 75 días. Si bien esta diferencia en el valor de temperatura es reducida, proporciona una estimación térmica del grado de alteración que las muestras están sufriendo. Sin embargo, no hay paralelismo con el termograma del óxido de grafito, que a diferencia del material de partida y de los productos alterados, presenta un máximo en los 223,5°C. Estos resultados indican que el grafito está sufriendo modificaciones en su cristalinidad, y la temperatura necesaria para vencer la energía reticular se hace menor a medida que incrementan los tiempos de oxidación, por tanto la energía reticular también es menor. El termograma del OG revela que se trata de un material con muy baja cristalinidad.
FT-IR
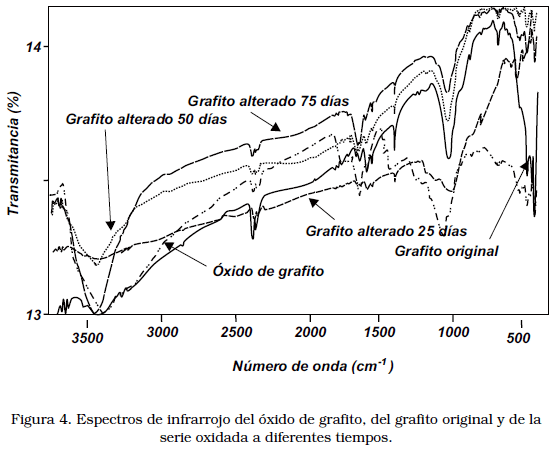
A través de los diferentes espectros de IR, se pudo observar:
- La señal ubicada a 3430 cm–1, experimenta un incremento a medida que incrementa la oxidación. Esta señal bien puede ser asignada a la vibración O–H de moléculas de agua presentes en la estructura entre las capas de grafeno; otra posibilidad es que esta señal pueda estar asociada al estiramiento O–H de grupos fenólicos o alcoholes [11], similar a la observada en dispersiones acuosas coloidales de OG. Esta observación permite una conexión entre el incremento de esta señal y la oxidación incipiente del grafito a medida que avanza la alteración en el laboratorio;
- Los cambios en las restantes señales son poco perceptibles, con excepción tal vez de algunos cambios menores en las señales a 1530 y 1650 cm–1 aproximadamente.
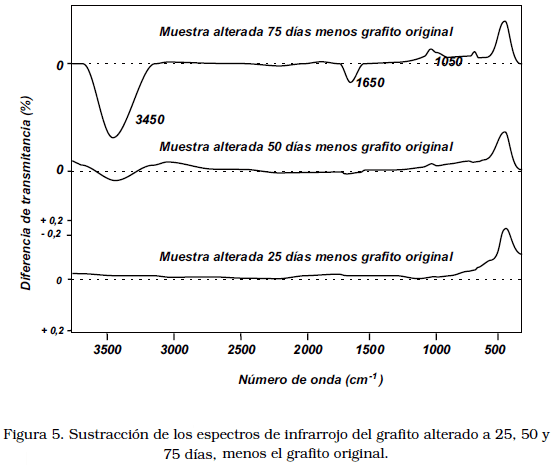
La sustracción de los distintos espectros de infrarrojo de la Figura 4 contra el espectro del grafito original permitió no obstante, visualizar con claridad los cambios que acontecen en el material grafitoso a medida que la alteración por oxidación procede. La Figura 5 ilustra las divergencias entre la muestra alterada a 75 días luego de sustraer las señales propias del grafito original. En la zona media de la figura, se aprecian las variaciones entre la muestra alterada a 50 días menos el grafito original, mientras que en la parte inferior, aparece el resultado de la sustracción de la muestra alterada a sólo 25 días respecto al grafito original. La muestra con sólo 25 días de tratamiento oxidativo no manifiesta prácticamente diferencias respecto a la muestra intacta; los cambios son mínimos aún en la muestra alterada a 50 días, apreciándose diferencias leves en la zona superior a los 3000 cm–1. La muestra expuesta a 75 días de oxidación controlada manifestó la mayor variabilidad, destacando el incremento en la señal alrededor de 3450 cm–1, que como ya se explicó, puede ser atribuida a agua adsorbida al grafito como producto de la aparición de grupos polares, o simplemente se trata de grupos fenólicos. La sustracción también revela la aparición en el material oxidado de una absorción diferencial a 1650 cm–1, asignada a la aparición de grupos carbonilo, ausentes en el grafito original. Esta evidencia espectroscópica permite determinar el grado de alteración que alcanzaron las muestras. Por consiguiente hay una pérdida de aromaticidad de la estructura que puede estar asociada directamente con la incorporación parcial de oxígeno a la estructura de las láminas de grafeno, ya sea como carbonilos o como hidroxilos.
No obstante, no hay similitud con el espectro del óxido de grafito, que presenta como característica diagnóstica la aparición de una señal hacia los 1700 cm–1, propia de grupos carboxílicos [12]. Esta señal está ausente en el grafito original y en las muestras alteradas. Otras señales, como la que aparece aproximadamente en 1070 cm–1 en el óxido, son propias de la presencia de epóxidos. Al igual que en el caso anterior, esta banda está ausente en el grafito original y en el alterado.
Conclusiones
Los resultados en conjunto revelaron que en la estructura del grafito tiene lugar un cambio en la cristalinidad a causa de la oxidación controlada en el laboratorio: el grafito alterado ha perdido en forma parcial su arreglo reticular por la expansión de la estructura del mineral, posiblemente por la incorporación de oxígeno formando enlaces covalentes. Las evidencias espectroscópicas permiten por tanto afirmar que:
- Tiene lugar una disminución de la cristalinidad del grafito con disminución de su energía reticular (Rayos X, Termogravimetría).
- Ocurre un incremento del desorden en el cristal del grafito, conforme es oxidado (Raman).
- Se incorpora oxígeno a la estructura como carbonilos, posiblemente también hidroxilos (infrarrojo).
- La alteración alcanzada no llega a la formación de OG sensu stricto.
Estos hallazgos son de gran relevancia para comprender mejor el destino geoquímico del grafito en los procesos de meteorización de rocas grafitosas. Por otra parte, se destaca la potencialidad de las herramientas térmicas (termogravimetría) y sobre todo las espectroscópicas (DRX, Raman, Infrarrojo) en el estudio planteado. La sustracción digital de los espectros permite revelar los cambios en el material conforme es alterado.
Agradecimiento
Este trabajo fue financiado por FONACIT mediante el proyecto individual S1-98003208.
Referencias Bibliográficas
1. Buseck P. y Bo-Jun H. “Conversion of carbonaceous material to graphite during metamorphism”. Geochimica et Cosmochimica Acta, Vol. 19 (1985), 2003-2016. [ Links ]
2. Martínez M., Vivas M., Marrero S., Melendez W., Garbán G., Benavides A. “Características morfológicas y cristalográficas del grafito de Osumita, Venezuela, y su uso como geotermómetro”. Estudios Geológicos, Vol. 59 (2003), 267-276. [ Links ]
3. Schiffbauer, J., Yin, L., Bodnar, R., Kaufman, A., Meng, F., Hu, J., Shen, B., Yuan, X., Bao, H., Xiao, S. “Ultrastructural and Geochemical Characterization of Archean-Paleoproterozoic Graphite Particles: Implications for Recognizing Traces of Life in Highly Metamorphosed Rocks”. Astrobiology, Vol. 7 (2007), 684-704. [ Links ]
4. Crespo, E., Luque, J., Fernández-Rodríguez, C., Rodas, M., Díaz-Azpiroz, M., Fernández-Caliani, J.C., Barrenechea, J. “Significance of graphite occurrences in the Aracena Metamorphic Belt, Iberian Massif”. Geological Magazine, Vol. 141 (2004), 687-697. [ Links ]
5. Parthasarathy, G., Sreedhar, B., Chetty, T. “Spectroscopic and X-ray diffraction studies on fluid deposited rhombohedral graphite from the Eastern Ghats Mobile Belt, India”. Current Science, Vol. 90, (2006), 995-1000. [ Links ]
6. Hristea G. y Panaitescu C. “Structural aspects about graphite oxides”. Revue Roumaine de Chimie, Vol. 46 (2000), 1107-1111. [ Links ]
7. Titelman, G., Gelman, V., Bron, S., Khalfin, R., Cohen, Y. “Characteristics and microstructure of aqueous colloidal dispersion of graphite oxide”. Carbon, Vol. 43 (2005), 641-649. [ Links ]
8. Wopenka B., Pasteris J. “Structural characterization of kerogens to granulite-facies graphite”. American Mineralogist, Vol. 78 (1993), 533-557. [ Links ]
9. Beyssac O., Goffe B., Chopin C., Rouzaud J. “Raman spectra of carbonaceous materials in metasediments: A new geotermometer”. Journal of Metamorphic Geology, Vol. 20 (2002), 859-871. [ Links ]
10. Beyssac O., Bollinger L., Avouac J. P. y Goffé B. “Thermal metamorphism in the lesser Himalaya of Nepal determined from Raman spectroscopy of carbonaceous material”. Earth and Planetary Science Letters, Vol. 225 (2004), 233-241. [ Links ]
11. Weng, W., Chen, G., Wu, D., Lin, Z., Yan, W. “Preparation and characterizations of nanoparticles from graphite via an electrochemically oxidizing method”. Synthetic Metals, Vol.139 (2003), 221-225. [ Links ]
12. Jeong, H., Noh, H., Kim, J., Jin, M., Park, C. y Lee, Y. “X-ray absorption spectroscopy of graphite oxide”. Europhysics Letters (EPL Journal), Vol. 82 (2008), 67004.1-67004.5. [ Links ]