Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Técnica de la Facultad de Ingeniería Universidad del Zulia
versión impresa ISSN 0254-0770
Rev. Téc. Ing. Univ. Zulia v.32 n.3 Maracaibo dic. 2009
Preparation and characterization of supported Ce/Tb mixed oxide for use in TWC catalysts
María Da Costa, Víctor Ferrer, Jorge Sánchez, Jeanette Zárraga y Dora Finol
Instituto de Superficies y Catálisis, Facultad de Ingeniería, Universidad del Zulia, P.O. Box 15251. Maracaibo 4003A, Venezuela. dfinol@luz.edu.ve
Abstract
The CeTbOX/La2O3-Al2O3, CeO2/La2O3-Al2O3, CeTbOX/SiO2 and CeO2/SiO2 catalysts were prepared by incipient wetness impregnation technique from aqueous solutions of cerium, terbium and lanthanum chlorides. The catalysts were characterized by X-ray fluorescence (XRF), Surface area, Temperature-programmed reduction (TPR), Temperature-programmed desorption of hydrogen (TPD-H2), Oxygen storage capacity (OSC). The catalytic behavior was studied using methane oxidation reaction after different thermal treatments. The TPR study showed that the addition of Tb ion improves the reduction properties of cerium oxide. TPR profiles showed appreciable changes in the nature of the superficial phases in surface after the different thermal treatments, and that the oxides supported on silica reduce in a temperature range lower than those corresponding to the modified alumina-supported catalysts; this effect is advantageous but it does not correlate with the low values of OSC and catalytic activity. The higher OSC and the higher conversions were obtained with CeTbOX/La2O3-Al2O3 catalyst. The methane oxidation reaction is not favored with the increase of the oxygen partial pressure.
Key words: Three-way catalysts, TPR, TPD, methane oxidation.
Preparación y caracterización de un óxido mixto de Ce/Tb soportado para su uso en catalizadores TWC
Resumen
Se prepararon catalizadores de CeTbOX/La2O3-Al2O3, CeO2/La2O3-Al2O3, CeTbOX/SiO2 y CeO2/SiO2, utilizando la técnica de impregnación a humedad incipiente a partir de soluciones acuosas de cloruros de cerio, terbio y lantano. Los catalizadores fueron caracterizados mediante las técnicas de Fluorescencia de rayos X (XRF), Área superficial, Reducción a Temperatura Programada (TPR), Desorción a Temperatura Programada de H2 (TPD-H2), Capacidad de Almacenamiento de Oxígeno (OSC). El comportamiento catalítico de las muestras sometidas a distintos tratamientos térmicos fue evaluado a través de la reacción de oxidación de metano. Los estudios de TPR muestran que la adición del ión Tb mejora la reducibilidad del óxido de cerio. En los perfiles de TPR se observan cambios en la naturaleza de las fases presentes en superficie luego de ser sometidas a distintos tratamientos térmicos y que los óxidos soportados en sílice se reducen en un rango de temperatura menor que los correspondientes a los catalizadores soportados sobre alúmina modificada, efecto que es ventajoso pero que no tiene correlación con los valores obtenidos de OSC y actividad catalítica. La mayor OSC y conversión fueron obtenidas para el catalizador CeTbOX/La2O3-Al2O3. La reacción de oxidación de metano se desfavorece con el incremento de la presión parcial de oxígeno.
Palabras clave: Catalizadores de tres vías, TPR, TPD, oxidación de metano.
Recibido el 9 de Octubre de 2008
En forma revisada el 7 de Septiembre de 2009
Introducción
Las emisiones generadas a través del escape de los automóviles constituyen una de las principales fuentes de contaminación ambiental. En tal sentido, se han realizado numerosas investigaciones en busca de catalizadores que transformen los gases tóxicos generados (CO, Hidrocarburos y NO), en sustancias menos perjudiciales como CO2, H2O, N2 y H2. Esta transformación de los gases tóxicos es llevada a cabo en los catalizadores de tres vías ó TWC (Three Way Catalysts), que son colocados en el tubo de escape bajo el chasis del automóvil [1, 2]. Estos catalizadores están compuestos básicamente por un soporte, típicamente g-Al2O3 de alta superficie, un promotor redox, clásicamente el CeO2 y diversas combinaciones de metales nobles como lo son el Pt, Rh y Pd los cuales constituyen la fase activa de estos catalizadores [3, 4].
Las especificaciones de los TWC de última generación son cada vez más exigentes, lo cual obliga a la búsqueda de promotores redox alternativos con el propósito de obtener un catalizador que mejore los sistemas clásicos basados en CeO2, especialmente en las condiciones denominadas de arranque en frío del automóvil; instante en el cual se produce más del 90% de las emisiones de hidrocarburos a la atmósfera [5].
En los últimos años, la importancia económica y tecnológica alcanzada por los catalizadores tipo TWC, es un hecho evidente [6, 7]. La combustión catalítica de hidrocarburos está creciendo en importancia para el control de emisiones de compuestos orgánicos volátiles, ya que esta puede reducir drásticamente la temperatura requerida para una combustión completa en comparación con los procesos térmicos de combustión sin catalizador [8]. Estudiar la combustión catalítica de metano tiene una particular importancia, ya que es el hidrocarburo más estable, su transformación es clave como punto de referencia para la reacción de oxidación de otros hidrocarburos presentes en los gases de escape [9, 10]. Esto implica que es necesario el desarrollo de nuevos catalizadores alternativos que eliminen estos efectos indeseables por la presencia del CeO2 en estos nuevos sólidos.
La presente investigación se plantea preparar y caracterizar un oxido mixto a base de cerio, para ser utilizado como soporte en catalizadores del tipo TWC. Para tal fin se han preparado varios óxidos: CeTbOx/SiO2, CeO2/SiO2, CeTbOx/ La2O3-Al2O3 y CeO2/La2O3-Al2O3, que serán caracterizados por distintas técnicas y cuyo comportamiento catalítico se evaluará mediante la reacción de oxidación de metano sobre muestras sometidas a distintos tratamientos térmicos. El propósito de evaluar la actividad de muestras sometidas a ciclos sucesivos de oxidación-reducción es evaluar el comportamiento catalítico bajo condiciones similares a las que están sometidos los catalizadores TWC en los automóviles.
Parte Experimental
Preparación de los catalizadores
Los catalizadores CeTbOX/La2O3-Al2O3, CeO2/La2O3-Al2O3, CeTbOX/SiO2 y CeO2/SiO2 fueron preparados por el método de impregnación a humedad incipiente. Los soportes La2O3-Al2O3 y SiO2 previamente se calcinaron a 700°C por 5 h, se impregnaron con una solución acuosa de cloruro de cerio y cloruro de terbio mezclado en proporción molar de Ce/Tb=7/3, equivalente a una carga másica de 16.7% de óxido mixto en 100 gr de muestra. Se realizaron 5 ciclos sucesivos de impregnación/secado, secando a 80°C en aire entre ciclos, y finalmente las muestras se calcinaron en una mufla a 700°C por 4 h.
Área superficial
Se utilizó un equipo Micromeritics ASAP 2010 para determinar el área superficial específica y volumen de poro de las muestras preparadas, siguiendo el método BET. Se usaron 100 mg de muestra previamente secada a 150°C por 3 horas en alto vacío antes del análisis.
Fluorescencia de rayos X
La composición química de todas las muestras fueron determinadas por Fluorescencia de rayos X empleando el espectrómetro SHIMADZU EDX-700HS, trabajando en base seca y a alto vacío.
Desorción térmica programada de hidrógeno (TPD-H2)
Las medidas de TPD-H2 fueron realizadas en una línea de reacción de acero inoxidable acoplada a un TCD. La muestra (100 mg) fue sometida inicialmente a un tratamiento estándar de limpieza (TSL) que consiste en el calentamiento en flujo de 30 mL/min de O2(5.09%)/He por 1 h a 550°C), luego de enfriada en el mismo flujo hasta 150°C, se conmutó a Ar (30 mL/min) y se enfrió hasta temperatura ambiente. Concluido dicho tratamiento, la muestra fue reducida a distintas temperaturas (300-700°C) en flujo de H2(5.225%)/Ar a 30 mL/min por 1 h y posteriormente enfriada en el mismo flujo hasta temperatura ambiente. El flujo de gas se conmutó a Ar (60 mL/min), y se calentó la muestra en el mismo flujo hasta 1000°C a 10°C/min.
Reducción a temperatura programada (TPR)
Se realizó en el mismo equipo empleado para las pruebas de TPD-H2 y con 100 mg de muestra sometida a un TSL. Seguidamente, el flujo se conmutó a H2(5.225%)/Ar (30 mL/min), y se registró el perfil de TPR calentando la muestra desde temperatura ambiente hasta 1000°C a 10°C/min.
Capacidad de almacenamiento de oxígeno (OSC)
La muestra (100 mg) fue sometida a un TSL, luego se calentó en gas inerte a 10°C/min hasta la temperatura de reducción (500°C, 600°C y 700°C) y se mantuvo 30 minutos hasta lograr una completa estabilización. Seguidamente, se introdujo la mezcla reductora a 30 mL/min durante un minuto y se evacuó durante 15 minutos a la temperatura de reducción. Posteriormente se enfrió en flujo de gas inerte hasta 150°C, para introducir cada 30 s pulsos de 25 µL de O2(5.09%)/ He.
Actividad catalítica
100 mg de muestra fueron sometidas al TSL, seguido de un tratamiento de reducción en mezcla de H2(5%)/N2 a 30 mL/min, durante 1 h a las temperaturas de 500 y 700°C previo a la realización de la reacción. Las medidas se llevaron a cabo sobre muestras sometidas al TSL y sobre las muestras reducidas, y en muestras sometidas a ciclos sucesivos de oxidación-reducción. La mezcla de reacción (60 mL/min) está constituida de metano, oxígeno y de nitrógeno como gas de balance. El metano y el oxígeno fueron mezclados en una relación estequiométrica (CH4/O2=0.5) ó en exceso de oxígeno (CH4/O2=0.25), con una velocidad espacial de 14342 h-1. A la salida del reactor se analizó la composición del metano para temperaturas entre 23 y 700°C, mediante un cromatógrafo de gases equipado con una columna empacada de tamiz molecular 5A de 2.5 m, utilizando un FID.
Resultados y Discusión
Área superficial
La Tabla 1 muestra el área superficial BET y el volumen de poro obtenido para las muestras preparadas, observándose una disminución en el área superficial y en el volumen de poro luego de la adición de CeO2, CeTbOX ó La2O3 comparada con los valores reportados para los soportes SiO2 y Al2O3. Este efecto ha sido observado por Damyanova y col. [11], los cuales indicaron que durante la impregnación, los compuestos óxidos se depositan en las cavidades de los poros, causando un decrecimiento en el volumen y en el área superficial específica del SiO2 y Al2O3.
Superficie BET y Volumen de poro para todas las muestras preparadas
| Muestras | Superficie BET (m2/g) | Volumen de poro (cm3/g) |
| SiO2 | 266 | 1.19 |
| CeO2 / SiO2 | 200 | 0.86 |
| CeTbOx / SiO2 | 188 | 0.83 |
| Al2O3 | 136 | 0.47 |
| La2O3 – Al2O3 | 97 | 0.32 |
| CeO2 / La2O3 – Al2O3 | 91 | 0.27 |
| CeTbOx / La2O3 – Al2O3 | 72 | 0.22 |
Fluorescencia de rayos X
Los resultados de composición química aparecen registrados en la Tabla 2. La composición de CeO2 es similar al valor nominal (16.7%) mientras que los valores mostrados para los óxidos mixtos soportados se encuentran alrededor del 18-20 %.
Composición química (% m/m) de las diferentes muestras preparadas
| Muestras | CeO2 | SiO2 | Al2O3 | Tb4O7 | La2O3 |
| CeO2 / SiO2 | 16.5 | 83.4 | - | - | - |
| CeTbOx / SiO2 | 12.8 | 78.8 | - | 8.4 | - |
| CeO2 / La2O3 – Al2O3 | 16.7 | - | 70.9 | - | 12.3 |
| CeTbOx / La2O3 – Al2O3 | 11.9 | - | 65.8 | 6.9 | 15.4 |
Reducción a temperatura programada (TPR)
La Figura 1 contiene los perfiles de TPR registrados para la muestra CeTbOx/La2O3-Al2O3, luego de ser sometida al tratamiento estándar y ciclos sucesivos de oxidación/reducción. Estos tratamientos fueron realizados con la finalidad de detectar posibles cambios en la muestra. En la Figura 1a, la reducción del óxido mixto comienza alrededor de 400°C y se extiende hasta 950°C. El diagrama de TPR presenta dos señales principales: la primera presenta un máximo alrededor de 685°C con un hombro a 543°C y la segunda señal a 925°C. Estas dos señales también aparecen en el diagrama de reducción a temperatura programada registrado para el óxido de cerio soportado sobre alúmina modificada (Figura 1e). En este caso, las dos señales se corresponden con dos etapas de reducción de CeO2; la primera señal corresponde a un proceso de reducción superficial mientras que la segunda ha sido asignada a un proceso de reducción en masa [12]. Se ha reportado la coexistencia de los iones Tb4+ y Tb3+, aún después de someter la muestra a tratamientos de oxidación a 600°C, por lo que no se descarta una pequeña contribución en las señales reportadas en la Figura 1, correspondientes a la reducción de los iones Tb4+ [12-14]. Las diferencias observadas en las señales reportadas para el óxido mixto soportado y el óxido de cerio soportado, estarían indicando que el óxido mixto soportado mejora la reducibilidad del óxido de cerio ya que la desplaza a más baja temperatura [12, 13, 15].
El perfil de TPR obtenido para la muestra de CeTbOx/La2O3-Al2O3 reoxidada a 700°C (Figura 1b), indica la desaparición en gran escala de las especies reducibles como consecuencia de las elevadas temperaturas a las cuales fue sometida durante el primer TPR, sugiriendo la sinterización del soporte y la pérdida irreversible del óxido mixto. Esta sugerencia está soportada en la cantidad de hidrógeno consumido durante la reducción, la cual es menor a la consumida por el óxido mixto fresco (Tabla 3). Finol [12], en estudios realizados sobre óxido mixto soportado de Ce/Tb, mostraron que después de un tratamiento de reducción a 900°C se formaba una fase tipo perovskita (LaAlO3). El perfil de TPR registrado a esta misma muestra luego de reoxidada a 550°C (Figura 1c) presenta cambios en la forma del diagrama debido a la pérdida irreversible del cerio. Aunque el diagrama de TPR obtenido para la muestra fresca de óxido mixto soportado sobre alúmina modificada a 700°C (Figura 1d) es muy semejante al registrado para esa muestra pero oxidada a 550°C (Figura 1a), se observan pequeños cambios en cuanto a los máximos de las señales de reducción y del consumo total de H2 (Tabla 3), lo cual sugiere modificaciones en la superficie producto de la alta temperatura de oxidación empleada.
Consumo total de H2 (mmol H2/g muestra) registrado para las muestras
| Tratamiento | CeO2/La2O3-Al2O3 | CeTbOx/ La2O3-Al2O3 | CeO2/SiO2 | CeTbOx/SiO2 |
| Oxidado 550°C durante 1 h | 1.31 | 0.74 | 1.09 | 1.22 |
| Reoxidado 700°C durante 1 h | 0.43 | 0.29 | 0.79 | 0.78 |
| Reoxidado 550°C durante 1 h | 0.38 | 0.21 | 0.42 | 0.31 |
| Oxidado 700°C durante 1 h | 1.04 | 0.65 | 0.76 | 0.88 |
En la Figura 2 se muestran los perfiles de TPR registrados para CeTbOx/SiO2 (Figura 2c) y CeO2/SiO2 (Figura 2d) y, con la finalidad de establecer comparaciones, se muestran los diagramas de TPR para el CeTbOx/La2O3-Al2O3 (Figura 2a) y CeO2/La2O3-Al2O3 (Figura 2b). Los perfiles de TPR registrados para los dos óxidos soportados sobre sílice son muy semejantes, ambos comienzan alrededor de los 400°C y finalizan a los 925°C. No obstante, las dos señales antes mencionadas bien pueden corresponder a las dos etapas de reducción indicadas para el cerio.
Comparado los perfiles de TPR obtenidos para el óxido mixto soportado sobre alúmina modificada y sílice, es evidente que este óxido se reduce en un menor rango de temperatura cuando está soportado sobre este último. Asimismo, las dos señales principales de reducción aparecen desplazadas alrededor de 130°C, a más baja temperatura. La SiO2 tiene como característica ser de naturaleza más inerte que la Al2O3, evitando la pérdida de cerio ó de óxido mixto por la interacción con el soporte. Este comportamiento, si se quiere ventajoso con respecto al CeTbOx/La2O3-Al2O3, no se corresponde con otras medidas realizadas y discutidas más adelante.
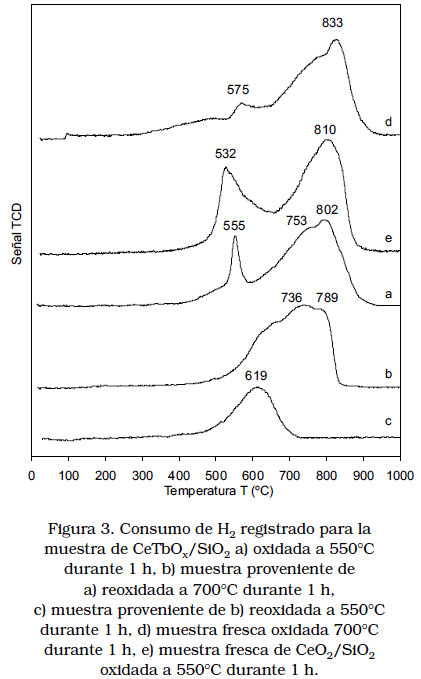
El CeTbOx/SiO2 fue sometido a ciclos sucesivos de oxidación/reducción, registrándose los perfiles de TPR en la Figura 3. La Figura 3a muestra las dos señales correspondientes a la reducción del cerio superficial y en masa respectivamente a 555°C y 802°C [16]. Cuando esta muestra, ya sometida a un primer TPR, es reoxidada a 700°C y es sometida a un segundo TPR (Figura 3b), se observa que la señal de más baja temperatura desaparece y disminuye la cantidad de hidrógeno consumido durante la reducción de 1.22 hasta 0.78 mmol H2/g (Tabla 3).
Esta disminución fue más acentuada en el tercer perfil de TPR (Figura 3c). Por otro lado, si se comparan los perfiles de TPR registrados para el óxido mixto fresco oxidado a 550°C (Figura 3a) y oxidado a 700°C (Figura 3d), se puede observar que la señal de baja temperatura, asignada a la reducción del cerio superficial disminuyó drásticamente con el último de los tratamientos, lo cual se correlaciona con el consumo de H2 registrado para las muestras. Esta observación sugiere que con el tratamiento de oxidación a 700°C, la muestra de CeTbOx/SiO2 sufre cambios importantes en las especies reducibles.
Capacidad de almacenamiento de oxígeno (OSC)
En la Tabla 4 se reportan los valores de OSC obtenidos para el óxido mixto soportado sobre alúmina modificada, y como muestra de referencia CeO2/La2O3-Al2O3. La cantidad de O2 adsorbido es mayor para la muestra de óxido mixto reducida por 1 min, demostrando que la adición de Tb mejora la movilidad del O2 en la red del CeO2, sugiriendo la formación del óxido mixto de CeTb. No obstante, asumiendo que todo el Ce+3 está asociado a una vacancia de oxígeno, entonces la OSC para el óxido mixto soportado reducido a 700°C está sobre estimada (0.72 mmol O2/g muestra) ya que el hidrógeno total consumido durante el TPR fue de 0.74 mmol H2/g muestra. En este caso podría pensarse que además de las vacancias de oxígeno, se esta valorando el hidrógeno transferido al soporte que no fue eliminado durante la evacuación. Es evidente que la introducción del terbio al óxido de cerio mejora considerablemente la OSC. Los valores de OSC para las muestras reducidas a 600 y 700°C durante 1 h se encuentran por debajo de la correspondiente reducida durante 1 min. Posiblemente, dado el tiempo prolongado de exposición en ambiente reductor, pudo haberse formado algún aluminato de cerio que impida la adsorción del oxígeno.
Cantidad de O2 adsorbido (mmol de O2/g) para todas las muestras soportadas sobre La2O3-Al2O3 luego de ser sometidas a distintos tratamientos térmicos
| Temperatura de Reducción (°C) | CeTbOx/La2O3-Al2O3 | CeO2/ La2O3-Al2O3 |
| 500°C durante 1 min | 0.30 | 0.17 |
| 600°C durante 1 min | 0.33 | 0.30 |
| 700°C durante 1 min | 0.72 | 0.36 |
| 600°C durante 1 h | 0.26 | 0.15 |
| 700°C durante 1 h | 0.26 | 0.16 |
Para las muestras de CeTbOX/SiO2 y CeO2/SiO2, los valores de OSC fueron despreciables bajo todos los tratamientos ensayados. Es posible que durante la preparación se haya formado una nueva fase que se reduce en el rango reportado para el CeO2. Sin embargo, esa fase no es accesible al oxígeno, ya que estaría estabilizando el ión Ce+3.
Desorción a temperatura programada de H2 (TPD-H2)
Los análisis realizados a todas las muestras preparadas no mostraron señales de desorción de hidrógeno, luego de ser tratados en flujo de H2(5.225%)/Ar durante 1 h a temperaturas comprendidas entre 200°C y 700°C. Este resultado permite descartar la influencia del soporte en el comportamiento de las mismas. Diferentes autores han indicado que la cantidad de hidrógeno adsorbido es sensible a las condiciones de pretratamiento, en muestras preparadas a partir de los nitratos de cerio y terbio respectivamente [11, 17]. En nuestro caso, los precursores utilizados para la preparación de las muestras fueron cloruros de cerio y terbio. Aunque los resultados de XRF no mostraron la presencia de cloro, el hecho de que los catalizadores no quimisorban hidrógeno podría explicarse por la presencia de cloro remanente que no fue eliminado por calcinación, y cuya cantidad es tal, que la técnica de XRF no lo detecta. Así, la adsorción reversible de hidrógeno a las distintas temperaturas ensayadas es inhibida por el cloro, ya que éste ocupa los sitios para la adsorción del mismo. Kondarides y Verykios [18] indicaron que el cloro inhibe la adsorción de hidrógeno en muestras de CeO2 preparadas por impregnación con soluciones acidificadas con acido clorhídrico.
Actividad catalítica
En la Tabla 5 se muestran los porcentajes de conversión a diferentes temperaturas y tratamientos estudiados, en condiciones estequiométricas. Para todos los tratamientos, la conversión aumenta a medida que se incrementa la temperatura. No se reportó reacción en ausencia de catalizador. Las conversiones registradas para la muestra reducida a 700°C parecen indicar que las mismas han experimentado cambios, comparada con las muestras reducidas a 500°C. Las conversiones disminuyen luego de someter las muestras a los tratamientos térmicos, indicativo de que se ha producido una desactivación de la muestra, posiblemente por sinterización inducida por el tratamiento de reducción [12]. Sin embargo, la muestra de CeTbOx/La2O3-Al2O3 presenta las mayores conversiones de CH4, indicando que la adición de Tb genera una superficie catalíticamente más activa. El comportamiento catalítico observado se puede correlacionar con el mayor valor de OSC reportado para este catalizador. Las muestras de CeTbOx/La2O3-Al2O3 y CeO2/La2O3-Al2O3 que fueron sometidas a ciclos sucesivos de oxidación/reducción (Tabla 6), registraron conversiones similares en todos los casos. Estos resultados son de gran interés, ya que el óxido mixto mantiene intacta su actividad luego de un tratamiento de reducción a 700°C.
Conversiones de metano registradas para los óxidos estudiados en condiciones estequiométricas y en exceso de oxígeno
| Temperatura (°C) | CeTbOx/La2O3-Al2O3 | CeO2/La2O3-Al2O3 | ||||
| Oxidación 550°C | Reducción 500°C | Reducción 700°C | Oxidación 550°C | Reducción 500°C | Reducción 700°C | |
| 23 | 10 (12) | 7 (7) | 4 (7) | 6 (5) | 5 (4) | 3 (3) |
| 100 | 12 (14) | 12 (13) | 5 (9) | 6 (5) | 7 (5) | 7 (4) |
| 200 | 21 (16) | 26 (15) | 6 (11) | 11 (8) | 8 (7) | 8 (6) |
| 300 | 30 (20) | 31 (18) | 11 (15) | 11 (17) | 8 (12) | 8 (11) |
| 400 | 81 (30) | 35 (21) | 23 (16) | 31 (29) | 9 (21) | 9 (17) |
| 500 | 98 (98) | 66 (73) | 60 (48) | 94 (73) | 22 (35) | 21 (29) |
| 600 | 100 (100) | 100 (100) | 99 (95) | 100 (100) | 100 (73) | 100 (65) |
| 700 | 100 (100) | 100 (100) | 99 (100) | 100 (100) | 100 (100) | 100 (100) |
Los valores entre paréntesis ( ) corresponden a la condición en exceso de oxígeno.
Conversiones de metano registradas para los óxidos estudiados en condiciones estequiométricas (CH4/O2=0.5) y expuestas a ciclos sucesivos de oxidación-reducción
| Temperatura (°C) | CeTbOx/La2O3-Al2O3 | CeO2/La2O3-Al2O3 | ||||
| Reducción 500°C(a) | Reducción 700°C(b) | Reducción 500°C(c) | Reducción 500°C(a) | Reducción 700°C(b) | Reducción 500°C(c) | |
| 23 | 7 (7) | 6 (6) | 7 (4) | 5 (4) | 3 (4) | 4 (3) |
| 100 | 12 (13) | 10 (10) | 11 (8) | 7 (5) | 5 (5) | 6 (3) |
| 200 | 26 (15) | 24 (12) | 25 (10) | 8 (7) | 5 (5) | 6 (4) |
| 300 | 31 (18) | 30 (15) | 31 (12) | 8 (12) | 5 (9) | 6 (4) |
| 400 | 35 (21) | 32 (18) | 33 (15) | 9 (21) | 6 (17) | 7 (15) |
| 500 | 66 (73) | 64 (60) | 65 (45) | 22 (35) | 20 (32) | 22 (20) |
| 600 | 100 (100) | 100 (75) | 100 (58) | 100 (73) | 100 (38) | 100 (34) |
| 700 | 100 (100) | 100 (92) | 100 (88) | 100 (100) | 100 (90) | 100 (78) |
(a)Muestra sometida al TSL y reducida en H2 a 500°C por 1 h. (b)Muestra proveniente de a) sometida al TSL y reducida a 700°C por 1 h. (c)Muestra proveniente de b) sometida al TSL y reducida a 500°C por 1 h. Los valores entre paréntesis ( ) corresponden a la condición en exceso de oxígeno.
Este comportamiento es contrario al observado para la muestra oxidada a 550°C y reducida a 700°C (Tabla 5) la cual mostró claramente signos de desactivación. Las muestras de CeTbOx/ SiO2 y CeO2/SiO2 no reportaron actividad catalítica. Esto posiblemente se deba a la formación de especies de silicato en el proceso de preparación, las cuales son inactivas para la reacción de combustión de metano. Los resultados de TPR (Figura 2) indican que a pesar de que las muestras presentan perfiles de reducción semejantes, su naturaleza química es distinta, dada la inactividad de las muestras soportadas sobre SiO2 para la reacción de combustión de CH4.
Las conversiones a diferentes temperaturas para la reacción de oxidación de metano en condiciones en exceso de O2 y expuesta a varios ciclos de reducción/oxidación, indicaron que el oxido mixto sufre una pérdida considerable de su actividad en el segundo ciclo.
Conclusiones
Los resultados de TPR muestran que el óxido mixto soportado mejora la reducibilidad del óxido de cerio. Los resultados de TPR obtenidos tras ciclos sucesivos de oxidación/reducción sugieren una pérdida importante de especies reducibles debido a la posible sinterización del soporte. Los óxidos soportados sobre sílice presentan mejor reducibilidad que los soportados sobre alúmina modificada con lantano; no obstante, este comportamiento no se correlaciona con las medidas de OSC y actividad catalítica. La OSC de los óxidos soportados sobre alúmina modificada incrementa con la temperatura de reducción y tiempos cortos de exposición en ambiente reductor. La introducción del ión terbio mejora la capacidad de almacenamiento de oxígeno y el comportamiento catalítico del óxido de cerio soportado sobre alúmina modificada. La ausencia de señales de hidrógeno en los experimentos de TPD sugiere la presencia de cloro, el cual podría estar inhibiendo la adsorción de hidrógeno sobre las muestras. Los resultados de actividad catalítica muestran que los catalizadores son sensibles a los tratamientos de reducción, siendo la muestra más activa la de CeTbOX/La2O3-Al2O3 luego del tratamiento estándar de limpieza. El catalizador de CeTbOX/La2O3-Al2O3 mantiene intacta su actividad catalítica luego de ser sometido a ciclos sucesivos de oxidación/reducción. La reacción de oxidación de CH4 se desfavorece bajo condiciones de exceso de O2.
Agradecimiento
Al Consejo de Desarrollo Científico y Humanístico de La Universidad del Zulia (CONDES) por el apoyo financiero prestado.
Referencias Bibliográficas
1. Harrison B., Diwell A. F. Y., Hallet C.: “Promoting platinum metals by ceria. Metal-support interactions in autocatalysts”. Platinum Met. Rev. 32(2), (1988) 73-83. [ Links ]
2. Miki T., Ogama T., Haneda M., Kakuta N., Ueno A., Tateishi S., Matsuura S., Sato M.: “Enhanced oxygen storage capacity of cerium oxides in cerium dioxide/lanthanum sesquioxide/alumina containing precious metals”. J. Phys. Chem., 94(16), (1990) 6464-6467. [ Links ]
3. Fornasiero P., Kaspar J., Sergo V., Graziani M.: “Redox Behavior of High-Surface-Area Rh-, Pt-, and Pd-Loaded Ce0.5Zr0.5O2 Mixed Oxide”. J. Catal., 167 (1997) 576-580. [ Links ]
4. Loof P., Kasemo B., Keck K.E.: “Oxygen storage capacity of noble metal car exhaust catalysts containing nickel and cerium”. J. Catal. 118(2), (1989) 339-348. [ Links ]
5. Fornasiero P., Di Monte R., Rao G.R., Kaspar J., Meriani S., Trovarelli A., Graziani M.: “Rh-Loaded CeO2-ZrO2 Solid-Solutions as Highly Efficient Oxygen Exchangers: Dependence of the Reduction Behavior and the Oxygen Storage Capacity on the Structural-Properties”. J. Catal., 151 (1995) 168-177. [ Links ]
6. Heck R., Farrauto R.: “Automobile exhaust catalysts”. Appl. Catal. A: General, 221 (2001) 443-457. [ Links ]
7. Deobert P.: “Automobiles and Pollution”. Society of Automotive Engineers, INC., Warrendal, PA, USA, (1995). [ Links ]
8. Pecchi G., Reyes P., Concha I., Fierro J. L. G.: “Methane combustion on Pd/SiO2 sol gel catalysts”. J. Catal., 179(1), (1998) 309-314. [ Links ]
9. Burch R., Urbano F. J.: “Investigation of the active state of supported palladium catalysts in the combustion of methane”. Appl. Catal. A:General, 124(1), (1995) 121-138. [ Links ]
10. Ribeiro F. H., Chow M., Dallabeta R.A.: “Kinetics of the complete oxidation of methane over supported palladium catalysts”. J. Catal., 146 (2), (1994) 537-544. [ Links ]
11. Damyanova S., Grange P., Delmon B.: “Surface characterization of zirconia-coated alumina and silica carriers”. J. Catal., 168(2), (1997) 421-430. [ Links ]
12. Finol D.: “Investigación de un óxido mixto de Ce/Tb como promotor alternativo al dióxido de cerio en catalizadores tipo TWC”. Tesis Doctoral, Universidad de Cádiz, (1999). [ Links ]
13. Bernal S., Blanco G., Cauqui M.A., Corchado M.P., Larese C., Pintado J.M., Rodriguez-izquierdo J.M.: “Cerium-terbium mixed oxide as alternative components for three-way catalysts: A comparative study of Pt/CeTbOx and Pt/CeO2 model systems”. Catal. Today, 53 (1999) 607-612. [ Links ]
14. Bernal S., Calvino J. J., Cifredo G. A., Gatica J. M., Pérez Omil J. A., Pintado J. M., Varo A.: “Hydrogen Chemisorption on Ceria: Influence of the Oxide Surface Area and Degree of Reduction”. J. Chem. Soc. Faraday Trans., 89(18), (1993) 3499-3506. [ Links ]
15. Burnham D., Eyring L., Kordis J.: “High-temperature X-ray diffraction studies of the terbium oxide-oxygen and mixed cerium terbium oxide-oxygen systems”. J. Phys. Chem., 72(13), (1968) 4424-4431. [ Links ]
16. Rocchini E., Trovarelli A., Llorca J., Grahan G., Weber W., Maciejewski M., Baiker A.: “Relationships between structural/morphological modifications and oxygen storage-redox behavior of silica-doped ceria”. J. Catal., 194(2), (2000) 461-478. [ Links ]
17. Eyring L.: “The tensimetric reflection of atomic order”. J. Solid State Chem., 1(3-4), (1970) 376-385. [ Links ]
18. Kondarides D., Verykios X.: “Effect of chlorine on the chemisorptive properties of Rh/ CeO2 catalysts studied by XPS and temperature programmed desorption techiques”. J. Catal., 174(1), (1998) 52-64. [ Links ]