Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista Latinoamericana de Metalurgia y Materiales
versión impresa ISSN 0255-6952
Rev. LatinAm. Metal. Mater. v.30 n.1 Caracas jun. 2010
Mecanismo de oxidación de un acero 1,25Cr-0,5Mo Wt% en aire a 600ºC
Yliana S. Barón*, Gladys Navas, Augusto Ruiz
Dpto. de Ciencia de los Materiales. Universidad Simón Bolívar. Caracas, Venezuela. * E-mail: ylianabaron@usb.ve
Publicado On-Line el 14-Jun-2010 Disponible en: www.rlmm.org
Resumen
Se estudió el mecanismo de oxidación de los aceros 1,25Cr-0,5Mo en aire a 600ºC mediante la evaluación por microscopía electrónica de barrido y espectroscopía de rayos X (MEB-EDX) de la sección transversal de muestras oxidadas a distintos tiempos. Se comprobó la existencia de una interfase inmóvil, que representa la superficie original de la aleación, indicada por la presencia de cromo en esa interfase, producto de la oxidación interna de ese elemento. Adicionalmente, se evidenció la formación de wustita y magnetita por mecanismos de difusión de iones de hierro vía vacancias y de hematita por difusión de iones de hierro vía intersticial, obteniéndose que la cinética de oxidación del acero en estudio está controlada por la estabilidad de la capa de magnetita. Esto fue corroborado mediante la medición continua de la ganancia de peso en función del tiempo, mediante el uso de una termobalanza.
Palabras Claves: oxidación, aceros 1,25Cr-0,5Mo.
Abstract
The mechanism of oxidation of a 1,25Cr-0,5Mo steel at 600 ºC was evaluated. The characterization of the crosssections of oxidized samples was performed with scanning electron microscopy (SEM-EDX). It was found that there is an immobile interface marked by the presence of chromium. This chromium oxide is formed by internal oxidation of this element present in the steel. It also was found that wustite and magnetite are formed due to outward cationic diffusion, but hematite is formed by the reaction between interstitial iron ions and oxygen. Thus, the oxidation rate depends of the stability of the magnetite. These results were also evaluated by the weight gain curve obtained with a thermo-balance.
Keywords: oxidation, 1,25Cr-0,5Mo steel
Recibido: 25-Feb-2009; Revisado: 22-Nov-2009; Aceptado: 16-Dic-2009
1. INTRODUCCIÓN
Diferentes autores han estudiado el mecanismo de oxidación de aceros con bajo porcentaje de cromo; sin embargo, no todos llegan a las mismas conclusiones. Kahveci et al. [1] estudiaron el mecanismo de oxidación de aleaciones Fe-3Cr wt%, estableciendo que la presencia de Cr inhibe la formación de wustita. Skalli et al. [2] estudiaron la cinética y termodinámica de oxidación de aceros al cromo-molibdeno, observando que el dominio de estabilidad de la wustita desaparece por la disolución de cromo en la magnetita y que la formación de los óxidos a temperaturas mayores a 750ºC se debe a dos mecanismos simultáneos: difusión de oxígeno hacia el interior de la aleación y difusión de hierro hacia el exterior. Singh et al. [3] estudiaron el mecanismo de oxidación de aceros 1,25Cr-0,5Mo en aire a 600ºC, observando la formación de tres capas: una capa externa formada por hematita, una capa intermedia de hematita y magnetita y una capa interna de espinela de hierrocromo. También se reporta oxidación interna. Goncharov [4] señala que es posible observar oxidación interna en aleaciones hierro-cromo debido a la oxidación de los elementos dopantes. Además, Wood [5] establece que para aleaciones de 5-10% de cromo, hay oxidación interna que conduce a la formación de la espinela Fe(Fe2-xCrx)O4. Baron et al. [6] indican que entre 500-750ºC ocurre oxidación interna de los aceros 1,25Cr-0,5Mo debido a que el cromo se encuentra en bajo porcentaje en la aleación, lo que no permite la formación de una capa continua de Cr2O3. En el presente trabajo se estudia el mecanismo de oxidación de los aceros 1,25Cr-0,5Mo en aire a 600ºC, mediante técnicas termogravimétricas, MEB y EDX.
2. METODOLOGÍA EXPERIMENTAL
Se utilizaron muestras de acero 1,25Cr-0,5Mo de aproximadamente 1*1.5*0,3 cm3; las cuales se desbastaron con carburo de silicio y pulieron con suspensión de alúmina de 1 μm hasta obtener una superficie especular. Las muestras se sometieron a ensayos de oxidación en aire estático durante 20 h, 40 h y 96 h, a 600ºC en una termobalanza. Luego de transcurrido el tiempo del ensayo de oxidación, las muestras fueron embutidas con resina epóxica, cortadas a través de la sección transversal, desbastadas y pulidas con suspensión de alúmina hasta obtener superficie especular. Luego, la sección transversal fue evaluada mediante MEB-EDX con el fin de caracterizar los productos de la oxidación. Adicionalmente se realizó ensayo de difracción de rayos X (DRX) sobre la superficie de una muestra oxidada durante 96 h, mediante radiación de cobalto.
3. RESULTADOS
En la Figura 1 se presenta la sección transversal de las muestras sometidas a oxidación en aire a 600ºC. En ella se observa la evolución del proceso de oxidación en función del tiempo. En la Figura 1a se observa la presencia de wustita (FeO), de la espinela hierro-cromo (FeO.Cr2O3), de la magnetita (Fe3O4) y de la hematita (Fe2O3); donde, la capa de oxidación total tiene un espesor aproximado de 88μm (ver en Tabla 1 los espesores aproximados de cada capa). La espinela hierro-cromo (FeO.Cr2O3) surge mediante la reacción en estado sólido de la wustita (FeO) con el Cr2O3 originado por oxidación interna. En estos aceros, la oxidación interna ocurre porque el cromo es un elemento reactivo que se encuentra en baja concentración. Así, una cantidad de oxígeno, que no es suficiente para oxidar al metal base Fe, puede difundir en la aleación causando precipitación en la sub-superficie de los óxidos del elemento aleante. De esta forma, la actividad de oxígeno dentro del metal aumenta y oxida al cromo formando islas de Cr2O3 dentro de la matriz de Fe. Sin embargo, como el cromo se encuentra en baja concentración, no se logra formar una capa continua y protectora, por lo que es posible la oxidación del hierro. Con el avance del frente de oxidación, el óxido de cromo, producto de la oxidación interna, se transforma y junto con el hierro forma la espinela, debido a la estabilidad de ésta. Luego, debido a la disminución del contenido de cromo en las zonas cercanas a la interfase metal/óxido, el proceso de oxidación continúa igual que para el caso del hierro puro, formándose las capas de Fe3O4 y Fe2O3 [1,3-5,7-11].
En la Figura 1b se presenta la sección transversal de una muestra de acero 1.25Cr-0.5Mo oxidada a 600ºC durante 40 horas. En ella se observa que el espesor de la capa de óxidos es de 122μm, mayor al espesor observado a las 18 horas, y una definición mas marcada de las tres zonas características producto de la oxidación del hierro: wustita, magnetita y hematita. Además, se aprecia la presencia de la espinela hierro-cromo, que como se explicó anteriormente es producto de la oxidación interna del cromo. Skalli et al. [2] demostraron mediante el uso de marcadores de oro depositados por PVD, que la interfase entre las capas con óxidos de cromo y las capas de óxidos de hierro (sin cromo) permanece inmóvil durante el proceso de oxidación. Por lo tanto, el cromo actúa como un marcador inerte, señalando la posición de la superficie original de la aleación. De este modo, el cromo no difunde hacia el exterior, sino que va quedando dentro de los óxidos que se van formando.
En la Figura 1c se presenta la sección transversal de la muestra sometida a 600ºC durante 96 horas; en ella se observan varias capas de distinta morfología. La capa cercana al metal base corresponde a wustita (FeO) con la presencia de espinela de cromo, la cual tiene un espesor aproximadamente igual al observado en la figura 1b. Como se explicó anteriormente, este óxido es producto de la oxidación interna y transformación del óxido de cromo [3,4] que va quedando dentro del óxido de hierro por el avance del frente de oxidación. La capa intermedia se forma por la continua difusión catiónica de hierro a través de las capas internas para formar magnetita. Pero, como el coeficiente de difusión del cromo es mucho menor que el coeficiente de difusión del hierro en la magnetita [1], éste permanece en la zona cercana a la wustita (no difunde) y reacciona con los óxidos de hierro, formando la espinela FeCr2O4 (las capas de magnetita y FeCr2O4 son la misma capa de espinela, en la que los cationes son hierro y cromo).La última capa está formada por hematita [6,11]. Al igual que en la Figura anterior (1b) se aprecia que la capa de magnetita es la que mas rápidamente aumenta su espesor; mientras que la capa de wustita (FeO + FeO.Cr2O3) tiene un espesor constante pero a mayor distancia de la superficie original de la aleación y la capa de hematita aumenta ligeramente su espesor. De este modo, se podría asumir que ocurre un crecimiento cooperativo, donde los cationes para el crecimiento de la hematita provienen de la magnetita y los aniones para el crecimiento de la magnetita, vienen de la hematita.
Schwenk y Rahmelt [12] concluyeron mediante cálculos teóricos, que es posible el engrosamiento de la capa de magnetita a expensas de la hematita. A continuación se describe el mecanismo propuesto por dichos autores y se hace una comparación entre estos resultados y los presentados en la Figura 1.
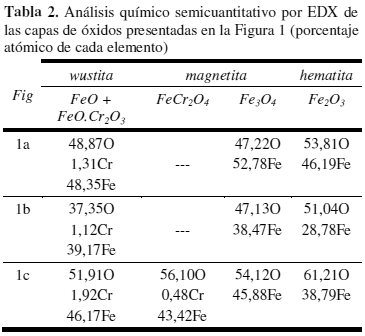
Durante las primeras 20 horas hay difusión catiónica y crecimiento de la wustita de acuerdo a la ecuación 1. En todos los casos las ecuaciones presentadas por Schwenk y Rahmelt [12] incluyen el balance simultáneo de masa, carga y sitios de red; donde, VFe y VFe representa las vacancias de hierro en los distintos estados de oxidación, h˙ a los huecos electrónicos, Oo corresponde al oxígeno, FeFe al hierro en sitios de red del óxido, Vi representa los sitios intersticiales disponibles y Fei al hierro en sitios intersticiales. El crecimiento de la magnetita, al igual que para la wustita, ocurre por difusión catiónica y de acuerdo a la ecuación 2. Para el caso de la hematita, Schwenk y Rahmelt [12] proponen dos mecanismos: (a) difusión de hierro vía intersticios hacia la interfase hematita-aire o (2) difusión de oxígeno vía vacancias aniónicas hacia la interfase magnetita-hematita. Sin embargo, en función de los resultados presentados en la figura 1b y de los EDX de la Tabla 2, se observa que la capa de hematita presenta exceso de oxígeno (o deficiencia catiónica), por lo que se considera que para el sistema en estudio el mecanismo (1) es más favorable; sin embargo, los mecanismos pueden ser simultáneos.
Para tiempos mayores, se establece una capa estable de magnetita que controla la cinética de oxidación del acero 1,25Cr-0,5Mo. Por lo tanto, continúa el crecimiento de la magnetita a expensas de la hematita y el crecimiento de la hematita debido a la difusión de hierro vía intersticial (ecuaciones 3 y 4). Adicionalmente, debido a que la capa de magnetita es la que fija la actividad de oxígeno en la superficie exterior de la capa de wustita [13], puede ocurrir la desestabilización de la wustita a magnetita como se observa en la figura 1c (ecuación 5).
Para comprobar la presencia de los óxidos identificados por EDX, se realizó difracción de rayos X sobre la superficie de una muestra oxidada durante 96 horas (ver Figura 2). Mediante esta técnica se identificó la presencia de óxido de hierrocromo (FeO.Cr2O3), que como se explicó anteriormente, surge mediante la reacción en estado sólido de la wustita con el óxido de cromo producto de la oxidación interna del acero; sin embargo, como en esta aleación el cromo se encuentra en baja concentración, no se forma una capa continua de FeO.Cr2O3, por lo que fue posible detectar FeO mediante DRX. Adicionalmente, se confirmó la presencia de espinela (Fe3O4 y FeCr2O4) y hematita (Fe2O3).
Para verificar la cinética de oxidación se realizó la medición continua de la ganancia de peso mediante el uso de una termobalanza. En la Figura 3 se presenta el cuadrado de la ganancia de peso del acero 1,25Cr-0,5Mo en función del tiempo de exposición al aire a 600ºC. En ella se observa que el comportamiento general puede ser considerado como dos comportamientos lineales, lo que denota una cinética parabólica de acuerdo a la ecuación 6.
Durante las primeras 25 horas ocurre la oxidación interna del cromo y la formación de wustita, que para temperaturas cercanas a los 600ºC se forma sobre la superficie de la muestra [14], magnetita y hematita. Para tiempos mayores, se establece una capa estable de magnetita que disminuye la velocidad de oxidación y fija la actividad de oxígeno, desestabilizando la wustita en magnetita. Por lo tanto, el carácter protector de la aleación 1,25Cr-0,5Mo viene dado por la estabilidad de la espinela y no por la formación de la capa de Fe2O3.
A pesar de las consideraciones anteriores, es posible ajustar los datos experimentales a líneas rectas con el fin de obtener la constante cinética del proceso [15], de la que se obtienen dos constantes cinéticas kp: una constante para la etapa inicial de 4,31 mg2/cm4h, y una constante para la etapa de final de 3,34 mg2/cm4h.
4. CONCLUSIONES
1. Durante la oxidación a 600ºC de los aceros 1,25Cr-0,5Mo hay formación de óxidos de cromo por oxidación interna y formación de wustita y magnetita por difusión catiónica, reacción en el estado sólido entre los óxidos de hierro y cromo, y crecimiento de la capa externa de hematita por difusión de hierro vía intersticios.
2. El mecanismo de oxidación sigue un comportamiento parabólico, donde la etapa controlante es la difusión de especies a través de la capa de espinela.
5. AGRADECIMIENTOS
Los autores desean agradecer la colaboración prestada por el Decanato de Estudios de Postgrado de la Universidad Simón Bolívar
6. REFERENCIAS BIBLIOGRÁFICAS
1. Kahveci AI, Welsch GE. Oxid. Met. 1986; 26: 213-230. [ Links ]
2. Skalli A, Galerie A, Caillet M. Solid State Ionics, 1987; 25: 27-36. [ Links ]
3. Singh Raman RK, Al-Mazrouee A. Metall. Mater. Trans. A, 2007; 38: 1750-1759. [ Links ]
4. Goncharov O. Inorg. Mater. 2004; 40: 1295-1300. [ Links ]
5. Wood GC. Corros. Sci. 1961; 2: 173-196. [ Links ]
6. Baron YS, Ruiz A, Navas G. Surf. Coat. Tech. 2008; 202: 2616-2622. [ Links ]
7. West J. Basic Corrosion and Oxidation. Inglaterra: Ellis Horwood Limited, 1980, p 163. [ Links ]
8. Stott FH, Wood GC, Stringert J. Oxid. Met. 1995; 44: 113-145. [ Links ]
9. Chang YN. Corros. Sci. 1994; 50: 3-10. [ Links ]
10. Labun PA. Metall. Trans. A. 1982; 13: 2103-2112. [ Links ]
11. Birks N, Meier G. Introduction to High Temperature Oxidation of Metals. Gran Bretaña: Edward Arnold, 1983, p 3-7, 119, 138-141. [ Links ]
12. Schwenk W, Rahmelt A. Oxid Met. 1986; 25: 293-303. [ Links ]
13. Landolt D. Traité des matériaux: corrosion et chimie de surfaces des métaux. Lausanne: Presses Polytechniques et Universitaires Romandes, 1997, p 349-352. [ Links ]
14. Chen R, Yuen W. Oxid Met. 2003; 59: 433-468. [ Links ]
15. Monceau D, Pieraggi B. Oxid Met. 1998; 50: 477-493. [ Links ]