Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de la Facultad de Agronomía
versión impresa ISSN 0378-7818
Rev. Fac. Agron. v.21 n.1 Caracas ene. 2004
Espesor de la pared celular de Rhodotorula
rubra expuesta al calor y estrés osmótico
Z. Medina de Salcedo, B. Sulbarán de Ferrer,
A. Ferrer Ocando, and G. Ojeda de Rodríguez
Laboratorio de Alimentos. Departamento de Química, Facultad Experimental de Ciencias.
La Universidad del Zulia. Apartado postal 526. Maracaibo. Venezuela
Resumen
La levadura Rhodotorula rubra se cultivó en jugo de naranja preparado a 12°Brix y 52°Brix, siendo posteriormente pasteurizado. Las células de la levadura fueron analizadas con un microscopio electrónico de transmisión, antes y después del tratamiento térmico, con el fin de verificar las modificaciones debido al estrés producido por el calor y el efecto osmótico. El espesor de la pared celular y el área del protoplasma disminuyeron ligeramente en la muestra de 52°Brix, aunque la disminución fue mucho mayor en las muestras expuestas a estrés osmótico y de temperatura.
Palabras clave: ultraestructura, pared celular, levadura, sólidos solubles, jugo de naranja.
Cell wall thickness of Rhodoturola rubra exposed to osmotic and heat stress
Abstract
Rhodotorula rubra was grown in orange juice prepared at 12ºBrix and 52ºBrix and exponed to a pasteurizing process. The yeast cell wall was analyzed Ander and electronic transmisión microscope befote and after the heat process in order to verify modifications due to heat and osmotic stress. Cell-wall thickness and protoplasmic area slightly diminished at 52ºBrix whereas the decrease was much higher when exposed to both osmotic and thermal stresses.
Key words: ultrastructure, cella wall, yeast, soluble solids, orange juice.
Recibido el 19-3-2003 Aceptado el 16-10-2003
Introducción
La contaminación microbiana más común observada en naranja y otros productos cítricos es la que está producida por la levadura, porque puede sobrevivir y crecer bajo condiciones adversas. El género de Rhodotorula es uno de los microbios mayormente aislados en jugo de naranja. En la mayoría de los casos, estos microorganismos son responsables de cambios organolépticos que ocurren en el jugo de naranja pasteurizado.
Varios estudios se han realizado con R. rubra para determinar el efecto de la concentración los sólidos solubles en su resistencia al calor. Estos estudios mostraron que la R. rubra resiste al proceso de la pasteurización bajo concentraciones 12, 20, 30, 36, 38, 40, 42, 52, 56, 58 y 62 (1.2.3.4), °Brix concluyendo que la resistencia al calor de la R. rubra aumenta al igual que la concentración en sólido soluble. Aunque el mecanismo por el que la alta concentración del azúcar ofrezca la protección del calor en levadura es desconocido, se ha sugerido que el aumento en resistencia es debido a la deshidratación pasiva del protoplasma de la célula y que los lípidos tienen un efecto protector, debido a cambios en los lípidos y/o las proteínas en la pared celular (5.6). El propósito de este estudio es examinar, bajo microscopio electrónico de la transmisión, la pared el espesor de la pared celular de R. rubra aumentada en 52 °Brix ambos antes y después tratamiento de calor, comparándolo con un control no tratado de 12 °Brix.
Materiales y métodos
Preparación de la cepa común de R. rubra.
Un volumen de 30 ml de jugo de naranja (Citrus sinensis) limpio, maduro, de las naranjas fue esterilizado en un autoclave por 15 minutos a 105 °C. Después de enfriar a temperatura ambiente, fue inoculado un cultivo con un loopful por 48 h de R. rubra e incubado por 48-72 h hasta que había 40-60 células por campo (40X) en el cultivo (1).
Preparación de muestras del jugo anaranjado.
El porcentaje de sólidos en un volumen 50-ml de jugo de naranja fue ajustado agregando la sucrosa, la glucosa y la fructosa en una proporción de 2:1:1 hasta que alcanzó un valor total aproximado de azúcar del 12% y 52%. Las concentraciones del sólido soluble fueron determinadas con un refractómetro Model Carl Zeiss 130486, que produjo lecturas directas de los porcentajes del sólido soluble (°Brix), calculado en base a un factor determinado de acuerdo con la temperatura del análisis. Tres muestras de jugo de naranja (A: 12°Brix, B: °Brix 52 y C: 52 °Brix) fueron esterilizadas en un autoclave a 105 °C por 15 minutos Después de esterilización, las muestras fueron enfriadas a temperatura ambiente, inoculados con un cultivo de solución madre de R. rubra. e incubados a 28 °C por 48- 72 h. Las muestras A y B fueron diluidas desde de 10-1 a 10-5 con agua peptonizada. Cada dilución fue rayada con 2 placas de agar de malta e incubadas a 28 °C por 48-72 h.
Prueba de la resistencia térmica.
La muestra C, del cultivo a 52 °Brix/48-72 h (de la parte previa) fue sujeto al estrés del calor a 67 °C por 15 segundos. La muestra C fue diluida desde de 10-1 a 10-5 con agua peptonizada. Cada dilución fue rayada en 2 placas de agar de malta e incubadas a 28°C por 48-72 h.
Preparación de las muestras para la microscopia electrónica.
Inmediatamente después de la incubación, se tomaron de tres a cuatro colonias para cada concentración del sólido soluble para ser estudiadas, 12 °Brix, 52 °Brix y 52 ºBrix de estrés de calor. La fijación primaria fue de 4 % de glutaraldehído por 10-12 h. Luego de la fijación estas fueron lavadas tres veces por 10 m con 0.1 M, de solución de cacodilato al pH 7.4; por cada lavada, fueron resuspendidas nuevamente con tetraóxido de osmio al 1% por 2 h como fijador secundario. Luego fueron lavadas con 0.1 M, pH 7.4 % de solución amortiguadora/buffer de cacodilato al pH 7.4 por 10 minutos y centrifugado en 5000 RPM para la fijación de 15 minutos.
Luego, fueron deshidratadas con etanol en las concentraciones de aumento de 50, 70, 80 y el 90% en 5 pases sucesivos cada uno, seguido por 2 cambios de óxido de propileno en etanol (3:1) –los primeros 1 h 30 los segundos, 2 h 30 segundos. Fueron infiltradas y colocadas en una resina de epóxido 502 de araldite (Merck, Darmstad, Alemania). Después de la polimerización en el horno a 60 °C por 72 h, estas fueron cortadas en secciones de 0.5 a 2 mm de espesor en un piramidótomo.
Las secciones Giemsa fueron manchadas y después examinadas en un microscopio de luz para verificar la presencia de la levadura. Una vez que esa presencia fuera verificada, fueron cortadas en secciones finas de 200-400 A con una hojilla ultramicrótomo de cobre de Sorvall- Porter-Blum; las secciones fueron manchadas con uranilo saturado y citrato al pH (> 7), y examinado en un microscopio electrónico Siemens Elmiskap.
El espesor de la pared celular y el área de la célula del protoplasma fueron medidos usando una lupa SPI (modelo 4863). La pared de célula y el área fueron medidas diez veces para cada una de las cinco células seleccionadas, para cada tratamiento.
El análisis estadístico, ANOVA y la prueba de Duncan fueron aplicados a las mediciones.
Resultados y discusión
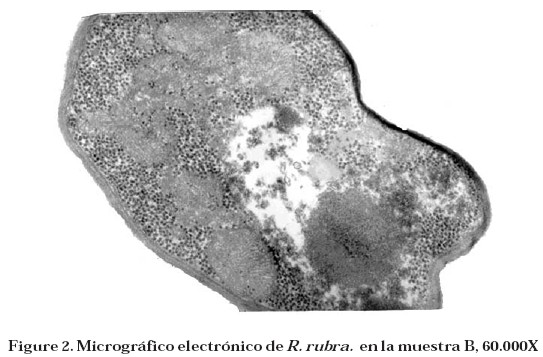
El cuadro 1 reporta el espesor de la pared celular de R. rubra. aumentada bajo condiciones de la muestra A, B, y C. El espesor medio de la pared celular fue de 61.23 nm a 12 °Brix; 55.60 nm a 52 °Brix y 37.21 nm a 52 °Brix, sujetos al estrés del calor a 67 °C por 15 s (figuras 1, 2 y 3), siendo las diferencias entre los tratamientos muy importantes (p<0,0001). No hubo diferencias importantes (p<0,05) entre las células dentro de cada tratamiento, significando que las células eran muy homogéneas dentro de cada tratamiento con muy pequeñas y similares variaciones.
Los resultados indican que el espesor de la pared celular disminuye con la actividad del agua la cual rodea la disminución de la célula, los resultados coinciden con los de otros investigadores que trabajaron en el efecto del estrés osmótico en la ultraestructura de Saccharomyces cerevisiae, mostró que la suspensión de estas levaduras en soluciones hypertónicas induce una reducción en el volumen de la pared de la célula y de la membrana plasmática (7).
También fue observado en el actual estudio una reducción considerable en el espesor de la pared celular en suspensiones de R. Rubra en ambientes hipertónicos a 67 °C por 15 segundos. Sin embargo, la literatura no menciona el efecto del calor en la pared celular en ambientes hipertónicos. Esta reducción puede ser debido al efecto del calor letal de los elementos constitutivos de la pared, proteínas entre ellos, que son muy sensibles a las altas temperaturas.
El cuadro 1 también muestra el área del protoplasma de las muestras bajo estudio. El área plasmática de la muestra A fue de 10.034 nm2; para la muestra B, 8.207 nm2 y para la muestra C, 6.771 nm2 (figuras 1, 2 y 3). Como puede ser observado, hubo una reducción en el área plasmática de 18.21% para la levadura sujeta al estrés osmótico, y una reducción de 32.52% (sin plasmólisis) para la levadura sujeta a los estrés osmóticos y de calor. Se ha reportado que la reducción en volumen del protoplasma de la célula es evidentemente osmótica y no simple un efecto electroquímico de soluciones concentradas en la estructura de la célula, como ocurre en las paredes de célula bacterianas aisladas. Otras doce especies de la levadura, entre ellas R. glutinis. y R. toruliodes, respondieron de forma similar cuando fueron expuestas a las soluciones hipertónicas con la presencia del calor, redujeron su volumen celular aún más, pero sin el plasmólisis (7).
La reducción correspondiente en la superficie del área (alrededor del 20%), fue más baja que la obtenida en ese estudio (7), y puede dar lugar a cambios a la estructura de la pared celular y a la membrana plasmática.
Estos cambios compensatorios pueden incluir cambios en densidad y/o grosor de la pared, la compresibilidad elástica 2-3% de la membrana (8), los movimientos verticales (9), liberación de las proteínas de la membrana, y finalmente un osmoregulación ocurre para prevenir muerte de la célula después del estrés hiperosmótico (8). Sin embargo, ninguna de las alteraciones arriba mencionadas que pudieron haber ocurrido eran perceptibles por transmisión de microscopia electrónica.
En estudios de S. cerevisiae sujeto al estrés osmótico con el cloruro de sodio, fue encontrado que una contracción inmediata de la célula fue producida por la reducción del agua, pero 2 horas después del máximo estrés osmótico, las células restauraron su volumen celular. Este proceso es relacionado con la actividad de la síntesis de la proteína. Durante el período de recuperación, las células acumulan el glicerol intracelular como un soluto compatible, para restaurar la presión del turgor de la célula y el incremento de la célula cuando la glucosa se utiliza como fuente del carbón (9, 10). Con técnicas electrónicas de la microscopia de la transmisión, no se observó ningunas ordenaciones químicas moleculares en la pared de célula, las ordenaciones que se podrían evidenciar con técnicas immunocytochemical.
El efecto de tensión del calor puede aumentar la sensibilidad de las levaduras a componentes específicos, tales como losque constituyen los de aceites esenciales (11). Este descubrimiento es de relevancia para los jugos cítricos porque contienen los aceites esenciales, aunque la R. rubra es una de las levaduras que su sensibilidad fue afectada lo menos posible.
En la respuesta osmótica de la reducción de la célula y su volumen celular cuando es expuesta a las soluciones hipertónicas moderadas, se han observado en una gran cantidad de células plantadas, y se refiere como mecanismo protector que evita mayores daños a la célula (12). Quizás, esto es una respuesta a lo que sucede en R. rubra cuando es sumergida a altas concentraciones de sólidos solubles y al calor.
Por otra parte, algunos estudios condicionan el aumento de la resistencia térmica debido a la deshidratación pasiva del protoplasma celular, según lo observado en el presente estudio (5).
Conclusiones
El espesor de la pared celular disminuye mientras que la actividad del agua en el medio que rodea la célula disminuye también, y hubo una reducción del área de la célula de 32.52% sin plasmólisis cuando la R. rubra es sujeta a las tensiones osmóticas y de calor.
Agradecimiento
Los autores desean agradecer a La Universidad del Zulia y al Consejo de Desarrollo Científico y Humanístico (CONDES) por su ayuda financiera.
Literatura citada
1. Medina de Salcedo, Z., S. de Ferrer, B., Ferrer, A. y O. de Rodríguez, G. 2001.Resistencia térmica de levaduras en jugo de naranja a diferentes concentraciones de sólidos solubles. Archivos Latinoamericanos de Nutrición. 51(2):167-172 [ Links ]
2. Sulbarán de Ferrer, B., D. Trávez, A. Ferrer, G. Ojeda de Rodríguez, and R. Nava. 1998. Effect of sugar concentration and pasteurization on survival of Rhodotorula rubra and Candida intermedia in orange juice. Rev. Fac. Agron. (LUZ), 15(3):256-261 [ Links ]
3. Fennema, O.R. (Ed.). 1975. Physical principles of food preservation. Ed. Dekker. New York. pp. 199-202. [ Links ]
4. Walter, R.P., J.G. Morris and D.B. Kell. 1987. The roles of osmotic stress and water activity in the inhibition of the growth, glycolisis and glucose phosphotransferase system of Clostridium pasteurianum». J.Gen.Microbiol. 133:259-266. [ Links ]
5. Morris G.J., L. Winters G.E. Coulson and K.J. Clarke. 1983. Effect of osmotic stress on the ultrastructure and viability of the yeast Saccharomyces cerevisiae. J. Gen. Microbiol. 129: 2023-2030. [ Links ]
6. Wolfe, J. and P. Steponkus. 1981. The stress: strain relation of the plasma membrane of isolated protoplasts. Biochem. Biophys. Acta. 643: 663-668. [ Links ]
7. Neidermeyer, W., G. Parish, and H. Moor. 1976. The elasticity of the yeast cell tonoplast related to its ultrastructure and chemical composition. 1. Induced swelling and shrinkage: heeze-etch membrane study. Cytobiol. 13:364- 374.
8. Martínez de Marañón, I., P. Marechal, and P. Gervais. 1996. Passive response of Sacharromyces cerevisiae to osmotic shift: cell volume variations depending on the physiological state. Biochem. Biophys Res. Commun. 227:519- 523. [ Links ]
9. Blomberg, A. and L. Adler. 1992. Physiology of osmotolerance in fungi. Adv. Microb. Physiol. 33:145-212. [ Links ]
10. Van Eck, J., B. Prior and E. Brandt E. 1993. The water relations of growth and polihydroxy alcohol production by ascomicetous yeast. J. Gen. Microbiol. 139:1047-1054. [ Links ]
11. Albertyn, J., S. Hohman and B. Prior. 1984. Characterization of the osmotic- stress response in Saccharomyces cerevisiae: osmotic stress and glucose repression regulate glycerol-3-phosphate dehydrogenase independently. Curr. Genet. 25: 12-18. [ Links ]
12. Conner, D. and L. Beuchat. 1984. Sensitivity of heat-stressed yeast to essential oils of plants. Appl. Environ. Microbiol. 42: 229-233. [ Links ]