Investigación Clínica
versión impresa ISSN 0535-5133
Invest. clín v.47 no.1 supl.1 Maracaibo mar. 2006
Eritema fijo pigmentario medicamentoso relacionado con el uso de carbamazepina: Presentación de un caso.
Verónica J. Álvarez-H.1, Jesús E. Picón-C.1, Alexis R. Morales-O.2, Edith T. Goncalves-F.2 y José Rafael Luna2.
1Laboratorio de Toxicología, Hospital Universitario de Los Andes y
2Departamento de Toxicología y Farmacología, Facultad de Farmacia y Bioanálisis. Universidad de Los Andes. Mérida, Venezuela. Correo electrónico: lunajr@ula.ve
Resumen:
La Carbamacepina es una droga anticonvulsivante bien tolerada y que origina la aparición de efectos adversos dermatológicos de manera poco frecuente. En este reporte, se describe el caso de un paciente del sexo femenino, quien acudió al Servicio Farmacocinético Clínico del Laboratorio de Toxicología del Hospital Universitario de los Andes, solicitando la realización de niveles de Carbamacepina, por presentar en sus manos manchas hipercrómicas, concéntricas y pruriginosas, de aparición a los 6 meses de iniciado el tratamiento con dicho medicamento; los niveles terapéuticos reportaron un valor de 8,51 μg.mL–1, ubicados dentro de rango terapéutico 4-12 μg.mL–1. Luego de ser remitida al servicio de Dermatología, le fue diagnosticado: eritema fijo pigmentario medicamentoso, el cual comenzó a desaparece a los 15 días de haber suspendido la carbamazepina y con un tratamiento coadyuvante de ungüento magistral.
Palabras clave: Carbamazepina, reacción adversa, eritema fijo pigmentario medicamentoso.
Fixed pigmented erythema related to the oral administration of Carbamazepine: Report of one case.
Abstract.
Carbamazepine (CBZ) is an oral anticonvulsant drug, structurally similar to tricyclic antidepressants. It is preferred over other drugs because it has fewer adverse effects on behavior and alertness. However, hematologic toxicity is possible during therapy with CBZ. Patients should undergo routine monitoring of hematologic function. CBZ can make the skin more sensitive to the sun or ultraviolet light, therefore, dermatological effects of this drug also can happen such as, skin rash, urticaria, and erythema multiforme. The present study reports the case of a female patient that presented hyperchromic-concentric-pruriginous- spots on the skin of her hands after six months of treatment with CBZ. She came to the physicians of the Clinical Pharmacokinetic Service (Laboratory of Toxicology of IAHULA, Mérida-Venezuela) requesting a drug monitoring. The results showed a level of 8,51 μg.mL–1, which was found within the therapeutic range (4-12 μg.mL–1). Subsequently, the dermatologist diagnosed fixed pigmented erythema related to the ingestion of a specific medication which began disappearing after 15 days of CBZ free-treatment and with the aid of a dermatologic formulation.
Key words: Carbamazepine, fixed pigmented erythema, adverse effects.
Recibido: 19-10-2004. Aceptado: 21-07-2005.
INTRODUCCIÓN
La carbamazepina (CBZ) es un derivado tricíclico del iminostilbeno, con un grupo carbamilo en la posición 5; esta mitad es esencial para la actividad anticonvulsiva (1). Fue desarrollado originalmente para el tratamiento de la depresión bipolar y en 1962 introducido en el tratamiento de la neuralgia del trigémino, además demostró ser útil para la epilepsia, por lo que más tarde la Food and Drug Administration (FDA) la aprobó como agente antiepiléptico para los pacientes de más de 6 años de edad, dándole este uso clínico desde 1974 (2).
Además de sus efectos terapéuticos, también se han reportado reacciones secundarias dérmicas adversas, tales como exantemas, urticaria, eritema multiforme, síndrome Stevens– Johnson. Raramente se ha observado un síndrome similar al lupus eritematoso sistémico, dermatitis exfoliativa y eritroderma (3-5). En casos aislados se han reportado necrólisis epidérmica tóxica, fotosensibilidad, alteraciones de la pigmentación cutánea, púrpura, acné, sudores y caída del cabello, el cual es un efecto adverso ocasional de muchas drogas neurofarmacológicas (6-7). Las reacciones pueden aparecer luego de 2 meses de iniciado el tratamiento con CBZ, denominándose así Síndrome de Hipersensibilidad Tardía, y el mismo es independiente de la concentración plasmática del medicamento (4, 8-13).
Es importante destacar, que los efectos secundarios relacionados a la carbamazepina pueden ser disminuidos si se comienza con dosis bajas, aumentándolas progresivamente y conservando una concentración plasmática mínima efectiva. Sin embargo, como en la mayoría de los antiepilépticos, sus efectos terapéuticos o tóxicos correlacionan mejor con su concentración plasmática que con la dosis (2,14).
En este trabajo se presenta un caso probable de eritema fijo pigmentario medicamentoso, descrito en un individuo tratado con carbamazepina, con la finalidad de brindar un antecedente registrado en la Ciudad de Mérida, Estado Mérida.
PRESENTACIÓN DEL CASO
Paciente femenina de 13 años de edad, natural de San Simón, Estado Táchira y procedente de El Vigía, Estado Mérida, Venezuela; conocida por el servicio de Neurología por ser portadora de Síndrome Epiléptico Parcial Criptogénico con electroencefalograma focal paroxístico centro temporal izquierdo y tratada con CBZ, quien ingresó al Instituto Autónomo Hospital Universitario de Los Andes (IAHULA) presentando manchas hipercrómicas de forma concéntrica y pruriginosas, en el dorso de la mano y región anterior del antebrazo de ambos miembros superiores. Las lesiones en su inicio fueron de color rojo tornándose luego de una coloración parda, las zonas afectadas presentaron cierta inflamación con pequeñas vesículas que posteriormente desaparecieron en forma espontánea, permaneciendo la hiperpigmentación (Fig. 1).
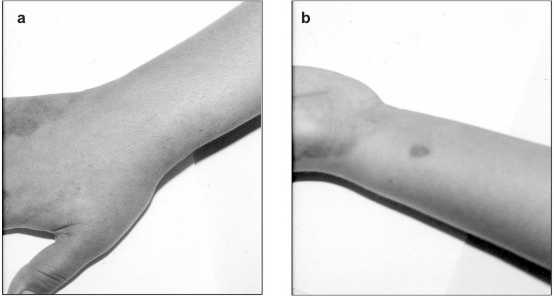
La paciente refiere haber iniciado el tratamiento desde hace 6 meses con CBZ, a una dosis de 500 mg/día, durante los 3 primeros meses, sin control adecuado del cuadro clínico; por lo que el neurólogo tratante, le aumentó la dosis a 600 mg orden diaria (O.D) con aparente control de episodios convulsivos.
En virtud a la aparición de la afección cutánea y para precisar niveles terapéuticos de CBZ, es remitida al Laboratorio de Toxicología del Hospital Universitario de Los Andes adscrito al Departamento de Toxicología y Farmacología de la Facultad de Farmacia y Bioanálisis, reportándose una concentración de 8,51 μg.mL–1, cifra encontrada dentro del rango terapéutico (4-12 μg.mL–1) (9). Para la realización de este análisis se utilizó el método de Inmunoensayo por Polarización de Fluorescencia (FPIA), empleando el equipo TDx de Abbot. Posteriormente es remitida al servicio de Dermatología para ser valorada, donde se le diagnostica eritema fijo pigmentario medicamentoso.
Debido a la reacción adversa presentada con el uso terapéutico de CBZ, se le sugiere consultar con el servicio de Neurología a fin de cambiar la CBZ, siendo reemplazada por el ácido valproico (40 mg/kg/ día). Tras suprimir gradualmente la CBZ, a las 2 semanas, comenzó notablemente a desaparecer el eritema, eliminándose por completo en un lapso de 2 meses.
Como medida coadyuvante se utilizó tratamiento de uso externo, Ungüento Magistral: Elomet® (Furoato de mometasona), Oxido de Zinc, Talco, Vaselina, Lanolina, aplicado 3 veces al día por 1 mes.
DISCUSIÓN
El eritema fijo pigmentario medicamentoso, aunque infrecuente, es una de las reacciones adversas cutáneas producidas con el uso terapéutico de la CBZ; caracterizada por una lesión eritemato-violácea circular u oval, localizada en cualquier sitio, que recidiva con la readministración del medicamento. La lesión activa se acompaña de edema o incluso de la formación de una vesícula (que se resuelve con rapidez) pero que al involucionar deja una mancha hiperpigmentada de color pardo y persistente (8).
En la paciente, la reacción adversa, se presentó a los 6 meses de iniciado el tratamiento con CBZ, siendo valorada por el servicio de Dermatología previa monitorización de los niveles del medicamento.
Existen casos, en los cuales las reacciones adversas comunes no generan en los exámenes de laboratorio de rutina alteraciones específicas, como ejemplo se puede citar el caso de una mujer de 71 años de edad, con una lesión eritematosa a consecuencia de haber tomado 100 mg de CBZ, debido a una neuralgia del trigémino, cuyo contaje de células sanguíneas fue normal (15). Por otra parte, se han reportado desordenes hematológicos (leucocitopenia, eosinofilia y trombocitopenia) y en las pruebas de funcionalismo hepático asociados a reacciones alérgicas, en pacientes epilépticos, bajo terapia con CBZ (3, 16-18). Sin embargo, el dermatólogo tratante no ordenó la realización de exámenes de laboratorio, ni biopsia de piel, sino orientado por la clínica de la paciente, diagnosticó las lesiones como eritema fijo pigmentario medicamentoso. Dentro de las medidas terapéuticas a seguir, se le indicó la suspensión gradual de CBZ, observándose a las 2 semanas la desaparición progresiva del eritema. Es importante resaltar, que la paciente, durante el tratamiento con CBZ no se le prescribió el uso concomitante de otros medicamentos descartándose por lo tanto posibles efectos de interacción farmacológica (2, 9, 19-20).
A pesar que el mecanismo de producción del eritema fijo pigmentario medicamentoso no se ha dilucidado completamente, su aparición se ha atribuido a la deficiencia de la epóxido hidrolasa, enzima responsable de la desintoxicación de los intermediarios reactivos (arilaminas) generados por las enzimas citocromo P450 a partir de la CBZ (8).
En los pacientes es fundamental la prevención de la aparición de este tipo de reacciones adversas dermatológicas inducidas por medicamentos. Aunque, se considera que los efectos adversos dermatológicos de la carbamazepina son más frecuentes en los pacientes psiquiátricos que en los neurológicos, siendo el caso aquí presentado un paciente neurológico (21). Actualmente se recomienda una mayor relación médico–paciente a fin de indagar si el paciente ha presentado reacciones de hipersensibilidad previa a medicamentos. Además, algunos investigadores han sugerido parches con el medicamento aplicado sobre la piel para predecir o corroborar hipersensibilidad dérmica al medicamento (15, 22).
Para reacciones leves (exantemas), la suspensión del medicamento será suficiente, pudiéndose añadir lociones emolientes antipruriginosas, o corticoides tópicos de menor o mayor potencia según la naturaleza de la lesión, y por vía sistémica (23).
Finalmente, es importante mencionar que desde el año 2000 hasta agosto del 2003 en el IAHULA, todos los casos registrados de reacciones adversas a la CBZ se corresponden con reacciones tóxicas, debido a la ingestión de dosis superiores a 2 g (24), por lo que el caso aquí reportado se convierte en uno de los primeros mediante el uso de dosis terapéuticas de CBZ.
REFERENCIAS
1. Hardman J, Limbird L, Molinoff P, Raymond R, Goodman A. Las bases farmacológicas de la terapéutica. 9 ed. México, D.F.: Editorial Mc Graw-Hil Interamericano; 1996. [ Links ]
2. De los Santos A. Uso de eutímicos en psiquiatría infanto-juvenil. Rev Psiquiatr Psicol Niño y Adolesc 2001; 2(1):41-8. [ Links ]
3. Konishi T, Naganuma K, Murakami M, Yamatani M, Okada T. Carbamazepine-induced skin rash in children with epilepsy. Eur J Pediatr 1993; 152:605-608. [ Links ]
4. Klassen B, Sadler R. Induction of hypersensitivity to a previously tolerated antiepileptic drug by a second antiepileptic drug. Epilepsia 2001; 42(3): 433-435. [ Links ]
5. Feliciani C, Verrotti A, Coscione G, Toto P, Morrelli F, Di Benedetto A, Salladini C, Chiarelli F, Tulli A. Skin reactions due to anti-epileptic drugs: several case-reports with long-term follow-up. Int J Immunopathol Pharmacol 2003; 16(1): 89-93. [ Links ]
6. Lacy C Armstrong L, Goldman M, Lance L. Drug Information Handbook. 9 ed. Cleveland, USA: Lexi-Comp Inc; 2001-2002. [ Links ]
7. Kohno Y, Ishii A, Shoji S. A case of hair loss induced by carbamazepine. Rinsho Shinkeigaku 2004; 44(6):379-381. [ Links ]
8. Fitzpatrick TB. Reacciones Cutáneas a Fármacos. Dermatología en Medicina General. 5 ed. Buenos Aires, Argentina: Editorial Médica Panamerica; 2001. [ Links ]
9. Sociedad Española de Neurología, Liga Española Contra la Epilepsia. Epilepsia. Madrid: Ergon; 2003. [ Links ]
10. Kamini K, Sant K. Unusual reactions to carbamazepine: areport of 2 cases in India. Indian J Pharmac 1990; 22:110-112. [ Links ]
11. Durán E, Mir J, Morales M, Martínez P. Síndrome de hipersensibilidad por antiepilépticos con repercusión cutánea y renal grave por carbamazepina. Rev Neurol 2004; 38(2):1136-1138. [ Links ]
12. Troost R, Van Parys J, Hooijkaas H, Van Joost T, Benner R, Prens E. Allergy to carbamazepine: parallel in vivo and in vitro detection. Epilepsia. 1996; 37(11):1093-1099. [ Links ]
13. Schlienger R, Shear N. Antiepileptic drug hypersensitivity síndrome. Epilepsia 1998; 39(7):S3-7. [ Links ]
14. Gómez B, Tejeiro J. Farmacos antiepilepticos y laboratorio: monitorización de niveles plasmáticos y controles bioquímicos y hematológicos periódicos. Rev Neurol Clin 2000; 1: 326-338. [ Links ]
15. de Argila D, Angeles M, Rovira I. Carbamazepine-induced fixed drug eruption. Allergy 1997; 52(10):1039. [ Links ]
16. Garavelly P, Azzini M. Skin rash induced by carbamazepine. Description of 2 clinical cases. Minerva Med 1990; 81(7-8):115-116. [ Links ]
17. Galindo P, Borja J, Gomez E, Mur P, Gudin M, Garcia R, Encinas C, Romero G, Garrido J, Cortina P, Feo F. Anticonvulsant drug hypersensitivity. J Invest Clin Immunol 2002; 12(4):299-304. [ Links ]
18. Hómez A, Jiménez M, Luna J, Salazar J, Peña J. Trastornos hematológicos en pacientes tratados con carbamazepina, que acuden al Instituto Autónomo Hospital Universitario de Los Andes, Mérida, Venezuela. Rev Fac Farmacia 2004; 46(1): 22-26. [ Links ]
19. Zarranz J. Epilepsia. Compendio de Neurología. Madrid, España: Ediciones Harcourt; 2001. [ Links ]
20. Ashmark H, Wiholm B. Epidemiology of adverse reactions to carbamazepine as seen is a spontaneous reporting system. Acta Neurol Scand 1990; 81:131-140. [ Links ]
21. Ramadasan P, Chaudhury S, Vaishampayne S, John T. Stevens_Johnson syndrome due to carbamazepine. J Assoc Physicians India. 2000; 48(7): 742-743. [ Links ]
22. Alanko K. Contact dermatitis. 1993; 29(5):254-257. [ Links ]
23. Mc Van BF. Carbamacepina. Índice de Medicamentos. 1 ed. en español (traducida de la 5ª Edición en ingles). México: El Manual Moderno, S.A.; 1995. [ Links ]
24. Departamento de Registros y Estadísticas de Salud del Instituto Autónomo Hospital Universitario de Los Andes. Morbilidad Hospitalaria. Mérida, Venezuela. [ Links ]
Autor de correspondencia: José Rafael Luna. Departamento de Toxicología y Farmacología, Facultad de Farmacia y Bioanálisis, Universidad de Los Andes. Mérida, Venezuela. Correo electrónico: lunajr@ula.ve












 uBio
uBio 
