Saber
versión impresa ISSN 1315-0162
Saber vol.26 no.3 Cumaná set. 2014
Características tintoriales de Neisseria gonorrhoeae por la tinción diferencial de fluorescencia modificada
Staining characteristics of Neisseria gonorrhoeae by modified differential fluorescent staining method
Evelin Margarita Flores Fernández, Susanny del Carmen Caraballo Suniaga, Luzmila Sofía Albarado Ysasis
Universidad de Oriente, Núcleo de Sucre, Escuela de Ciencias, Departamento de Bioanálisis, Cumaná, Venezuela. E-mail: eve_linff@yahoo.com
RESUMEN
Son pocas las técnicas de coloración de fluorescencia utilizadas en estudios del ciclo celular bacteriano, de manera que se evaluaron las características tintoriales de Neisseria gonorrhoeae con la tinción diferencial de fluorescencia modificada y la asociación con la presencia de ADN y ARN. El propósito del estudio fue aportar evidencias sobre el mecanismo de reacción de la tinción de fluorescencia modificada, así como la de ofrecer esta técnica como una herramienta complementaria en estudios del ciclo celular. A los aislamientos de N. gonorrhoeae se les realizó el ciclo celular transfiriendo un cultivo en crecimiento óptimo a un caldo BHI con 5% de sangre humana. Se tomaron alícuotas para realizar extendidos para la tinción, pre y post tratamiento con ADNasa y ARNasa a intervalos de 5 a 120 min, y se aplicó la prueba de McNemar para verificar la asociación de la reactividad tintorial antes y después del tratamiento enzimático. En el ciclo celular, la tinción de la bacteria fue predominante el anaranjado ligeramente fluorescente y la secuencia de color en el ciclo fue amarillo, anaranjado y verde. Las células que se tiñeron de anaranjado o amarillo, después del tratamiento enzimático, cambiaron a verdes ligeramente fluorescentes o verdes casi imperceptibles, existiendo asociación estadísticamente significativa (p < 0,05) entre el color amarillo y anaranjado ligeramente fluorescente o fluorescente con presencia de ADN y ARN. Se concluye que el ADN y ARN participan en el carácter tintorial amarillo y anaranjado ligeramente fluorescente o fluorescente del método de coloración diferencial de fluorescencia modificado en el ciclo celular de N. gonorrhoeae.
Palabras clave: Ciclo celular, ADN, ARN, ADNasa, ARNasa.
ABSTRACT
There are few fluorescent staining techniques used in studies of the bacterial cell cycle, so that the staining characteristics of Neisseria gonorrhoeae were analyzed by the modified differential fluorescent staining method and the association with the presence of DNA and RNA. The purpose of this study was to provide evidence on the reaction mechanism of modified differential fluorescent staining method, as well as offering the technique as a complementary tool in studies of the cell cycle. The cell cycle was evaluated in isolates of N. gonorrhoeae transferring a culture in optimal growth to BHI broth with 5% human blood. Aliquots were taken to prepare slide spreads for staining, before and after treatment with DNase and RNase at 5 to 120 min intervals, and the McNemar test was applied to verify the association of the staining reactivity before and after enzyme treatment. In the cell cycle, the bacteria staining was predominantly slightly fluorescent orange and the color sequence in the cycle was yellow, orange and green. Cells which stained orange or yellow, after the enzyme treatment, changed to slightly fluorescent green or almost imperceptible green, with statistically significant association (p < 0,05) between the yellow and orange slightly fluorescent or fluorescent with the presence of DNA and RNA. We conclude that DNA and RNA are involved in the yellow and orange dye by modified differential fluorescent staining method in the cell cycle of N. gonorrhoeae.
Key words: Cell cycle, DNA, RNA, DNase, RNase.
Recibido: marzo 2014. Aprobado: junio 2014. Versión final: julio 2014.
INTRODUCCIÓN
Las coloraciones diferenciales de fluorescencia, en el estudio microscópico de los frotis, se aplican desde que Kronvall y Myhre (1977), introdujeron el fluorocromo naranja de acridina para la detección de bacterias. En el año 2002, Fazii et al. observaron que bacterias grampositivas y gramnegativas teñidas con naranja de acridina eran decoloradas diferentemente con alcohol etílico-acetona, ideando así un método de coloración diferencial para la detección y distinción de bacterias grampositivas y gramnegativas por fluorescencia. Ellos utilizaron dos fluorocromos: naranja de acridina y fluoresceína de sodio; las bacterias grampositivas se tiñen de amarillo fluorescente y las gramnegativas de verde fluorescente. La hipótesis que manejaron para explicar el mecanismo de tinción se fundamentó en la interacción del naranja de acridina con componentes de la pared celular, tales como polisacáridos y lipopolisacáridos. Probablemente, en las bacterias gramnegativas, al decolorar con alcohol etílico-acetona se desestabiliza la membrana externa rica en lipopolisacáridos, removiéndose parcialmente el naranja de acridina e incorporándose la fluoresceína y así se tiñen de color verde. Sin embargo, el alcohol etílico-acetona produce poco cambio en las bacterias que retienen el naranja de acridina (grampositivas), éstas se observan de color amarillo cuando al fluorocromo rojo, naranja de acridina, se le añade el segundo fluorocromo verde, fluoresceína de sodio. Los investigadores la aplicaron en extendidos de secreciones uretrales de pacientes con cultivos positivos para N. gonorrhoeae y los gonococos se visualizaron verdes fluorescentes.
Posteriormente, Flores et al. (2008), publicaron un estudio que evaluó la coloración diferencial de fluorescencia, introduciendo una modificación en el pH de la solución colorante de fluoresceína, con el propósito de mejorar la fluorescencia emitida por las bacterias. Detectaron que los diplococos emitieron un tinción distinta a la referida por Fazii et al. (2002), observándose anaranjados fluorescentes, no obstante, esta variación en la tinción no se han dilucidado, sugiriendo que podría estar relacionada al proceso de transcripción de ARN durante el ciclo celular. A propósito de la modificación de la técnica, se ha publicado que la coloración diferencial de fluorescencia modificada representa una contribución significativa como herramienta en el diagnóstico de gonorrea en muestras perianales y uretrales, teniendo mayor capacidad discriminatoria que la tinción de Gram, especialmente, en los pacientes asintomáticos, lo que sería importante para el control de la enfermedad (Flores y Albarado 2009a).
Basado en la similitud entre las propiedades moleculares del ADN y ARN de células eucariotas y procariotas, en el presente estudio se plantea una hipótesis para explicar la reacción de coloración del método de tinción diferencial de fluorescencia modificada. Ésta se fundamenta sobre los principios químicos de coloración, por lo que, la hipótesis sobre las variaciones de color es apoyada con el trabajo de Darzynkiewicz (1990), quien señala que el naranja de acridina es un colorante catiónico y metacromático, que emite fluorescencia cuando interactúa con los ácidos nucleicos. Con el ADN se intercala produciendo una coloración verde fluorescente y con el ARN interactúa expresando una tonalidad rojo fluorescente. Las variaciones de color observadas con la tinción diferencial de fluorescencia modificada, posiblemente, se fundamentan en los procesos de síntesis de ADN y ARN en el ciclo celular bacteriano, naturaleza química y mecanismo de acción del naranja de acridina sobre los ácidos nucleicos, de manera que, en esta investigación, se planteó como objetivo evaluar las características tintoriales de N. gonorrhoeae obtenidas por la coloración diferencial de fluorescencia modificada y asociarlas con la presencia de ADN y ARN antes y después de tratamiento con ADNasa y ARNasa, con el fin de aportar una evidencia sobre el mecanismo de reacción de la coloración de fluorescencia modificada en N. gonorrhoeae, ya que se ha demostrado que es útil en el diagnóstico oportuno de pacientes asintomáticos; así como ofrecer la técnica como una herramienta complementaria en los estudios del ciclo celular bacteriano.
MATERIALES Y MÉTODOS
Se evaluaron siete aislamientos de N. gonorrhoeae procedentes de 18 muestras uretrales de pacientes masculinos con sospecha de infección que acudieron a la consulta de Infecciones de Transmisión Sexual del ambulatorio "Dr. Arquímedes Fuentes Serrano", Cumaná, estado Sucre, en el periodo febrero-mayo 2011. La recolección de las muestras fue realizada por el médico especialista, jefe del área de ITS-SIDA, bajo estrictas normas de ética médica, según la declaración de Helsinki (AMM 2008) y aprobado por la Comisión de Trabajo de Grado y Ética del Departamento de Bioanálisis, Universidad de Oriente, Núcleo de Sucre, así como también cumpliendo con las normas del Código de Ética para la Vida (MPPCTII 2010). El estudio bacteriológico se realizó siguiendo los protocolos convencionales de cultivo, aislamiento e identificación de N. gonorrhoeae (Koneman et al. 1999, Pardi et al. 2004).
Crecimiento y ciclo celular de Neisseria gonorrhoeae
Para lograr que las células de un cultivo alcancen la fase de crecimiento óptimo para desarrollar los experimentos, se inoculó una colonia a partir del cultivo primario, en agar GC de la estirpe a trabajar, en 3 mL de caldo infusión cerebro corazón (BHI) enriquecido con sangre humana al 5%, incubándolo a 37ºC en ambiente de microaerofilia, entre 16 y 18 h (Salguero 2007, Li et al
. 2014).Sobre la base de estudios de crecimiento de
N. gonorrhoeae en medio líquido, se estima que la fase de crecimiento exponencial se inicia en la primera hora después de haber sido transferido un cultivo a otro medio de composición idéntica y continúa durante las siguientes 7 h (Jones y Talley 1976), de modo que, para obtener esta fase de crecimiento y una población bacteriana sincrónica para el estudio del ciclo celular, se transfirieron cinco gotas del cultivo BHI enriquecido con 5% de sangre humana, a un caldo fresco del mismo medio de cultivo, incubándose por 1 h a 37ºC. A partir de este cultivo, se realizó el ciclo celular, tomando alícuotas para realizar los extendidos desde el tiempo 0 min hasta los 120 min, a intervalos de 5 min.Elaboración de extendidos
Se realizaron extendidos para el pre y post tratamiento enzimático. Los extendidos se elaboraron con, aproximadamente, 1 μL de la alícuota tomada, en portaobjetos nuevos, se fijaron con calor, se colorearon con la tinción de fluorescencia modificada y se observaron al microscopio de epifluorescencia.
Tinción diferencial de fluorescencia modificada
Se preparó el colorante naranja de acridina (Sigma- Aldrich, USA) al 0,7% (p/v) en buffer acetato pH 4,0. El buffer acetato pH 4,0 se preparó mezclando 82 mL de ácido acético 0,2 mol.L-1 con 18 mL de acetato de sodio 0,2 mol.L-1. El decolorante alcohol etílico-acetona se preparó en una proporción 1:1. La solución de fluoresceína de sodio se ajustó a un pH de 6,5 y se preparó al 0,002% en alcohol etílico. Un volumen de 100 mL de solución contenía 2 mg de fluoresceína de sodio (Sigma-Aldrich, USA), 1,5 mL de ácido acético 0,4 mol.L-1, 0,5 mL de buffer acetato pH 4,6 y 98 mL de alcohol etílico. El buffer acetato contenía 52 mL de ácido acético 0,2 mol.L-1 y 48 mL de acetato de sodio 0,2 mol.L-1. La lámina preparada con el extendido se cubrió con la solución naranja de acridina durante 2 min, luego, se lavó con agua de chorro y se procedió a decolorar con alcohol etílico-acetona, exactamente, por 10 s, inclinando la lámina en un ángulo de 45o, se enjuagó nuevamente; se aplicó la solución de fluoresceína de sodio por 2 min y se eliminó el colorante con agua. Se dejó secar para su observación con microscopio de epifluorescencia (Flores et al. 2008).
Tratamiento con las enzimas ADNasa y ARNasa
La enzima ADNasa RQ1 libre de ARNasa (Promega, USA), degrada cadenas simples y dobles de ADN, produciendo oligonucleótidos 3´-OH. La enzima se diluyó en una proporción 1:1 con el tampón de reacción 10X (400 mmol.L-1 de Tris-HCl [pH 8,0 a 25°C], 100 mmol.L-1 de MgSO4, 10 mmol.L-1 de CaCl2). Se colocó 1 μL de la enzima ADNasa diluida sobre los extendidos del ciclo celular para la digestión de ADN, dejándose reaccionar por 48 h a 37ºC en cámara húmeda. La enzima ARNasa ONE ribonucleasa (Promega, USA), cataliza la degradación del ARN a nucleótidos de monofosfatos cíclicos. Para la degradación de ARN, se colocó sobre los extendidos del ciclo celular, 1 μL de la enzima ARNasa ONE ribonucleasa (Promega, USA) con una dilución previa de 1:10 con el tampón de reacción 10X (100 mmol.L-1 de Tris-HCl [pH 7,5 a 25°C], 50 mmol.L-1 de EDTA, 2 mol.L-1 de acetato de sodio) por 48 h a 37ºC en cámara húmeda.
Identificación microscópica
láminas se observaron con magnificación de 1000x, empleando un microscopio de epifluorescencia Olympus BX 60. Para la coloración de fluorescencia modificada se empleó un filtro de excitación azul de banda amplia de 450-480 nm, espejo dicromático de 500 nm y un filtro de barrera de 515 nm. Las fotomicrografías fueron tomadas con una cámara digital marca Motic modelo Moticam Cooled 3000.
Controles
Para el control de las diferentes tinciones se utilizaron las cepas Staphylococcus aureus ATCC 25923 como control de bacteria grampositiva y Escherichia coli ATCC 25922 como control de bacteria gramnegativa. Estas cepas se procesaron del mismo modo que los aislamientos de N. gonorrhoeae evaluados y, adicionalmente, se les realizaron cultivos sincronizados, los cuales están compuestos por células donde todas se encuentran en la misma etapa del ciclo celular, permitiendo estudiar la sucesión de eventos que se llevan a cabo en una sola célula (Brooks et al. 2002). El método excelente de selección para obtener cultivos sincrónicos es la técnica de Helmstetter-Cummings (HC), basado en el hecho que algunas bacterias se adhieren fuertemente a las membranas de filtros de nitrato de celulosa (Stainer et al.
1991).Se colocó una colonia con crecimiento de 24 h de los controles en caldo triptosa fosfato (TF) y se dejó por 16-18 h. Para obtener un cultivo sincronizado de cada control, se colocaron cinco gotas del cultivo bacteriano del medio TF sobre una membrana de filtro de nitrato de celulosa con poros de 0,2 μm y diámetro de 47 mm. La membrana se colocó dentro de una placa de Petri estéril, se incubó a 37ºC por 1 h o hasta que el líquido fue absorbido. Inmediatamente, se procedió a lavar suavemente con 5 mL de cultivo fresco de caldo TF, empleando pipeta Pasteur estéril, con el fin de separar aquellas células ligadas débilmente a la membrana, las cuales corresponden a las células recién formadas y que se encuentran en la misma etapa del ciclo celular, conservando la sincronía por 2 h, aproximadamente. El lavado se recogió en tubos secos estériles y correspondieron a los cultivos sincrónicos que se emplearon para realizar el estudio microscópico del ciclo celular de los controles.
Análisis estadístico
Se construyeron tablas de 2 x 2, para expresar las frecuencias observadas. Asimismo, se aplicó la prueba de McNemar, para asociar la reactividad tintorial por el método de coloración diferencial de fluorescencia modificada antes y después del tratamiento con ADNasa y ARNasa en
los aislamientos de N. gonorrhoeae (Pértega y Pita 2004).RESULTADOS
Características morfotintoriales por tinción de fluorescencia modificada de Neisseria gonorrhoeae en el ciclo celular
Se observaron mono, diplococos y el color predominante en el ciclo celular de N. gonorrhoeae fue el anaranjado ligeramente fluorescente, observándose dicha fluorescencia en 103 tiempos (Fig. 1) y la secuencia de color fue amarilla, anaranjada y verde. En la Figura 2 se muestran las características tintoriales por el método de tinción diferencial de fluorescencia modificada presentadas por la bacteria en los diferentes tiempos del ciclo celular.
Asociación entre la reactividad tintorial en el ciclo celular de Neisseria gonorrhoeae por la coloración diferencial de fluorescencia modificada con presencia de ADN y ARN, antes y después de tratamiento con ADNasa y ARNasa
Con la coloración de fluorescencia modificada, las células que se tiñeron de anaranjado o amarillo, después del tratamiento con ADNasa y ARNasa, se colorearon verdes ligeramente fluorescentes o verdes casi imperceptibles. Para determinar la asociación entre la reactividad tintorial por fluorescencia con presencia de ADN y ARN, mediante la degradación con las enzimas ADNasa y ARNasa, se seleccionaron aquellos tiempos donde los mono y diplococos presentaron, exclusivamente, una intensidad de fluorescencia antes del tratamiento: amarillo ligera o intensamente fluorescente, y anaranjado ligera o intensamente fluorescente. De manera que, se seleccionó un total de 75 tiempos con
tinción amarilla, de los cuales 67 tiempos presentaron células con intensidad de fluorescencia ligera y ocho fueron intensamente fluorescentes. Del mismo modo, se seleccionaron 63 tiempos con bacterias anaranjadas, 52 ligeramente fluorescentes y 11 fluorescentes.En la asociación entre la reacción de tinción amarillo ligera o intensamente fluorescente con presencia de ADN hubo 61 pares de tiempos discordantes, en donde el 98,36% (60/61) de los pares de tiempos presentó mono y diplococos con tinción amarillo ligera o intensamente fluorescente y cambiaron a verde ligeramente fluorescente o fueron poco perceptibles después del tratamiento con ADNasa. En la asociación con presencia de ARN, se obtuvo 53 pares de tiempos discordantes, en donde el 98,11% (52/53) de los pares de tiempo, mostró células que se colorearon anaranjado ligeramente fluorescente o fluorescente y presentaron cambio después del tratamiento, existiendo asociación estadísticamente significativa (
p < 0,05) entre el color amarillo ligeramente fluorescente o fluorescente y la presencia de ADN y ARN (Tabla 1).Con respecto a la asociación entre la tinción anaranjado ligera o intensamente fluorescente con presencia de ADN, se obtuvo 37 pares de tiempos discordantes, en donde en el 94,59% (35/37) de los pares de tiempo, las células que se colorearon anaranjado ligeramente fluorescente o fluorescente se visualizaron verde ligeramente fluorescente o fueron poco perceptibles después del tratamiento con ADNasa.
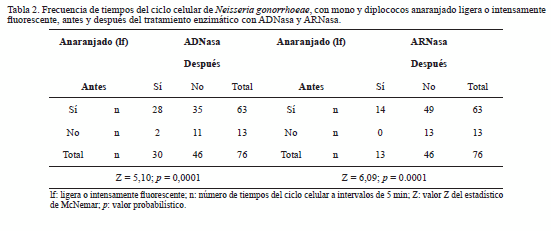
En la asociación con presencia de ARN, hubo 49 pares de tiempos discordantes, en donde en el 100% (49/49) de los pares de tiempos, las células que se colorearon anaranjado ligeramente fluorescente o fluorescentes cambiaron de color después del tratamiento con ARNasa, existiendo asociación estadísticamente significativa (p < 0,05) entre el color anaranjado ligeramente fluorescente o fluorescente y presencia de ADN y ARN (Tabla 2).
El control grampositivo S. aureus ATCC 25923 y el gramnegativo E. coli ATCC 25922, mostraron el mismo patrón tintorial de fluorescencia, que los desarrollados en N. gonorrhoeae, durante el ciclo celular. Se halló asociación estadísticamente significativa (p < 0,05) entre la tonalidad amarilla y anaranjada con síntesis de ADN y ARN.
DISCUSIÓN
Al observar que las células de N. gonorrhoeae presentan cambios de color después de un tratamiento con ADNasa y ARNasa y establecerse una asociación estadísticamente significativa (p < 0,05) entre las características tintoriales con la presencia de ADN y ARN, se demuestra que la reactividad tintorial por fluorescencia se está llevando a cabo por interacción con los ácidos nucleicos; así pues las diferentes tonalidades encontradas en el ciclo celular de N. gonorrhoeae se explican por el mecanismo de tinción del colorante naranja de acridina sobre el ADN y ARN.
Mecanismo de tinción del naranja de acridina
El naranja de acridina es un colorante catiónico y metacromático, que colorea ortocromáticamente al ADN, y le imparte color verde. Al ARN lo tiñe metacromáticamente de rojo. La coloración del ARN, probablemente, siga el principio general del mecanismo de metacromasia; cuando el naranja de acridina interactúa con una cadena simple en espiral aleatoria, como lo es el ARN, se une a casi todos los nucleótidos por su grupo fosfato de carga negativa, permitiendo el acercamiento entre las moléculas del colorante, de modo que, éstas interactúan y forman un polímero, produciendo una fluorescencia metacromática roja.
Se ha establecido que hay dos procesos por los cuales el naranja de acridina se une al ADN: un proceso de unión fuerte, en el cual predomina un alto radio molar de fosfato del ADN al colorante; y un proceso de unión débil con menor radio molar. Cuando los cationes del naranja de acridina se unen en la doble cadena de ADN, se intercala cada tercer par de bases púricas o pirimídicas y forman un complejo estable, mediante uniones iónicas y uniones dipolo-dipolo. En estas condiciones la distancia entre las moléculas es lo suficientemente grande para prevenir la interacción colorante-colorante, de forma que la fluorescencia que se obtiene es la de un monómero de naranja de acridina, con emisión de color verde (Rost 1995).
Las variaciones de tinción e intensidad de fluorescencia observadas en los mono y diplococos coloreados con la tinción diferencial de fluorescencia modificada, posiblemente, están asociadas a los mecanismo de replicación y transcripción del ADN.
Hipótesis del mecanismo de coloración de la tinción diferencial de fluorescencia modificada
El fluorocromo naranja de acridina doble sal hemi (C17H20ClN3HCl.1/2ZnCl2), de carácter fuertemente básico, presenta mayor afinidad por estructuras de carga negativa, como los ácidos nucleicos de la célula, impidiéndose la remoción del colorante naranja de acridina con el alcohol etílico-acetona en aquellas bacterias donde la síntesis de ARN sea mayor, la fluoresceína a baja concentración no ejercería el efecto diferencial, adquiriendo, por lo tanto, una coloración anaranjado fluorescente. Por otro lado, las bacterias que no se encuentran en proceso de síntesis de ARN son decoloradas completamente tras la aplicación del alcohol-acetona, manifestando una tinción verde fluorescente o de baja fluorescencia, que puede estar asociada a síntesis de ADN. La tinción amarilla se produce dado que el naranja de acridina es removido parcialmente, pudiendo este hecho estar relacionado con una síntesis no tan activa de ARN, y al incorporar la fluoresceína de sodio se forma el sistema rojo/verde (Flores et al.
2008).Las variaciones de tinción por el método de coloración de fluorescencia modificado, también se han reportado en otros géneros bacterianos como
Pseudomonas, Staphylococcus, Streptococcus y Enterococcus (Albarado y Flores 2008, Flores y Albarado 2009b). Albarado y Flores (2008) proponen por primera vez un patrón de tinción por fluorescencia asociado a fases del ciclo celular bacteriano, sobre la base de que dicho ciclo comprende una secuencia de acontecimientos interconectados, como la fase B, que es el período en el que ocurre una activa síntesis de ARN y proteínas, además, de otros componentes celulares; una fase C, caracterizada por la replicación del ADN cromosómico y una fase D que es el tiempo entre la finalización de la replicación y terminación de la división. Los investigadores sugirieron, que el color verde correspondía a la fase C, y que dicho color se presentaba, posiblemente, como producto de la intercalación del naranja de acridina al ADN. La tonalidad amarilla de baja fluorescencia, tal vez, representa a la fase D, así como también a la B, ya que observaron un incremento paulatino de la tonalidad amarilla a medida que transcurría el tiempo en el ciclo celular y la presencia de estructuras redondas amarillas, las cuales sugirieron que se trataban de nucleoides, lugar donde se inicia el proceso de síntesis de ARN; infirieron también que la tonalidad amarilla de baja fluorescencia se debe a una menor cantidad de ARN; por último la tonalidad anaranjada fluorescente, corresponda a la fase B en donde pueda existir un alto contenido de ARN y que al interactuar con el naranja de acridina se produzca dicho color.Los cambios de color visualizados por la tinción de fluorescencia representan fases del ciclo celular bacteriano, sugiriéndose, asociación del color anaranjado a una síntesis activa de ARN (Flores
et al. 2008). En esta investigación se obtuvo que en un alto número de pares de tiempos discordantes (49) se observaron células anaranjadas con intensidad de fluorescencia variable, confirmándose su asociación con la presencia de ARN. Después del tratamiento con ADNasa, aunque, en un menor número de pares de tiempos (35), se advirtió que desapareció el color anaranjado, constatándose asociación con la presencia de ADN. Se explica que el ADN induce metacromasia sobre el naranja de acridina, cuando el polímero de ADN de doble cadena cambia a cadena simple (Pal y Ghosh 1973). En los procesos de síntesis de ADN y ARN, hay tres momentos en donde el ADN puede estar en la configuración de cadena simple. En la replicación a nivel del origen de replicación, el ADN de doble cadena se convierte en ADN de cadena simple, al romperse los enlaces de hidrógeno por la acción de proteínas y enzimas. En la transcripción, en la etapa de iniciación se forma la burbuja de transcripción, en la cual se produce un desenrollamiento de la molécula de ADN en, aproximadamente, 20 pares de base, y en la fase de terminación de la transcripción, se produce el desenrollamiento del complejo ARNm-ADN por el factor rho (ρ) (Prescott et al. 2004). Es posible que, cuando el naranja de acridina interactúa con el ADN, lo esté haciendo con cadenas simples de ADN, de allí la asociación, entre el color anaranjado con ADN, sin embargo, no se puede especificar, cuál de estos momentos corresponde, requiriéndose de más estudios para ello.Se concluye que la secuencia de color del método de tinción diferencial de fluorescencia modificada en el ciclo celular de
N. gonorrhoeae es amarillo, anaranjado y verde, el color predominante es el anaranjado ligeramente fluorescente y, el ADN y ARN participan en el carácter tintorial amarillo y anaranjado ligeramente fluorescente o fluorescente en el ciclo celular de N. gonorrhoeae.AGRADECIMIENTO
A la Dra. Mireya Acuña, jefa del aérea de ITS-SIDA, las enfermeras Natalí, Luz Marina e Ingrid, quienes
gratamente colaboraron en la atención al paciente y toma de muestras y al Consejo de Investigación de la Universidad de Oriente, por el aporte financiero del proyecto CI-2-040102-1677/10.
REFERENCIAS BIBLIOGRÁFICAS
1. Albarado L, Flores E. 2008. Evaluación de la coloración diferencial de fluorescencia modificada en Pseudomonas
spp. aisladas de suelo. Kasmera. 36(1):17-27. [ Links ]2. A
MM (Asociación Médica Mundial). 2008. Declaración de Helsinki. 59na Asamblea General, Seúl, Corea, octubre de 2008.3. B
rooks GF, Butel JS, Ornston LN, Jawetz E, Melnick JL, Adelberg EA. 2002. Microbiología de Jawetz, Melnick y Adelberg. Manual Moderno, Ciudad de México, México, pp. 700. [ Links ]4. Darzynkiewicz Z. 1990. Differential staining of DNA and RNA in intact cells and isolated cell nuclei with acridine orange. Methods Cell Biol. 33:285- 298.
5. Fazii P, Ciancaglini E, Riario G. 2002. Differential fluorescent staining method for detection of bacteria in blood cultures, cerebrospinal fluid and other clinical specimens. Eur. J. Clin. Microb. Inf. Dis. 21(5):373-378.
6. Flores E, Albarado L. 2009a. Tinción diferencial de fluorescencia modificada en el diagnóstico de N. gonorrhoeae y correlación clínico-tintorial del diplococo. Salus. 13(3):42-48.
7. Flores E, Albarado L. 2009b. Ciclo celular por Gram y tinción de fluorescencia modificada en bacterias con aspecto morfotintorial semejante a Neisseria gonorrhoeae aisladas de muestras perianales y uretrales. NOVA. 7(11):27-33.
8. Flores E, Albarado L, Thomas D, Lobo A. 2008. Comparación de la tinción fluorescencia modificada y Gram, en muestras urogenitales y perianales de pacientes asistidos en el área de infecciones de transmisión sexual del ambulatorio Arquímedes Fuentes, Cumaná, estado Sucre. Salus. 12(2):29-35.
9. Jones RT, Talley RS. 1976. Simplified complete medium for the growth of Neisseria gonorrhoeae
. J. Clin. Microbiol. 5(1):9-14.10. K
oneman E, Allen S, Janda W, Schreckenberger P, Winn W. 1999. Diagnóstico microbiológico. Texto y atlas color. Editorial Médica Panamericana, Buenos Aires, Argentina, pp. 1432.11. K
ronvall G, Myhre E. 1977. Differential staining of bacteria in clinical specimens using acridine orange buffered at low pH. Acta Pathol. Microbiol. Scand. B. 85(4):249-254.12. L
i G, Xie R, Zhu X, Mao Y, Liu S, Jiao H, Yan H, Xiong K, Ji M. 2014. Antibodies with higher bactericidal activity induced by a Neisseria gonorrhoeae Rmp deletion mutant strain. PLoS One 9.(3):e90525. doi: 10.1371/journal.pone.0090525.13. MPPCTII (
Ministerio del Poder Popular para Ciencia, Tecnología eIndustrias Intermedias). 2010. Código de Ética para la Vida. Disponible en línea en: http://www.coordinv.ciens.ucv.ve/investigacion/coordinv/index/CONCIENCIA/codigoe.pdf. (Acceso 22.01.2011).14. Pal MK, Ghosh AK. 1973. Stoich iomet r y of metachromatic dye binding by deoxyribonucleic acid. Histochemie. 36(1):29-33.
15. Pardi G, Pérez MF, Pacheco A, Mata M. 2004. Algunas consideraciones sobre Neisseria gonorrhoeae. Acta Odontol. Venez. 42(2):57-63.
16. Pértega S, Pita S. 2004. Asociación de variables cualitativas: el test exacto de Fisher y el test de McNemar. Cad. Aten. Primaria. 11:304-308.
17. Prescott LM, Harley JP, Klein DA. 2004. Microbiología. McGraw Hill-Interamericana de España, Madrid, España, pp. 992.
18. Rost FWD. 1995. Fluorescence microscopy. Volumen II. Cambridge University Press, Great Britain, pp. 473.
19. Salguero I. 2007. Replicación genética en presencia de una nucleósido-difosfato reductasa codificada por el alelo nrdA101 de Escherichia coli. Badajoz: Universidad de Extremadura, Facultad de Ciencias, Departamento de Bioquímica, Biología Molecular y Genética [Memoria presentada para optar al título de Doctor en Biología], pp. 214.
20. Stainer R, IgrahamJ, Wheelis M, Painter P. 1992. Microbiología. Editorial Reverte S.A. Barcelona, España, pp. 768.












 uBio
uBio