Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de Ciencias Sociales
versión impresa ISSN 1315-9518
Revista de Ciencias Sociales v.16 n.2 Marcaibo jun. 2010
Regulación en el mercado farmacéutico colombiano (1)
Vásquez Velásquez, Johanna* Gómez Portilla, Karoll** Rodríguez Acosta, Sandra***
* Economista Universidad de Antioquia y Magister en Economía de la Salud del Centro de Investigaciones y Docencia Económicas -CIDE- México. Docente Catedrático de la Universidad Nacional de Colombia sede Medellín. Núcleo del Volador, Bloque 46, Medellín, Colombia. E-mail: jovasquezve@unal.edu.co Docente Investigadora, del Departamento de Economía de la Facultad de Ciencias Económicas de la Universidad de Antioquia. Bloque 13, oficina 109. Apartado aéreo 1226, Medellín, Colombia. Investigadora Grupo de Econometría Aplicada -GEA-, Centro de Investigaciones Económicas -CIC- Universidad de Antioquia y Centro de Estadística Aplicada a Estudios Socioeconómicos -CEAES-. Universidad Nacional de Colombia, sede Medellín. Núcleo. E-mail: jovasve@economicas.udea.edu.co (autor para envío de correspondencia).
** Economista y Magister en Economía Universidad de Antioquia. Docente e investigadora. Facultad de Ciencias Humanas y Económicas. Universidad Nacional de Colombia, Sede Medellín. Investigadora Grupo de Econometría Aplicada -GEA-, Centro de Investigaciones y consultarías -CIC-, Universidad de Antioquia y Centro de Estadística Aplicada a Estudios Socioeconómicos -CEAES-. Universidad Nacional de Colombia, sede Medellín. Núcleo del Volador, Bloque 46, Medellín, Colombia. E-mail: kgomezp@unal.edu.co.
*** Economista y Magister en Economía de la Universidad de Antioquia. Estudiante del Doctorado en Economía Universidad de Barcelona. Docente e investigadora, Departamento de Economía, Universidad del Norte - Barranquilla. E-mail: rsandra@uninorte.edu.co.
Resumen
La industria farmacéutica es un sector estratégico en la mayoría de los países y se caracteriza por una estructura oligopólica intensiva en conocimiento y tecnología, por lo que es una de las industrias más influenciadas por la regulación, siendo tres sus objetivos principales: preservar los incentivos para las actividades de I&D, certificar la seguridad y efectividad de los medicamentos y controlar la cantidad y calidad del gasto. Así, con el objetivo de analizar el cumplimiento de estos tres propósitos en el sistema regulatorio de la industria farmacéutica colombiana se realiza una investigación exploratoria y descriptiva que se basa en la revisión de literatura e información secundaria. Del análisis se puede concluir que la reglamentación en Colombia se ha desviado de los objetivos propuestos en términos teóricos y se ha orientado principalmente a temas de organización, dejando de lado aspectos que faciliten el pleno abastecimiento de medicamentos a través de los canales de distribución institucional y privado.
Palabras clave: Colombia, industria farmacéutica, regulación, gasto en medicamentos, control de precios.
Regulation in the colombian pharmaceutical market
Abstract
The pharmaceutical industry is a strategic sector in most countries. It is characterized by an oligopolistic structure, intensive in knowledge and technology, due to which it is a heavily regulated industry. The regulatory controls are intended to preserve R & D incentives, certify the safety and effectiveness of medicines and control the quantity and quality of expenditure. The objective of this study was to analyze fulfillment of these three purposes in the pharmaceutical industry's regulatory system in Colombia. The research was descriptive and exploratory, based on a review of literature and secondary information. The analysis led to conclusions that regulations in Colombia have deviated from the objectives proposed in theoretical terms and are oriented mainly toward market organization, ignoring aspects that facilitate a full supply of drugs through institutional and private distribution channels.
Key words: Colombia, pharmaceutical industry, regulation, drug expenditure, price control.
Recibido: 09-05-19 · Aceptado: 09-12-05
Introducción
Podría decirse que los mercados de salud están conformados por cuatro industrias: el seguro de salud, los servicios médicos, los servicios de hospitalización y los medicamentos (Santerre et al., 2000a y 2000b), cada una con su propia forma de organización y comportamiento sectorial. Particularmente, el sector farmacéutico se caracteriza por la gran inversión en investigación y desarrollo -I&D- y publicidad, altas tasas renovación y diferenciación de productos, la generación de beneficios financieros a las empresas y pacientes a estos últimos a través de reducciones en el número de muertes, en el costo de los tratamientos y en los días de hospitalización (2).
Lo anterior propicia una interacción entre oferta y demanda en un ambiente de mercado que difiere de otras industrias, por el lado de los consumidores se destaca la participación de varios agentes en la adquisición del bien y los fallos de información, y por el lado de los vendedores sobresale el poder de mercado que ganan las firmas a través del establecimiento de monopolios legales, fidelidad a la marca y selección adversa. Tales características permiten ubicar al sector farmacéutico en un escenario de mercado especialmente complejo con múltiples fallos, lo que genera incentivos para la intervención del estado ya sea a través de la intervención directa, ofreciendo incentivos al sector privado o como a través de la estabilización, asignación y distribución (Stiglitz, 2002). En consecuencia, los gobiernos han desarrollado sistemas para regular la industria, haciendo un seguimiento cercano a cada uno de los aspectos relacionados con el ciclo de vida del medicamento: pruebas, producción, mercadeo, distribución y precios.
Colombia no es un país ajeno a dicha problemática y el mercado farmacéutico se caracteriza por presentar una fuerte interacción entre productores privados y distribuidores del sector público, tener un listado de medicamentos genéricos y esenciales a los que tienen derecho los afiliados a la seguridad social, presentar dos canales de distribución y por tener una política de regulación de precios y de concentración del mercado que en muchas ocasiones desconoce las particularidades del sector. Sumado a lo anterior, las investigaciones y discusiones académicas se han concentrado en la Ley 100 de 1993, Ley que reformó el Sistema Nacional de Salud y dio inicio al Sistema General de Seguridad Social en Salud -SGSSS-, y las implicaciones de la Sentencia T760 de 2008 que modifica algunas disposiciones de la mencionada Ley, sin considerar el gran impacto que el sector farmacéutico tiene en el funcionamiento y logros del sistema de salud en general. De los trabajos académicos se destacan: Rossi (2003 y 2009), Archila y Meléndez (2005), Mojica, Villamil (2002), Jiménez y Hurtado (2005) e ICEX (2005).
En este sentido, este artículo describe en cuatro secciones las características claves del sistema regulatorio de la industria farmacéutica y se aplica el análisis al caso colombiano. En la primera sección se muestra de manera general el papel de la regulación en el sector farmacéutico desde el punto de vista teórico, en la segunda se describe la composición y regulación del mercado farmacéutico en Colombia, en la tercera se realiza un análisis de la normatividad vigente a la luz de los tres objetivos claves de la regulación en el mercado de medicamentos, donde se presenta un análisis de concentración de mercado para 224 medicamentos, 65 componentes activos y 811 concentraciones farmacéuticas en un período de ocho años, mostrando además el posible impacto de la política de precios. Finalmente se presentan las discusiones finales.
1. Aspectos teóricos sobre la regulación en la industria farmacéutica
Desde una perspectiva económica, la regulación se refiere al uso de mecanismos de no-mercado para direccionar la cantidad, el precio o la calidad de los bienes comprados en el mercado. Así cuando hay razones para creer que las fuerzas de mercado en una industria no son fuertes, los gobiernos pueden considerar alternativas de intervención tales como la regulación y la provisión pública (3). Estas alternativas, son incluso más probables de ser consideradas cuando los bienes intercambiados son necesarios e implican substanciales gastos para los consumidores.
Analíticamente, las razones que justifican la regulación en el sector salud tienen que ver con el logro de la equidad y la eficiencia (Jacobzone, 2000). La primera apunta a la realización de acciones públicas tendientes a mejorar el acceso de los grupos más pobres, redistribuir oportunidades y dar asistencia a grupos sociales menos favorecidos. Por su parte, el segundo se fundamenta en las características de la salud como bien público, teniendo en cuenta las externalidades asociadas a las acciones de salud pública que se puedan llevar a cabo pues, aunque el mercado privado pueda ejercer algún rol cuando las acciones de salud generan importantes externalidades el hecho de que quien demanda los servicios no valore el beneficio a terceros genera que dichas acciones se lleven a cabo en una escala económicamente ineficiente (Mushkin, 1958). Por tanto, en estos casos se requiere la gestión del Estado para asegurar que las acciones curativas y preventivas se provean.
Así dentro del sector salud, la industria farmacéutica cobra vital importancia debido a dos características fundamentales: i) su producto principal se constituye en el insumo más usado en casos de enfermedad o malestar ya que la forma en que terminan la mayoría de los encuentros médico/usuario-paciente es con una prescripción médica; ii) el gasto en medicamentos es el segundo rubro más importante del gasto en servicios de salud. Dichas características convierten a la farmacéutica en una de las industrias más influenciadas por la regulación, siendo tres los objetivos principales de ella: 1. Calidad de los medicamentos, 2. Acceso total o parcial a un conjunto de medicamentos y 3. Contención del gasto (Vincenzo et al., 2008).
En este sentido, el diseño de una correcta política de medicamentos debe basarse en: corregir las fallas de mercado y generar un cuerpo regulatorio saludable lo que constituye el marco general de política, desarrollar medidas que garanticen un acceso equitativo que incluya desde la mayor difusión de información hasta el desarrollo de programas focalizados de cobertura, y finalmente, coordinar dichas políticas dentro de una estrategia multisectorial de la cual se desprenda una lógica de atención, o lógica de contexto. De este modo, la selección de las acciones de política que tiendan a cubrir estos objetivos generales depende de las características de cada uno de los actores participantes, y de las posibilidades del Estado para generar respuestas a los diferentes problemas (Bisang et al., 1999).
Bajo estas consideraciones y siguiendo los objetivos de la política regulatoria se deben establecer las variables centrales a regular sobre cada uno de los actores de la industria farmacéutica, los cuales van desde el productor, prescriptor y farmacéuticos hasta los medios de comunicación; siendo los derroteros de la misma la búsqueda de medicamentos seguros, eficaces y de calidad. En este sentido y a partir de la revisión de la literatura se pueden agrupar en cuatro los aspectos susceptibles de regulación en el mercado farmacéutico tal como se muestra en la Tabla I.
Tabla I. Esferas de regulación en el mercado farmacéutico
| Aspectos a regular | Ítems |
| Comerciales |
|
| Sanitarios |
|
| Calidad |
|
| Información |
|
Fuente: Adaptado de Organización Mundial de la Salud -OMS- Effective drug regulation A multicountry study (2002).
En cuanto a la regulación de precios se podría decir que la mayoría de los países adoptan prácticas directas o indirectas justificadas por el supuesto de que la competencia en precios en este mercado es débil por varias razones: intencionalmente las patentes limitan la competencia y conducen a la diferenciación del producto; el seguro hace a los pacientes insensibles al precio y los médicos son los tomadores de decisiones primarios y pueden o no conocer el precio del producto generando un problema de agencia donde el agente (prescriptor) puede ser perfecto o imperfecto para los pacientes (Danzon et al., 2000).
2. El mercado farmacéutico en Colombia
En 1993 se reestructuró en Colombia el Sistema Nacional de Salud y se dio inicio al Sistema General de Seguridad Social en Salud -SGSSS-. Tal reforma opera bajo la estrategia de aseguramiento universal con los objetivos de regular el servicio público esencial de salud y crear condiciones de acceso en toda la población en todos los niveles de atención. A dicho sistema los colombianos pueden afiliarse bajo alguno de los dos sistemas de aseguramiento: régimen contributivo para los que tienen capacidad de pago y al régimen subsidiado la población pobre y vulnerable beneficiaria de subsidios parciales o totales. Ambos regímenes cuentan con empresas aseguradoras o Entidades Promotoras de Salud -EPS- encargadas de la afiliación y de suministrar el plan único de protección integral denominado Plan Obligatorio de Salud -POS- diferenciado por régimen de aseguramiento e incluye atención preventiva, médico-quirúrgica y un listado de medicamentos genéricos y esenciales; dichas entidades contratan a su vez la entrega de servicios de salud con Instituciones Prestadoras de Servicios de Salud -IPS- y/o profesionales.
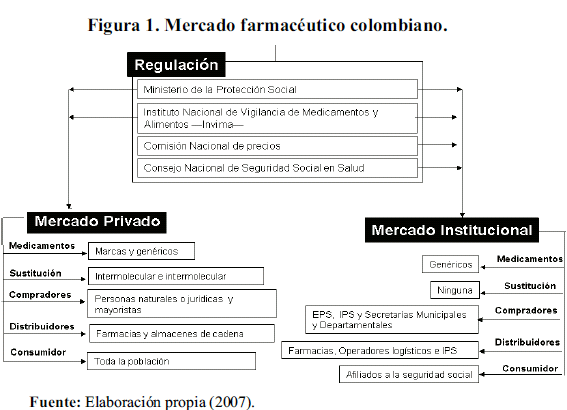
Básicamente el Sistema General de Seguridad Social en Salud, incorporó a los planes de beneficios dos instrumentos de política farmacéutica bien definidos: los medicamentos esenciales (4), como el mecanismo de seleccionar los mejores medicamentos para las patologías más frecuentes (corresponden a la lista de medicamentos de los planes de beneficios del sistema: el plan de atención básica y el plan obligatorio de salud); y los medicamentos genéricos, como el mecanismo de introducir competencia en el mercado entre productores de moléculas iguales (5) y además procuraba que el médico fuera un agente cada vez menos imperfecto del paciente. Dadas las particularidades mencionadas, se puede decir que en el mercado de medicamentos colombiano coexisten dos submercados derivados de los dos canales de distribución de medicamentos: el denominado institucional, para los afiliados al sistema de seguridad social, y el privado. En ambos casos las diferencias más importantes se presentan en los canales de distribución al consumidor final y en las posibilidades de sustitución.
En el mercado privado, la distribución y entrega de medicamentos se realiza a través droguerías y almacenes de cadena y la sustitución puede darse entre moléculas (intermolecular) o entre productores de marca y genérico (intramolecular) y puede ser realizada por quien prescribe, quien distribuye y quien consume, esto significa que el médico tiene la posibilidad de elegir entre moléculas iguales y de prescribir el medicamento bajo su nombre de marca o genérico, el distribuidor por su parte puede tener incentivos para sugerir el consumo de medicamentos de marca o genéricos y el consumidor puede estar motivado por los precios, publicidad o fidelidad a la marca a comprar uno u otro y consumir medicamentos tanto del mercado ético como del de venta libre.
Dentro del mercado institucional los medicamentos genéricos y esenciales son entregados por las IPS o por farmacias adscritas a la EPS del afiliado, previa prescripción médica, por lo que se podría considerar que todos los medicamentos se distribuyen en el mercado ético y según la clasificación anatómica, terapéutica y química conocida mundialmente como Anatomical Therapeutic Chemical -ATC- el listado de medicamentos al que tienen derecho los afiliados a la seguridad social no cuenta con moléculas que puedan reemplazarse unas con otras. Esto significa que desde el punto de vista económico en este submercado no existe la posibilidad sustitución ni a nivel intramolecular ni a nivel intermolecular. En la Figura 1 se muestra la organización del mercado de medicamentos en Colombia.
En ambos mercados la función de regulación es ejercida por el Ministerio de la Protección Social que es el máximo Organismo de Dirección del Sistema de Seguridad Social en Salud, entre sus funciones está expedir el Manual de Normas Técnicas de Calidad o las Guías Técnicas de Análisis y desarrollar un programa permanente de información sobre precios y calidad de los medicamentos. También se vale de un grupo de organismos e instituciones adscritos a él que se encargan de aspectos específicos en beneficio del buen funcionamiento del mercado y relacionados con calidad y precio. Entre los organismos adscritos se destaca la Comisión Nacional de Precios de Medicamentos (6) -CNPM- conformada por el Ministerio de la Protección Social, el Ministerio de Hacienda, un delegado del presidente y un grupo técnico asesor y se encarga de coordinar la acción de las diferentes entidades estatales y lograr el establecimiento de una política de precios que tenga en cuenta la capacidad adquisitiva de los consumidores; la rentabilidad razonable de la industria productora y comercializadora; el impacto social de los precios y las particularidades del mercado farmacéutico actividades que aplican a ambos mercados.
3. Análisis de esferas y de objetivos de la regulación en Colombia
Luego de revisar las esferas regulatorias a nivel teórico y de hacer su tipificación se realizó la lectura y clasificación de la normatividad del sector teniendo en cuenta Acuerdos; Circulares; Decretos; Leyes y Resoluciones desde 1993 hasta abril de 2009. Del análisis realizado se encontró que la regulación del mercado farmacéutico en Colombia se ha concentrado en aspectos organizativos relacionados con la reestructuración de los entes reguladores, distribución de recursos y funcionamiento de los regímenes de aseguramiento (7), representando estos aspectos el 38% de la normatividad. Así, el 23% corresponde a aspectos de calidad, 17% a aspectos sanitarios, 13% comerciales y 9% de información. De esta clasificación se podría decir que las Leyes, Decretos y Acuerdos se han dedicado a establecer normas de funcionamiento y organización del sector, las Resoluciones se han concentrado en aspectos de calidad y las Circulares van enfocadas a aspectos comerciales.
3.1. Calidad
El país cuenta con el Consejo Nacional de Seguridad Social en Salud -CNSSS- creado por el artículo 171 de la Ley 100 de 1993 y encargado de definir el grupo de medicamentos esenciales en su presentación genérica. Este grupo de medicamentos es actualizado por el Comité Técnico de Medicamentos y Evaluación de Tecnología, organismo asesor del CNSSS (Acuerdo 51 de 1997, modificado mediante el acuerdo 232 de 2002), que sólo tiene injerencia en el mercado institucional, y se encarga de la actualización del POS en términos de actividades, intervenciones, procedimientos y medicamentos. Inicialmente el listado de medicamentos genéricos y esenciales, contó con 393 principios activos distribuidos en 23 grupos terapéuticos, dicho listado ha sido modificado mediante los acuerdos 236 de 1998, 263 y 282 en 2004, 336 en 2006, 368 de 2007. Para el 2007 el listado contaba con un total de 423 principios activos y no ha sido actualizado desde ese año.
Adicionalmente, el país cuenta con el Instituto Nacional de Vigilancia de Medicamentos y Alimentos (8) -INVIMA- cuyas funciones están reglamentadas por el Decreto 1290 de 1994, es el encargado de la ejecución de políticas en materia de vigilancia sanitaria y control de calidad de productos (9) y se aplican a medicamentos comercializados distribuidos tanto en el mercado institucional como en el privado. Actualmente en Colombia hay un total 353 establecimientos certificados con Buenas Prácticas Manufactureras (Invima, 2009), estos están dedicados a la producción, comercialización, maquila y outsourcing de productos farmacéuticos, es decir empresas integradas verticalmente; de éstos el 38.24% son nacionales y el 61.75% filiales multinacionales, además se tienen 36 establecimientos con registros suspendidos 13.88% extranjeros y 86.11% nacionales.
3.2. Acceso
Con la formulación de la Ley 100 de 1993 se planteó como meta la afiliación de todos los colombianos al SGSSS en año 2000, meta que no fue alcanzada y, por tanto, ha sido el punto central en el debate, siendo nuevamente formulada en la Ley 1122 de 2007 y en el Plan de Desarrollo y el Plan Colombia 2019. En cuanto a la cobertura del SGSSS como datos más actuales se tienen las cifras al 2007 que muestran una cobertura total del 87.95% de la población donde 49.19% corresponde a población afiliada en el régimen subsidiado y 38.72% en el régimen contributivo. De esta población que tiene derecho por Ley al acceso al grupo de medicamentos genéricos y esenciales, según la encuesta de calidad de vida realizada por el Departamento Administrativo Nacional de Estadística de Colombia -DANE-, en 2003 se revela que pese a tener Seguridad social el 25.6% de los medicamentos requeridos por afiliados al régimen contributivo no le fue entregado, mientras que en el subsidiado esta cifra correspondió al 32.4%. Estos datos evidencian algunos problemas importantes. Primero, son cada vez más los afiliados al régimen subsidiado y la canasta de medicamentos a los que se tienen derecho es menor. Segundo, los afiliados al SGSSS deben, en muchos casos, recurrir al mercado privado y pagar de su bolsillo por los medicamentos a los que tienen derecho y tercero, el canal institucional carece de moléculas sustitutas dentro del listado de medicamentos lo que facilitaría la concentración de mercado para productores.
De otra parte, debido a que un porcentaje significativo de la población recurre al mercado privado para obtener medicamentos ya sean genéricos o de marca es importante examinar la regulación de precios. Como hecho importante se destaca que hasta finales de 2006 predominó la Ley 81 que estableció el control de precios bajo tres esquemas. i) Control Directo: mediante resolución sobre precio máximo; ii). Libertad Regulada: mediante criterios y metodología para que los productores y distribuidores determinen o modifiquen los precios máximos; y iii). Libertad Vigilada: cuando los productores y distribuidores determinan libremente los precios, bajo la obligación de informar en forma escrita sobre las variaciones y determinaciones de sus precios, de acuerdo con la metodología que la entidad determine.
En el 2006 con la circular 004 del mes de septiembre, la Comisión de Regulación de Precios planteo un nuevo modelo de regulación que buscaba proteger a los consumidores y controlar posibles abusos de posición dominante por parte de productores, importadores y expendedores de medicamentos. En consecuencia, se determinó el control de precios bajo los tres esquemas antes mencionados, pero la clasificación de los mismos se hace bajo metodologías diferentes. En este sentido, se determinó que todos los medicamentos comercializados en el país se incluirían al régimen de libertad vigilada con excepción de aquellos que ingresen al sistema de control directo o libertad regulada, para los cuales se dispone lo siguiente: el establecimiento del techo para los precios de medicamentos bajo control directo se realizará tomando los precios de medicamentos iguales, en términos de: moléculas, concentración, presentación y forma farmacéutica, y comparando los precios en nueve países de referencia: Argentina, Brasil, Chile, Colombia, Ecuador, México, Panamá, Perú y Venezuela. Además se establece que para determinar el grado de concentración en la oferta de productos en las clasificaciones terapéuticas relevantes se utilizará el índice Herfindahl-Hirschman. Finalmente, bajo el régimen de libertad regulada estarán todos los medicamentos autorizados por el INVIMA para venta bajo la condición de fórmula facultativa.
Dichas estrategias parecen no haber tenido el impacto esperado ya que, de una parte, la variación del IPC medicamentos en los últimos cuatro años ha oscilado entre el 18% y 11%, encontrándose siempre por encima de la variación del IPC salud; lo que quiere decir que el incremento en los precios del subgrupo de gasto en medicamentos fue mayor al crecimiento promedio de los precios de todos los subgrupos contenidos en el IPC salud (cálculos propios información tomada del Departamento Administrativo Nacional de Estadística -DANE-, 2008). En consecuencia, el sector salud podría clasificarse como un sector altamente inflacionario constituyéndose en una barrera significativa para el acceso a medicamentos y además, puede ser el resultado de altos niveles de concentración (Caves, 1991).
Así, para mirar el posible impacto de la política de precios en la eliminación de posición dominante se construyó el indicador de concentración en ventas según el índice de Herfindahl-Hirschman para un total de 224 tipos de medicamentos contenidos en 13 grupos terapéuticos, 65 componentes activos, de los cuales el 84% tiene libertad regulada, el 12% tiene control directo y el restante (4%) aún sin información sobre el tipo de regulación que les compete. Los datos para este conjunto de medicamentos se obtuvieron del IMS Colombia tomando los precios de venta, las cantidades vendidas, la presentación en la que se encuentra, el número de laboratorios que los inserta en el mercado y el número de laboratorios que los distribuye con información completa entre 1993 y 2007 y con registro INVIMA vigente al 2007. Es importante resaltar que el análisis se realizó desagregando cada grupo hasta el quinto nivel de clasificación como lo sugiere el código ATC y se contó únicamente con información en ventas del mercado privado, pero luego el total de los medicamentos comercializados allí se distribuyen por el canal institucional o el privado. Los resultados del análisis se muestran en la Tabla II.
Tabla II. Concentración del mercado 1993-2007
| Grupos Terapéuticos | Número de principios | Número de presentaciones | Promedio de laboratorios de laboratorios | Concentración de mercado | USD precios promedio |
| Antigotosos y uricosuricos | 1 | 1 | 2 | Alta | 0,52 |
| Antihistamínicos | 2 | 3 | 9 | Alta y Media | 0,74 |
| Antiinfecciosos | 28 | 49 | 11 | Alta y Media | 2,07 |
| Antiinflamatorios no asteroides y antirreumáticos | 4 | 7 | 8 | Alta y Media | 0,78 |
| Cardiovascular y renal | 8 | 14 | 12 | Alta, Media y Baja | 0,63 |
| Gastrointestinal y Metabolismo | 6 | 7 | 9 | Alta y Media | 0,90 |
| Hormonas y reguladores hormonales | 3 | 3 | 3 | Alta y Media | 0,77 |
| Piel y mucosas | 3 | 6 | 8 | Alta y Media | 0,23 |
| Respiratorio | 5 | 8 | 8 | Alta y Media | 0,37 |
| Sistema nervioso central y periférico | 5 | 7 | 9 | Alta y Media | 0,49 |
Fuente: IMS (1993-2007) Cálculo de los autores. Dólares según la TRM de cada año.
Como datos importantes se destaca que independientemente del número de laboratorios productores la concentración oscila entre media y alta por lo que la política prevaleciente hasta el 2003 carecía de sentido al especificar que de haber más de tres productores se estaría en mercados bajo competencia. Ahora, según el índice de concentración estudiado todos los medicamentos deberían estar bajo el régimen de control directo porque el índice de concentración muestra posición dominante para cada año.
3.3. Contención de costos
Partiendo del ciclo de vida de un producto farmacéutico podría decirse que este inicia con el descubrimiento de nuevos medicamentos (pioneros), donde las firmas encaran altos gastos en I&D pero no perciben ingresos hasta que obtienen la patente. Con la producción o manufactura pioneros e imitadores obtienen unos niveles altos de cantidades vendidas y de precios; esto en mayor proporción para los primeros, debido a los recursos invertidos al inicio del proceso. Consecuentemente, los retornos crecerán a una tasa decreciente, así, en un período previo a la expiración de la patente el volumen de ventas, los precios y los ingresos ganados en los primeros años comienzan a caer, y lo hacen en mayor proporción debido a la competencia con la entrada de genéricos; finalmente, los productos de marca salen del mercado cuando se traslada la demanda a los genéricos (Bauer et al., 2000).
En este sentido y de acuerdo con la normatividad vigente la prescripción de medicamentos genéricos y esenciales a la población colombiana afiliada a la seguridad social buscaba que la producción y comercialización de genéricos generara precios bajos y altas cantidades disponibles para el consumo y que además promoviera y fortaleciera la industria nacional. Así, para el año 2006 el país contó con un crecimiento positivo de la industria jalonada por la producción nacional de genéricos, los cuales según cifras del IMS Colombia, ocupan alrededor del 70,1% del mercado en unidades y el 42,4% en valores, lo que garantizaría acceso y contención de costos en términos de precios.
Finalmente y aunque el mercado farmacéutico colombiano es el quinto más grande en la región, por debajo de México, Brasil, Argentina y Venezuela, la industria nacional está dominada por multinacionales y cuenta con una Balanza Comercial Relativa -BCR- (10) que ha mostrado desventaja competitiva desde 1974 hasta el 2008 y cuyo valor ha oscilando entre el -71.04 y -30.87 siendo mayor en cantidad y valor de importaciones al compararse con las exportaciones, debido en parte al hecho de que la industria nacional depende en gran medida de las importaciones de materias primas (cálculos propios información tomada del Departamento Nacional de Planeación, 2008).
4. Consideraciones finales
Como aspectos relevantes se destaca el esfuerzo por crear un sistema de salud con un paquete de medicamentos adscritos a los que los colombianos tendrían acceso en términos de disponibilidad y precios, y que además eliminaba los incentivos monetarios que comúnmente tienen quienes prescriben, por lo que se excluían posiciones dominantes por fidelidad a las marcas o sensibilidad de la demanda. Sin embargo, luego de quince años de la implementación de la Ley, la normatividad vigente sigue concentrándose en el establecimiento de legislación que permita el buen funcionamiento del sector en términos de organización, dejando de lado aspectos como el acceso, la concentración del mercado, el gasto de bolsillo y una efectiva política de control de precios que permita el pleno abastecimiento de medicamentos a los afiliados al SGSSS por el canal institucional.
De otro lado, es preocupante la ausencia de regulación desde agosto de 2008 y la no aplicación del control de precios basados en el índice de concentración del mercado propuesta en el año 2006, política que solo tendrá el impacto esperado si se definen bien las condiciones de mercado de los canales de distribución en cuanto a posibilidades de sustitución, distribución, diferenciación vertical y horizontal, concentración y tamaño (Sutton, 1991) y (Danzon et al., 2008). Dichos aspectos, cobran vital importancia cuando la afiliación al régimen subsidiado sobrepasa a la población con capacidad de pago afiliada y pone de manifiesta la fragilidad financiera del sistema.
Además, debido que las cuotas moderadoras en muchos casos superan el costo de los medicamentos, incluso de marca en el mercado privado y la escasez de medicamentos por efectos de relaciones de agencia en el mercado institucional generan un alto gasto de bolsillo para adquirir los mismos, podría considerarse la aplicación de regulación de precios vía precios de referencia como lo muestra Miraldo (2007).
Notas
1. El artículo es derivado de la investigación Estructura del mercado de medicamentos para uso ambulatorio en Colombia 1993-2002. financiada el Comité para el Desarrollo de la Investigación -CODI- de la Universidad de Antioquia. Entre febrero de 2004 y junio de 2005. Los investigadores contaron con el apoyo de las asistentes de investigación Karem V Espinosa Echavarría, Lina P Casas Bustamante y Diana M Ardila Londoño. Las cifras fueron actualizadas al año 2009 por iniciativa de las autoras. Las ideas, opiniones y posibles errores aquí expresados sólo comprometen a los autores.
2. Según Sosa (2002) aproximadamente 20 grandes empresas controlan más de la mitad del mercado internacional, al dominar casi la totalidad de la producción, investigación y comercialización de los fármacos en el mundo.
3. La definición fue tomada The Canadian Encyclopedia Dirección URL http://www.thecanadianencyclopedia.com/index.cfm?PgNm=TCE&Params=A1ARTA000251. Consultada el día 11 de mayo de 2009.
4. Estos son definidos en Colombia, por la Comisión Técnica Asesora de Medicamentos bajo criterios de de eficacia, seguridad y balance beneficio/riesgo/costo.
5. Esto debido a que la protección de patentes comenzó a regir a partir de 1993.
6. Creada mediante el Articulo 2° de Circular 004 de septiembre de 2006.
7. A las esferas teóricas se agregó la correspondiente a aspectos de organización del sector debido a su importancia dentro de la normatividad colombiana.
8. Creado mediante el artículo 245 de la Ley 100 de 1993.
9. Los productos vigilados en cuanto a calidad son los referidos en el artículo 245 de la Ley 100 de 1993y son los siguientes: medicamentos, productos biológicos, alimentos, bebidas, cosméticos, dispositivos y elementos médico quirúrgicos, odontológicos, productos naturales, homeopáticos y los generados por biotecnología, reactivo de diagnóstico, productos de aseo, higiene y limpieza, los plaguicidas de uso doméstico.
10. Fabricación de productos farmacéuticos y medicamentos según la clasificación Ciiu rev.2.Departamento Nacional de Planeación -DNP-. BCR=(exportaciones-importaciones)/ (importaciones + Exportaciones) valores cercanos a (1) muestran ventajas competitivas y los cercanos a ( -1) desventajas.
Bibliografía citada
1. Archila, Emilio; Meléndez, Marcela (2005). Estudio sobre la propiedad Intelectual en el sector farmacéutico colombiano. Fundación para la Educación Superior y el Desarrollo -Fedesarrollo-. Documento de trabajo 01. [ Links ]
2. Bauer, Hans y Fischer, Marc (2000). Product life cycle patterns for pharmaceuticals and their impact on R&D profitability of late mover products. International Business Review, Volume 9, Issue 6. Pp. 703-725. [ Links ]
3. Bisang, Roberto y Maceira, Daniel (1999). Medicamentos: apuntes para una propuesta de política integral. Universidad Nacional de General Sarmiento, Laboratorio de Investigaciones sobre Tecnología, Trabajo, Empresas y Competitividad (LITTEC), Documentos de Trabajo, 37, Pp 480. [ Links ]
4. Danzon, Patricia y Cho, Li-Wei (2000). Does regulation drive out competition in pharmaceutical markets?. Journal of Law & Economics, Vol. XLIII. [ Links ]
5. Danzon, Patricia M. y Epstein Andrew J. (2008). "Effects of Regulation on Drug Launch and Pricing in Interdependent Markets," NBER Working Papers 14041, National Bureau of Economic Research. [ Links ]
6. Caves, Richard E., Whinston, Michael D. y Hurwitz, M Mark A. (1991). Patent expiration, entry and competition in the U.S. pharmaceutical industry, Brookings Papers Econom. Activity, Microeconomics, pp. 1-66. [ Links ]
7. Instituto Español de Comercio Exterior ICEX (2005). El sector de productos farmacéuticos para uso humano en Colombia. Oficina Económica y Comercial de la Embajada de España en Bogotá. [ Links ]
8. Instituto Nacional de Vigilancia de Medicamentos y Alimentos -Invima- (2009). Servicio de consultas públicas http://web.invima.gov.co/Invima/consultas/index.jsp?codigo=41. Consultado el 4 de mayo de 2009. [ Links ]
9. Jacobzone, S. (2000). Pharmaceutical Policies in OECD Countries: Reconciling Social and Industrial Goals, OECD Labour Market and Social Policy Occasional Papers, No. 40, OECD Publishing. [ Links ]
10. Jiménez, Ismárlen y Hurtado, Alvaro (2005). La concentración de mercado en el sector farmacéutico colombiano 2002-2003. Un análisis parcial para las enfermedades cerebrovasculares e isquemias, diabetes mellitas y morbimortalidad cardiovascular, ecos de economía, No.21, Pp.173-202. [ Links ]
11. Miraldo, Marisa (2007). Reference Pricing Versus Co-Payment in the Pharmaceutical Industry: Price, Quality and Market Coverage. Centre for Health Economics University of York, Research Paper, No.25. http://www.york.ac.uk/inst/che/pdf/rp25.pdf (Mayo 14 de 2009). [ Links ]
12. Mojica, Ana y Villamil, Jesús (2002). Sistema de patentes en la industria farmacéutica colombiana. Http://www.kfpe.ch/download/columbia/Ana_Maria_Mojica_esp.pdf (Mayo 14 de 2009) . [ Links ]
13. Mushkin, Selma (1958). Toward a Definition of Health Economics Public Health Reports. Vol. 73, No. 9. Pp. 785-794. [ Links ]
14. Organización Mundial de la Salud (2002). Effective drug regulation A multicountry study, http://apps.who.int/medicinedocs/collect/medicinedocs/pdf/s2300e/s2300e.pdf. [ Links ]
15. Rossi, Francisco. (2003). El por qué de una política de medicamentos. Periódico el Pulso. Año 5 No 57. Junio. Disponible en: http://www.periodicoelpulso.com/html/jun03/debate/debate-04.htm (Abril 14 de 2009). [ Links ]
16. Rossi, Francisco (2009). Ifarma: Lucha contra genéricos atenta contra salud pública y estabilidad del sistema. Periódico el Pulso. Año 10 No 125. Febrero. Disponible en: http://www.periodicoelpulso.com.co/html/0902feb/debate/debate-02.htm (Abril 14 de 2009). [ Links ]
17. Santerre, Rexford, y Stephen, Neun (2000a). The Demand for Medical Services, capítulo 4. Health Economies: Theory, Insights and Industry Studies. [ Links ]
18. Santerre, Rexford, y Stephen, Neun (2000b). The Pharmaceutical Industry, capítulo 16. Health Economies: Theory, Insights and Industry Studies. [ Links ]
19. Sosa, Mario Roberto (2002). Análisis sectorial: La industria farmacéutica. Centro de estudios para la producción. Ministerio de la producción. República de Argentina 2002. [ Links ]
20. Stiglitz, Joseph (2002). La Economía del Sector Público, Antoni Bosch Editor. Tercera Edición. [ Links ]
21. Sutton, J. (1991). Sunk cost & market structure: price competition, advertising and the evolution of concentration. Mit press, London. [ Links ]
22. Vincenzo, Atella, Bhattacharya, Jay y Carbonari, Lorenzo (2008). Pharmaceutical Industry, Drug Quality and Regulation: Evidence from US and Italy. Research Paper Series, Vol. 6, Issue 11, No. 138. November. [ Links ]