Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Bioagro
versión impresa ISSN 1316-3361
Bioagro v.24 n.1 Barquisimeto abr. 2012
Efecto de la contaminación por hidrocarburos sobre algunas propiedades químicas y microbiológicas de un suelo de sabana
Alejandra Zamora1, Jesús Ramos1 y Marianela Arias2
1 Instituto de Zoología y Ecología Tropical, Facultad de Ciencias, Universidad Central de Venezuela. Apdo. 47114. Caracas. Venezuela e-mail: alejandra.zamora@gmail.com
2 Gerencia de Ambiente e Higiene Ocupacional, PDVSA-Intevep. Apdo. 47058. Caracas. Venezuela
Resumen
El derrame de hidrocarburos de petróleo al suelo tiene impactos importantes en la actividad de los microorganismos, y afecta la funcionalidad del ecosistema. El objetivo del estudio fue evaluar los cambios químicos y en la comunidad microbiana de un suelo contaminado con crudo mediano, y determinar la capacidad de restitución de la estructura funcional de las comunidades bacterianas luego de un período de incubación en condiciones de laboratorio. Se estableció un grupo de microcosmos control (suelo sin contaminar) y otro con suelo contaminado con crudo mediano al 9 % p/p, y se incubaron durante 120 días. Se determinaron características químicas del suelo y la caracterización bioquímica de cepas bacterianas al inicio y al final del experimento. Se encontró que la contaminación con hidrocarburos ocasionó un aumento de la saturación con aluminio y disminución del pH, conductividad eléctrica y capacidad de intercambio catiónico del suelo, modificación de la comunidad bacteriana y reducción de su diversidad por selectividad de grupos funcionales. Se concluye que la contaminación con hidrocarburos afecta la estructura funcional de la comunidad, pero aunque ésta no se restituye a su condición original, el funcionamiento del ecosistema no es afectado a largo plazo, ya que los procesos continúan ocurriendo.
Palabras clave adicionales: Comunidades bacterianas, diversidad funcional, grupos funcionales
Effect of oil pollution on chemical and microbiological properties of a savanna soil
Abstract
The spill of petroleum hydrocarbons to soil has significant impacts on microbial activity, affecting ecosystem function. The aim of this study was to evaluate the chemical and microbial changes in a soil contaminated with medium petroleum, and determine the restoration capacity of the functional structure of bacterial communities after an incubation period under laboratory conditions. For this purpose, two microcosms were established and incubated for 120 days: a) control, with uncontaminated soil, and b) oil-contaminated soil to 9 % w/w. Soil chemical characteristics and biochemical characterization of strains were performed at the beginning and end of the experiment. The results indicate that oil pollution increased aluminum saturation and decreased pH, electrical conductivity and cation exchange capacity of the soil, and altered the bacterial community, reducing its functional diversity by selectivity of functional groups. It is concluded that oil pollution affects the functional structure of the community, and although it is not returned to its original condition, the functioning of the ecosystem is not affected in the long term, since the processes keep occurring.
Additional keywords: Bacterial communities, functional diversity, functional groups
Recibido: Septiembre 23, 2010 Aceptado: Julio 29, 2011
INTRODUCCIÓN
Los derrames de hidrocarburos de petróleo son una de las principales fuentes de contaminación de suelos y aguas ya que ocasionan perturbaciones en los ecosistemas al afectar su estructura y bioprocesos. Este tipo de contingencias ambientales originan efectos directos sobre la biota, ya que el petróleo contiene compuestos químicos tóxicos que producen daños a plantas, animales y humanos pero principalmente sobre las poblaciones de microorganismos, los cuales representan parte importante del ecosistema y son claves para los procesos biogeoquímicos (Vasudevan y Rajaram, 2001).
La estructura funcional de las comunidades microbianas ha sido ampliamente utilizada como indicador biológico, debido a la sensibilidad a los cambios y a su capacidad de proveer información que integre diversos factores ambientales (Alkorta et al., 2003). De esta manera, la identificación de grupos funcionales en un determinado ecosistema permite hacer una evaluación precisa de sus propiedades, tales como capacidad de recuperación y regeneración, resistencia a cambios ambientales y potencial degradativo.
De acuerdo con el análisis funcional, cada cepa individual que difiere de las demás representa un grupo funcional (GF) distinto dentro de la comunidad. Esta metodología aborda inicialmente la delimitación y cuantificación de GF utilizando la técnica multivariada de agrupamiento (clúster). Este procedimiento permite obtener gráficamente mediante un dendrograma las coincidencias en cuanto a la ausencia o presencia de utilización de sustratos de cada cepa, y por tanto, provee una estimación de la similitud total entre las cepas que conforman los grupos. A partir de esta información se puede calcular entonces el índice de diversidad funcional (IDF) donde el valor de 1 representa el máximo de diversidad. También se utiliza como criterio de comparación la distancia máxima de agrupamiento (DMA) que separa los grupos funcionales, y representa la mayor disimilitud o mayor diversidad funcional (Zamora, 2006).
La presente investigación se orientó a evaluar los cambios en algunos parámetros químicos de un suelo de sabana y su efecto en la estructura funcional de la comunidad bacteriana debido a la contaminación con un crudo mediano.
MATERIALES Y MÉTODOS
Se prepararon microcosmos experimentales utilizando un suelo de sabana franco arenoso (87,9 % arena y 5,4 % arcilla), de baja fertilidad y ligeramente ácido, proveniente de Santa Bárbara, estado Monagas, Venezuela. Se establecieron dos tratamientos, un suelo sin contaminar o control (SC) y un suelo contaminado con hidrocarburo de petróleo (HCP) al 9 % en peso (C). El HCP consistió en un crudo mediano de 24,3 ºAPI (36,2 % saturados, 40,31 % aromáticos, 19,35 % resinas, 4,14 % asfaltenos). Cada tratamiento contó con tres réplicas que consistieron en bandejas con 4 kg de suelo cada una. El suelo fue disturbado periódicamente utilizando un rastrillo de jardinería para facilitar su aireación y sometido a riego controlado una vez a la semana durante 120 días. La temperatura promedio del invernadero fue de 27 °C. Las muestras para los análisis químicos y microbiológicos se tomaron luego de 24 h de aplicado el crudo para determinar los cambios al inicio de la contaminación y luego de 120 días para evaluar el comportamiento del sistema en el tiempo. Las muestras para análisis microbiológico se procesaron inmediatamente y las destinadas a análisis químico se guardaron en refrigeración (4 °C) hasta su procesamiento.
Para cada microcosmo se determinó el pH (EPA, 1980), conductividad eléctrica (CE) (APHA, 1992), capacidad de intercambio catiónico (CIC) (Adams, 1995), porcentaje de saturación de aluminio (% Al) (Adams, 1995) y porcentaje de aceites y grasas (% A y G) (EPA, 1994).
La densidad de bacterias se determinó mediante el conteo en placas PCA de unidades formadoras de colonias. Se mezclaron 5 g de suelo y 95 mL de una solución 0,85 % de NaCl, se agitó durante 8 horas y posteriormente se tomó una alícuota de 1 ml para realizar diluciones seriadas y siembra en placas de Petri. Se aisló un pool de bacterias de cada réplica por tratamiento y luego se seleccionaron al azar (mediante una tabla de números aleatorios) veinte cepas bacterianas por cada tratamiento y se cultivaron en placas PCA para su purificación y crecimiento.
Cada cepa se caracterizó morfológicamente a través de la tinción Gram y observación al microscopio de la forma y composición de la pared celular. La caracterización funcional de las comunidades bacterianas del control y del suelo contaminado se realizó a través del potencial bioquímico de cada cepa aislada. Se realizaron un total de 23 pruebas bioquímicas que incluyeron diversos carbohidratos, aminoácidos, sustratos orgánicos y producción de enzimas (Cuadro 1). Las pruebas bioquímicas de las cepas se realizaron utilizando el sistema API 20NE (Biomereux, St Louis, MO). Las pruebas de degradación de celulosa, lignina y lípidos se realizaron determinando el crecimiento de las cepas en agar cuya única fuente de carbono eran cada uno de estos polímeros (medio mínimo mineral 50 %, agua 50 %, agar 1,5 % y celulosa, lignina o tween 80 al 1 %). La utilización de cada sustrato se expresó como frecuencia de utilización (número de respuestas positivas) respecto al total de cepas aisladas en cada tratamiento.
Cuadro 1. Sustratos utilizados para determinar el perfil bioquímico de las cepas bacterianas aisladas
| Carbohidratos | Aminoácidos | Sustratos orgánicos | Pruebas enzimáticas |
| Glucosa oxidativa [GLU(OX)] y fermentativa [GLU(FER)] | Arginina (ADH) | Manitol (MNE) | Ureasa (URE) |
| Arabinosa (ARA) | Triptofano (TRP) | N-acetil-glucosamina (NAG) | Proteasas (GEL) |
| Manosa (MAN) |
| Gluconato (GNT) | Nitrato reductasas (NO2; N2) |
| Maltosa (MAL) |
| Caprato (CAP) | β-glucosidasa (β -glu) |
| Celulosa (CEL) |
| Adipato (ADI) | β-galactosidasa (β-gal) |
| Lignina (LIG) |
| Malato (MLT) |
|
|
|
| Citrato (CIT) |
|
|
|
| Fenil-acetato (PAC) |
|
|
|
| Tween 80 (TWN) |
|
Con base a los perfiles bioquímicos se realizó el análisis funcional de las comunidades bacterianas. Los resultados de ausencia o presencia de utilización de cada cepa aislada se utilizaron para realizar un análisis de agrupamiento en el cual cada amalgamiento representó un grupo funcional (GF) y se determinó el índice de diversidad funcional como el cociente entre el número de GF formados y el total de aislados.
Se efectuaron pruebas de t en las variables químicas entre el suelo control y el contaminado, y entre el inicio y final del experimento, y se realizó un análisis multivariado de agrupamiento para delimitar los grupos funcionales con base al perfil bioquímico de las cepas.
RESULTADOS Y DISCUSIÓN
Efecto de los HCP sobre las propiedades químicas del suelo
Se evidenció que el pH del suelo disminuyó en presencia del crudo (Cuadro 2), posiblemente debido a la disminución en la concentración de cationes intercambiables (Amadi et al., 1993; Osuji et al., 2005). La disminución del pH en suelos contaminados con HCP también ha sido reportada por Caravaca y Roldán (2003). Okolo et al. (2005) y Osuji y Opiah (2007) atribuyen este efecto a limitación de Ca y Mg, mientras que Britton (1984) señala que puede ser producto de la liberación de ácidos grasos y compuestos de cadena larga durante la biodegradación.
Cuadro 2. Propiedades químicas y densidad bacteriana del suelo como respuesta a la contaminación con HCP
| Variables | Control | Contaminado | ||
| 1 día | 120 días | 1 día | 120 días | |
| pH | 6,36 Aa | 6,49 Aa | 5,41 Ba | 5,81 Ba |
| CE (mS·cm-1) | 212,17 Ab | 569,75 Aa | 292,12 Aa | 111,09 Bb |
| CIC (meq/100 g suelo) | 1,28 Ab | 1,89 Aa | 0,65 Ba | 0,8 Ba |
| Alint (%) | 0,87 Ba | 0,58 Ba | 1,76 Aa | 1,54 Aa |
| A y G (%) | ND | ND | 8,79 a | 6,83 b |
| Db (UFC/g suelo) | 7,57x107 Aa | 9,95x106 Bb | 1,51x108 Aa | 5,26x108 Aa |
Letras diferentes indican diferencias significativas Prueba T (P≤0,05, n=3). Letras mayúsculas para comparación entre tratamientos en una misma fecha y letras minúsculas para la comparación de un mismo tratamiento en diferentes fechas. CE: conductividad eléctrica. CIC: capacidad de intercambio catiónico. %Alint: aluminio intercambiable. %AyG: aceites y grasas. Db: densidad bacteriana. ND: no detectable
La CE aumentó significativamente con el tiempo en el microcosmos control (Cuadro 2), lo cual es atribuible, entre otros, a la actividad biológica durante la descomposición de materia orgánica y procesos redox. En el suelo contaminado se observó, al inicio del experimento, un aumento de la CE lo cual posiblemente se deba a que el HCP puede contener restos de compuestos salinos utilizados durante la extracción y purificación, pero luego disminuyó a los 120 días. Similar tendencia fue reportada por Martínez y López (2001) quienes señalan que esta variación en los valores de CE puede ser debida de un incremento en la actividad microbiana, y el uso de aceptores de electrones alternativos (como el nitrato o el azufre) lo cual aumenta el ambiente reductor en el suelo (Osuji y Opiah, 2007).
Por otra parte, hubo una reducción significativa de la CIC en el suelo contaminado (Cuadro 2), lo cual se relacionaría con la adsorción de los HCP en las partículas minerales del suelo. Martínez y López (2001) y Okolo et al. (2005) indican que la CIC disminuye debido a que los HCP interfieren en los sitios de intercambio de cationes (Karimi-Lotford et al., 1996) y en las interacciones electrostáticas (Pignatello y Xing, 1996). En el Cuadro 2 se observa que el porcentaje de saturación con aluminio incrementó en presencia del hidrocarburo, lo cual se asocia con la disminución de la capacidad de intercambio catiónico y pH (Adams, 1995). Se observa también que a los 120 días el porcentaje de aceites y grasas disminuyó significativamente, lo que sugiere que los microorganismos utilizaron el HCP como fuente de carbono y energía, es decir, durante la incubación se dio lugar a un proceso de biodegradación del contaminante, lo cual permitió la disminución de su concentración en casi 2 %.
Efecto de los HCP sobre la comunidad bacteriana del suelo
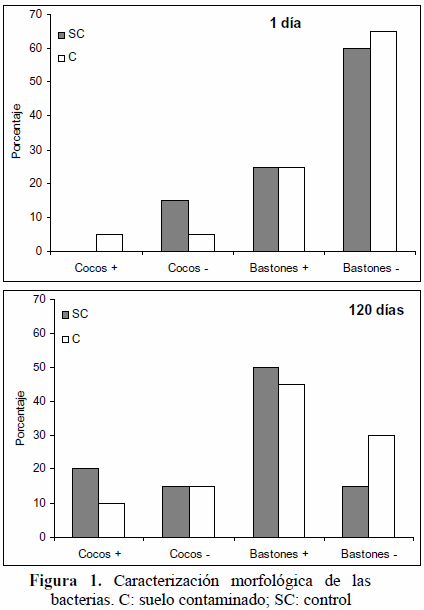
Hubo un aumento significativo en la densidad de bacterias en el suelo contaminado respecto al control (Cuadro 2), lo cual podría atribuirse a la incorporación de microorganismos provenientes del HCP y su proliferación debido a las nuevas condiciones del ambiente. Inicialmente, en ambas comunidades predominaron los bastones Gram negativos, mientras que al final del experimento predominaron los Gram positivos (Figura 1). Se observa que en el tratamiento control, luego de 120 días, se expresaron cocos Gram positivos, ausentes al inicio del experimento, y disminuyó la proporción de bastones Gram negativos. Similares cambios fueron reportados por Zelles et al. (1995) y Atlas y Bartha (2002). De hecho, Greene et al. (2000) y Kaufmann et al. (2004) señalan que después de la contaminación con HCP se produce un incremento de la comunidad microbiana, y un decrecimiento en la diversidad, quizá por selectividad de algunos organismos capaces de adaptarse y utilizar los nuevos sustratos, ya que los componentes tóxicos de los hidrocarburos podrían inhibir la expresión de algunos miembros de la comunidad bacteriana (Yerushalmi et al., 2003).
Análisis funcional de la comunidad bacteriana
La comunidad control (Figura 2) inicialmen se caracterizó por una alta proporción de cepas que degradan diversos sustratos orgánicos, ya que todas degradaron glucosa, manosa, celulosa, lignina, gluconato, N-acetil-glucosamina y tween. Se determinó alta proporción de cepas con actividad ureásica (70 %) y proteolítica (100 %). También se observa que hubo un 80 % de cepas denitrificantes (reducción completa de nitratos), y menos de la mitad de las cepas presentó actividad de β-glucosidasa y β-galactosidasa (25 y 30 %, respectivamente). Este perfil sugiere una alta diversidad funcional.
Luego de la adición del HCP la comunidad cambió. Se puede notar la ausencia de cepas capaces de degradar triptofano, pero se mantuvo alto el porcentaje de cepas que degradan glucosa, manosa, malato y citrato (100 %), celulosa y lignina (95 %). La actividad de la arginina dihidrolasa, de la β-glucosidasa y la β-galactosidasa fue mayor que en el control (90, 60 y 45 %, respectivamente; de igual modo el consumo de manitol (50 %), mientras que la actividad proteolítica (90 %), la reducción completa de nitratos (70 %), la actividad ureásica (35 %) y degradación de tween (85 %) fue menor que la comunidad control.
Al final del experimento, el perfil bioquímico de las comunidades del suelo control disminuyó en 15 % la fermentación de glucosa y en 20 % el uso de manosa, mientras que el uso de arabinosa y maltosa como fuente de carbono incrementó en 60 % (Figura 3). Se observa igualmente que la reducción completa de nitratos disminuyó considerablemente (de 80 a 5 %), siendo este proceso respiratorio sustituido por reducción de nitratos a nitritos, frecuencia que aumentó de 20 a 95 %. Se puede notar también que para esta comunidad la frecuencia de cepas con capacidad para degradar triptofano hasta indol disminuyó en 10 % en la comunidad final, tendencia observada también en la producción de arginina dihidrolasa (de 85 a 60 %); la actividad ureásica disminuyó un 55 %, la degradación de tween (de 100 a 65 %), la actividad proteolítica (de 100 a 90 %) y la utilización de celulosa y lignina como fuentes de carbono disminuyó un 30 %. Sin embargo, incrementó el número de cepas capaces de producir β-glucosidasa y β-galactosidasa (de 30 a 95 % y de 25 a 70 %, respectivamente).
La comunidad del suelo contaminado también varió en la proporción de cepas que utilizan arabinosa (de 45 a 70 %) y maltosa (de 70 a 100 %) como fuente de carbono, mientras que la actividad de arginina dihidrolasa y n-acetil-glucosaminidasa se mantuvo igual que al inicio del experimento (90 y 95 %), así como la frecuencia de cepas que degradan tween (80 %), con actividad proteolítica (90 %) y actividad de la β-galactosidasa (45 %). El número de cepas que consumen fenil-acetato aumentó al final de la incubación (de 45 a 95 %), así como la actividad de la β-glucosidasa (de 60 a 85 %) y la reducción de nitratos a nitritos como proceso de respiración bacteriana (de 30 a 95 %).
En el tratamiento control al inicio del experimento se observó la formación de 12 GF, entre los cuales se encuentran cuatro grupos de identidad funcional (GIF I hasta GIF IV) (Figura 4), correspondientes a grupos de cepas diferentes con características funcionales idénticas (disimilitud igual a cero), e indican redundancia funcional dentro de la comunidad. El IDF para esta comunidad fue de 0,6 (12 GF respecto a un total de 20 cepas aisladas) y la distancia máxima de agrupamiento (DMA) de los grupos funcionales de 2,83.
Los resultados del análisis funcional de la comunidad bacteriana para el tratamiento control y contaminado al inicio y luego de 120 días de incubación se resumen en el Cuadro 3. Las tendencias indican que en la comunidad control se formó un mayor número de GF, y aumentó en consecuencia su diversidad funcional, mientras que en el suelo contaminado hubo menor número de GF, lo cual indica menor diversidad funcional.
Cuadro 3. Distribución de grupos funcionales y diversidad funcional de cada suelo
| Parámetro | Control | Contaminado | ||
| 1 día | 120 días | 1 día | 120 días | |
| GF | 12 | 20 | 18 | 16 |
| IDF | 0,6 | 1 | 0,9 | 0,8 |
| DMA | 2,83 | 2,45 | 2,24 | 1,73 |
GF: número de grupos funcionales. IDF: índice de diversidad funcional. DMA: distancia máxima de agrupamiento
El suelo control presentó la máxima diversidad luego de 120 días de incubación, mientras que en el contaminado la diversidad funcional aumentó con la adición de HCP, y luego de 120 días la diversidad tendió a disminuir (Cuadro 3). También se observa que la disimilitud entre los grupos o distancia máxima de agrupamiento fue mayor en el suelo control que en el contaminado, lo que indica que los grupos fueron más diferentes y funcionalmente más diversos en el primero de ellos (aunque el índice de diversidad resultó bajo).
Al relacionar los resultados de diversidad funcional, densidad bacteriana y los perfiles metabólicos de las comunidades se puede inferir que hubo un cambio en la estructura de la comunidad y que luego de la contaminación predominaron aquellas cepas heterotróficas con capacidad de utilizar los HCP como fuente de carbono sobre aquellas que no presentan esta adaptación. En tal sentido, la Figura 2 muestra que la contaminación con HCP indujo un incremento en la actividad microbiana respecto a la comunidad control, lo cual se evidencia en la actividad de la NAG y β-glucosidasa, enzimas utilizadas como indicadoras de actividad microbiana en suelos.
Se observó que la estructura de la comunidad control cambió en el tiempo, lo que también ha sido reportado por Brockman et al. (1998) y Bundy et al. (2002) quienes indican que en condiciones de laboratorio existe un efecto significativo en la actividad y composición de las comunidades microbianas en controles sin contaminación como resultado del proceso de incubación.
En general, la diversidad funcional fue más baja en el suelo contaminado que en el control tal como lo reportan Nyman (1999), Röling et al. (2002) y Kaufmann et al. (2004). En este respecto, Röling et al. (2002) indican que los HCP pueden inducir profagia, es decir, expresión de actividad lisogénica en algunas bacterias resultando en lisis de una gran proporción de estos microorganismos, lo cual puede explicar los cambios en la composición de la comunidad independientemente de la extensión de la biodegradación.
El análisis funcional muestra que, bajo las condiciones de este estudio, no ocurrió el total restablecimiento de la comunidad original luego de la perturbación, sino que con el tiempo la comunidad se vuelve diferente a la comunidad control tanto morfológica como fisiológicamente. Esto sugiere que los cambios que ocurren en su estructura probablemente se deban a la adaptación de los organismos al estrés nutricional y como consecuencia la competencia por recursos, así como presión selectiva en el medio, confirmando así los principios ecológicos de los procesos de biodegradación (Röling et al., 2002).
CONCLUSIONES
La contaminación con HCP induce cambios en las propiedades químicas del suelo, disminuyendo el pH, la conductividad eléctrica y la capacidad de intercambio catiónico, lo cual incrementa el porcentaje de saturación con aluminio. Estos cambios hacen menos diversa la estructura funcional de la comunidad bacteriana. También, ocurre una restricción de la diversidad funcional.
A pesar de ello, el suelo afectado tuvo capacidad de afrontar adecuadamente los factores estresantes, ya que los procesos siguieron ocurriendo, de lo que se infiere que el nivel de resiliencia fue alto y que el funcionamiento del ecosistema no fue afectado a largo plazo, aun cuando la estructura comunitaria no se restituyó por completo a su condición original.
AGRADECIMIENTO
Al personal del Laboratorio de Tratabilidad de Desechos Sólidos de Intevep por su colaboración en los análisis de laboratorio. Al Dr. Ismael Hernández del IZET-UCV por sus valiosos comentarios y sugerencias en la elaboración de este manuscrito.
LITERATURA CITADA
1. Adams, M. 1995. Fundamentos de Química de Suelos. Colección Estudios Consejo de Desarrollo Científico y Humanístico. Universidad Central de Venezuela. Caracas. 390 p. [ Links ]
2. Alkorta, I., A. Aizpurua, P. Riga, I. Albizu, I. Amezaga y C. Garbisu. 2003. Soil enzyme activities as biological indicators of soil health. Review Environmental Health 18: 65-73. [ Links ]
3. Amadi, A., A. Dickson y G. Maate. 1993. Remediation of oil polluted soils: Effect of organic and inorganic nutrient supplements on the performance of maize (Zea mays L.). Water, Air, and Soil Pollution 66: 59-76. [ Links ]
4. APHA (American Public Health Association). 1992. Standard Methods for the Examination of Water and Wastewater. Method 2520A. Washington D.C. [ Links ]
5. Atlas, R. y R. Bartha. 2002. Ecología Microbiana y Microbiología Ambiental. Edit. Addison Wesley. Madrid. [ Links ]
6. Britton, L. 1984. Microbial degradation of aliphatic hydrocarbons. In: D. Gibson (ed.) Microbial Degradation of Organic Compounds. Microbiology Series. Vol. 13. Marcel Dekker. New York. pp. 89-129. [ Links ]
7. Brockman, F.J., S.W. Li, J.K. Fredrickson, D.B. Ringelberg, T.L. Kieft, C.M. Spadoni, D.C. White y J.P. McKinley. 1998. Post-sampling changes in microbial community composition and activity in a subsurface paleosol. Microbial Ecology 36: 152-164. [ Links ]
8. Bundy, J.G., G.I. Paton y C.D. Campbell. 2002. Microbial Communities in different soil types do not converge after diesel contamination. Journal Applied Microbiology 92: 276-288. [ Links ]
9. Caravaca, F. y A. Roldán. 2003. Assessing changes in physical and biological properties in a soil contaminated by oil sludges under semiarid Mediterranean conditions. Geoderma 117: 53-61. [ Links ]
10. EPA (Environmental Protection Agency). 1980 y 1994. Test Methods for evaluating solid wastes physical/chemical methods. Method 9045C y 3540B. [ Links ]
11. Greene, E.A., J.G. Kay, K. Jarber, L.G. Stehmeier y G. Voordouw. 2000. Composition of soil microbial communities enriched on a mixture of aromatic hydrocarbons. Applied Environmental Microbiology 66: 5282-5548. [ Links ]
12. Karimi-Lotford, S., M. Pickard y M. Gray. 1996. Reactions of polynuclear aromatic hydrocarbons in soil. Environmental Science Technology 30: 1145-1151. [ Links ]
13. Kaufmann, K., M. Christophersen, A. Buttler, H. Harms y P. Höhener. 2004. Microbial community response to petroleum hydrocarbon contamination in the unsaturated zone at the experimental field site Værløse, Denmark. FEMS Microbiology Ecology 48: 387-399. [ Links ]
14. Martínez, V. y F. López. 2001. Efecto de los hidrocarburos en las propiedades físicas y químicas de un suelo arcilloso. Terra 19: 9-17. [ Links ]
15. Nyman, J. 1999. Effect of crude oil and chemical additives on metabolic activity of mixed microbial populations in Fresh Marsh Soils. Microbial Ecology 22: 249-256. [ Links ]
16. Okolo, J.C, E.L. Amadi y C.T. Odu. 2005. Effects of soil treatments containing poultry manure on crude oil degradation in a sandy loam soil. Applied Ecology and Environmental Research 3(1): 47-53. [ Links ]
17. Osuji, L.C., E.J. Egbuson y C.M. Ojinnaka. 2005. Chemical reclamation of crude- oil-inundated soils from Niger Delta, Nigeria. Chemistry and Ecology 21(1): 1-10. [ Links ]
18. Osuji, L.C. y U.C. Opiah. 2007. Hydrocarbon contamination of a terrestrial ecosystem: the case of Oshire-2 oil spill in Niger Delta, Nigeria. Environmentalist 27: 337-340. [ Links ]
19. Pignatello, J. y B. Xing. 1996. Mechanisms of show sorption of organic chemicals to natural particles. Environmental Science Technology 30: 1-11. [ Links ]
20. Röling, W., M. Milner, D. Jones, K. Lee, F. Daniel, R. Swannell e I. Head. 2002. Robust hydrocarbon degradation and dynamics of bacterial communities during nutrient-enhanced oil spill bioremediation. Applied Environmental Microbiology 68: 5537-5548. [ Links ]
21. Vasudevan, N. y P. Rajaram. 2001. Bioremediation of soil sludge-contaminated soil. Environment International 26: 409-411. [ Links ]
22. Yerushalmi, L., S. Rocheleau, R. Cimpoia, M. Sarrazin, G. Sunahara, A. Peisajovich, G. Leclair y S. Guiot. 2003. Enhanced Biodegradation of Petroleum Hydrocarbons in contaminated soil. Bioremediation J. 7(1): 37-51. [ Links ]
23. Zamora, A.C. 2006. Análisis funcional de comunidades bacterianas asociadas a un proceso de biorremediación de muestras de suelo contaminadas con hidrocarburo. Tesis. Escuela de Biología. Facultad de Ciencias, UCV. Caracas. 89 p. [ Links ]
24. Zelles, L., Q. Bai, R. Rackwitz, D. Chadwick y F. Beese. 1995. Determination of phospholipid and lipopolysaccharide derived fatty acids as an estimate of microbial biomass and community structures in soil. Plant Soil 170: 115-122. [ Links ]