Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Agronomía Tropical
versión impresa ISSN 0002-192X
Agronomía Trop. v.54 n.2 Maracay abr. 2004
EL CULTIVO Y EL AGUA DE RIEGO SOBRE EL CARBONO DE LA BIOMASA MICROBIANA
Magaly Ruiz* y Jorge Paolini**
* Profesora. Universidad Rómulo Gallegos. Centro de Investigaciones y Extensión en Suelos y Aguas (CIESA). Vía El Castrero, San Juan de los Morros 2301. Estado Guárico.
** Investigador. Instituto Venezolano de Investigaciones Científicas (IVIC). Centro de Ecología. Apdo. 21827. Caracas 1020-A. Venezuela.
RESUMEN
En este estudio se determinó el carbono de la biomasa microbiana en ocho suelos cultivados con caña de azúcar y banano, regados con aguas de distinto origen (residuales, de pozo, de lago), y en dos suelos bajo vegetación natural (suelos testigo), localizados todos en la Cuenca del Lago de Valencia. El carbono de la biomasa microbiana (C-BM) se determinó por el método de la respiración inducida por sustrato. Los valores obtenidos variaron entre 206 y 1.553 µg C-BM g-1 suelo, siendo más altos en los suelos testigos y en los suelos lacustrinos sembrados con caña de azúcar bajo riego con aguas residuales industriales y domésticas. Los valores del C-BM resultaron superiores en los suelos bajo banano (P<0,05). El cociente C-BM/C total varió entre 1,4 y 4,1%, estando dentro del intervalo indicado para suelos agrícolas. Se encontró una correlación positiva (r = 0,787) y significativa (P<0,0001) entre el C-BM y el contenido de carbono orgánico total. Los resultados reflejan la influencia del cultivo y las prácticas de manejo agrícola sobre la biomasa microbiana del suelo.
Palabras Clave: Respiración inducida por sustrato; suelos lacustrinos; suelos aluviales; aguas de riego; caña de azúcar; banano.
SUMMARY
In the present study, soil microbial biomass carbon (MBC) was determined in eight soils located in the Valencia Lake basin, cultivated with sugarcane or banana and irrigated with waters of different composition or origin (waste-, ground- and lake-water), and in two soils under natural vegetation (control soils). MBC was estimated by substrate induced respiration method. MBC varied between 206 and 1.553 µg microbial C g-1 soil. Highest values occurred in control soils and in the lacustrine soil cultivated with sugar cane and irrigated with waste waters. The values of MBC were higher in the alluvial soils cultivated with sugarcane than in the alluvial soils cultivated with banana (P<0.05). The MBC to soil organic carbon ratio ranged from 1.4 to 4.1% and agreed with the data found in the literature for agricultural soils. MBC was correlated strongly with total organic carbon (r = 787; P<0.0001). Results show the influence of cultivation and crop management practices on MBC.
Key Words: Substrate induced respiration; lacustrine soils; alluvial soils; irrigation waters; sugar cane; banana.
RECIBIDO: noviembre 11, 2003.
INTRODUCCIÓN
Los microorganismos son los principales mediadores de la tasa de recambio del carbono en el suelo. Por definición ellos también son parte del carbono orgánico y del reservorio de nutrimentos, y como tales, ellos son denominados biomasa microbiana (INSAM, 1990).
La biomasa microbiana se define como la parte de la materia orgánica en el suelo constituida por los microorganismos vivos, con tamaños entre 5 y 10 µm3 menores de 5 a 10 µm3 (Alef y Nannipieri, 1995). La biomasa generalmente se expresa como mg de carbono por kilogramo de suelo, o también como µg de C por gramo de suelo seco.
El interés en estimar la biomasa microbiana se relaciona con su doble función como catalizador y como fuente (a través de la mineralización)/reservorio (a través de la inmovilización) en la transformación de nutrimentos; su papel en la formación y estabilización de la estructura del suelo y como un indicador ecológico (Alef y Nannipieri, 1995).
La biomasa microbiana del suelo es uno de los componentes vivos esenciales de todos los ecosistemas terrestres. Esta regula muchos procesos críticos del ecosistema, incluyendo la descomposición de materiales orgánicos, su transformación y el reciclaje de nutrimentos, y la integración biofísica de la materia orgánica con las fases sólida, acuosa y gaseosa del suelo.
A través de su interacción con otros organismos, por ejemplo con la fauna y las raíces de las plantas, la biomasa microbiana del suelo también llega a ser vital en la regulación de la cantidad y calidad de componentes en el ciclo hidrológico y en las emisiones de los gases de invernadero. Debido a esos atributos, la biomasa microbiana debe ser considerada como un indicador importante en la determinación de la calidad del suelo (Franzluebbers, 1999).
Algunos factores ecológicos determinan la biomasa microbiana del suelo y frecuentemente son responsables en gran parte de la variación espacial y temporal de la misma. La composición de las especies de plantas, principalmente a través de la producción primaria neta y de la calidad del mantillo, puede afectar las mediciones de la biomasa microbiana junto con la cadena trófica en el suelo, donde las interacciones entre los distintos organismos pueden influir en la actividad microbiana (Carter et al., 1999).
En general, las plantas sirven como una fuente de carbono para la comunidad microbiana y a su vez, los microorganismos proveen nutrimentos para el crecimiento de las plantas a través de la mineralización de los residuos de plantas y animales y de la materia orgánica del suelo (Srivastava y Singh, 1991).
La biomasa microbiana es el indicador más importante de la composición microbiana en el suelo, especialmente en combinación con un parámetro de actividad tal como la producción de CO2 (Anderson y Domsch, 1993).
El carbono de la biomasa microbiana (C-BM) responde mucho más rápidamente que el carbono orgánico total a los cambios en la calidad del suelo. Las variaciones en el carbono orgánico total son más lentas de detectar debido a que éste incluye un alto porcentaje de fracciones estables, las cuales pueden enmascarar variaciones que tienen lugar en las fracciones menos recalcitrantes.
Por otra parte, el C-BM responde eficazmente y con mucha sensibilidad a las prácticas de manejo agrícola (Brookes, 1995), en especial a la incorporación de materiales orgánicos, aún a bajas dosis (Pascual et al., 1997; Powlson et al., 1987). De allí que la determinación del carbono microbiano represente una herramienta útil para la comprensión y predicción de los efectos, que a largo plazo, puedan producir los cambios en las condiciones del suelo (Srivastava y Singh, 1991).
El cociente C-BM * 100/ COT (donde COT = carbono orgánico total) representa el carbono asociado a la fracción viva de la materia orgánica, expresado como porcentaje del carbono orgánico total del suelo. Se ha establecido que el C-BM de los suelos agrícolas, en los que el contenido de C se encuentra en equilibrio, varía entre 2,3 y 4,0% del carbono orgánico total, y aquellos suelos que se desvían de dicho intervalo se encontrarían, perdiendo carbono o bien acumulándolo (Insam, 1990).
En este estudio se determinó el C-BM en distintos suelos cultivados con caña de azúcar y banano, regados con aguas de distinto origen, y de dos suelos bajo vegetación natural, localizados en la Cuenca del Lago de Valencia, con la finalidad de evaluar la influencia del cultivo y la composición del agua de riego sobre el C-BM.
MATERIALES Y MÉTODOS
Para realizar el presente estudio se escogieron diez suelos dentro de la Cuenca del Lago de Valencia, cinco de ellos de origen lacustrino y cinco de origen aluvial (Cuadro 1). Los suelos lacustrino están ubicados en las siguientes zonas: a) sureste del municipio Guacara (estado Carabobo) en una unidad de producción agrícola localizada en el sector Las Palmeras, empresas campesinas El Cedro y Francisco de Miranda, en las que se cultivan 70 h de caña de azúcar.
En esta unidad se escogieron 3 tablones que se distinguieron con las siglas GL, GP, GS; b) Finca Torumo (suelo PAV), también en el municipio Guacara del estado Carabobo. Esta finca se encuentra limitada por la población de Guacara, al norte y el Lago de Valencia al sur; c) Caño Rico (suelo CR) en la empresa agrícola Inversiones Rico Caño.
Los suelos de origen aluvial se encuentran en las zonas que se mencionan a continuación: a) entre Santa Cruz y Cagua, en el municipio Lamas, estado Aragua, localizados en las haciendas Los Aguirre (AG), La Josefa (JO) y La Soledad (SD y SC); b) Palo Negro (PN), en la finca Morales, ubicada en el sector Paraparal, municipio Mariño, estado Aragua.
Entre los suelos seleccionados se incluyeron dos suelos testigo, uno lacustrino (PAV) y otro aluvial (SC), los cuales se encuentran bajo vegetación natural, nunca han sido cultivados ni regados. Los ocho suelos restantes se encuentran bajo cultivo de caña de azúcar o de banano y son regados con agua de distinto origen o composición. En el Cuadro 1 se resume la información sobre los suelos seleccionados, el tipo de cultivo que soportan y el agua de riego utilizada.
El suelo lacustrino CR está sembrado con banano y se riega con aguas tratadas que proceden del embalse de Taigüaigüay. Los suelos GS, GP y GL, también de origen lacustrino, están sembrados con caña de azúcar. El suelo GS se regó por 13 años con aguas residuales sin tratamiento, que son una mezcla de un efluente industrial proveniente de una planta de pulpa y papel ubicada en la zona y de las aguas residuales urbanas de un sector de la ciudad de Guacara. El suelo GP se riega con aguas subterráneas (pozo profundo), y el suelo GL se riega con agua del lago de Valencia.
Para conocer una descripción detallada de los suelos GS y GP, así como los resultados del análisis completo de las aguas utilizadas para el riego puede consultarse a Méndez (1998). La información relacionada con la composición del agua del lago de Valencia y del embalse de Taigüaigüay ha sido reseñada por Villafañe (1997). Los suelos de la finca Torumo son descritos por Viloria et al. (1996).
CUADRO 1. Propiedades de los suelos estudiados.
| Origen del Suelo | Suelo | Cultivo | Agua de riego | pH | %C | Textura |
| Lacustrino | PAV | Vegetación natural | Sin Riego | 6,97 | 8,14 | Suelo calcáreo |
| GL | Caña de azúcar | Agua de lago | 7,68 | 1,72 | Suelo calcáreo | |
| GP | Caña de azúcar | Agua de pozo | 7,64 | 1,71 | Suelo calcáreo | |
| GS | Caña de azúcar | Agua residual Industrial y doméstica | 7,41 | 3,29 | Suelo calcáreo | |
| CR | Banano | Agua sistema Taiguaiguay | 7,91 | 5,40 | Franca | |
| Aluvial | SC | Vegetación natural | Sin riego | 6,96 | 4,75 | Franca |
| AG | Caña de azúcar | Río Aragua | 7,54 | 1,99 | Franca | |
| JO | Caña de azúcar | Embalse Zuata | 7,52 | 2,11 | Franca | |
| SD | Banano | Embalse Zuata | 7,59 | 0,89 | Franca | |
| PN | Banano | Río Turmero | 7,78 | 1,29 | Franco-limoso |
Los suelos aluviales AG y JO (sembrados con caña de azúcar) se riegan con aguas tratadas del embalse de Zuata, pero el suelo AG ocasionalmente es regado también con aguas no tratadas del río Aragua. Los suelos aluviales PN y SD están cultivados con banano. El suelo PN se riega con aguas no tratadas del río Turmero, y el suelo SD con aguas del embalse Zuata.
Información sobre la composición de las aguas del embalse Zuata y el río Aragua ha sido reseñada por Villafañe (1997). Los resultados de los análisis del suelo PN y de los análisis de las aguas utilizadas en el riego de ese suelo, son indicados por Hernández (1999).
Los suelos lacustrinos clasifican todos como Mollic Ustifluvents, francosa, carbonática, mixta, isohipertérmica, y los aluviales como Fluventic Ustropepts, francosa gruesa mixta isohipertérmica, a excepción del suelo PN que clasifica como Fluventic Haplustolls.
Para el momento en que se tomaron las muestras, los suelos lacustrinos GS, GP, GL habían estado sembrados con caña de azúcar por un período de trece años; el suelo CR tenía veinte años cultivado con banano; los suelos aluviales AG y JO contaban siete y cuarenta y tres años bajo caña de azúcar, respectivamente; y los suelos SD y PN tenían seis años cultivados con banano (anteriormente se cultivó maíz en estos suelos entre diez y trece años).
Las muestras de suelo se tomaron a una profundidad de 0-5 cm. Para cada suelo se recogieron submuestras de igual volumen en 20 puntos diferentes del área a considerar, en forma aleatoria, y las mismas se mezclaron para obtener una muestra compuesta. Esta última se dividió en dos porciones. Una de las porciones se secó al aire, luego se trituró y se tamizó en una malla de 2 mm, y se utilizó para los análisis físicos y químicos del suelo. La otra porción no se secó, se conservó con la humedad del campo, se tamizó a un tamaño menor de 2 mm y se guardó en bolsas plásticas bajo refrigeración a 4 °C, para ser posteriormente utilizadas en un lapso no mayor de 2 semanas en la determinación del C_BM.
El C-MB se determinó por el método de la respiración inducida por sustrato (Anderson y Domsch, 1978), el cual se fundamenta en el hecho de que se pueda estimular la respiración de los microorganismos del suelo si se adiciona a este medio un sustrato fácilmente degradable, como la glucosa. Por medio de esta respuesta fisiológica se logra proveer una estimación del carbono de la biomasa microbiana. El CO2 producido durante la incubación del suelo con el sustrato, en un sistema cerrado, se captura en un vial con solución de NaOH, la cual es titulada posteriormente con HCl.
El carbono orgánico total se determinó mediante el método de digestión húmeda de Walkley y Black (1934), basado en la hidrólisis y oxidación del carbono orgánico por una mezcla oxidante de dicromato de potasio y ácido sulfúrico concentrado, acelerada por el calor de dilución del ácido sulfúrico en agua.
La cantidad de carbono orgánico oxidado por el Cr(VI) se mide por colorimetría, bien sea por la medida de la concentración de Cr(VI) remanente o por la concentración del Cr(III) formado durante la reacción (Sims y Haby, 1971). En este experimento se midió la intensidad del color verde de los iones Cr(III) producidos, en un espectrofotómetro Spectronic 20D Milton Roy Company, a una longitud de onda de 600 nm, y comparando con lecturas de una curva de calibración preparada previamente con soluciones patrones de glucosa, sometidas al mismo tratamiento que las muestras.
El pH se midió en una suspensión suelo:agua 1:1. La clasificación textural se realizó mediante el método de Bouyoucos modificado (López y López, 1978).
Todas las determinaciones se hicieron por triplicado. Los resultados se presentan con base al peso seco del suelo, por lo cual se efectuaron determinaciones de humedad de los suelos simultáneamente con los análisis mencionados. El contenido de humedad se determinó por la diferencia de peso que experimentaron las muestras después de ser sometidas a calentamiento a 105 °C por 24 horas.
El análisis estadístico de los datos se realizó con el programa STATISTIX para Windows versión 1.0, 1996. Se realizaron análisis de varianza, prueba de medias de Tukey, y análisis de regresión lineal.
RESULTADOS Y DISCUSIÓN
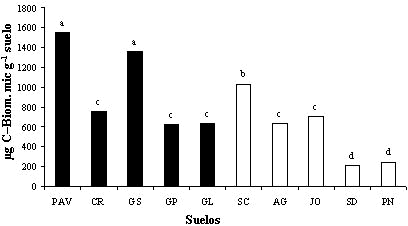
Los valores del C-BM determinados en los suelos estudiados varían entre 206 y 1.553 µg C g-1 de suelo (Figura 1). Estos valores son similares a los encontrados por otros autores para suelos de regiones templadas y tropicales. Por ejemplo, Hernández (1998) indica valores entre 394 y 1.587 µg C g-1 para un Inceptisol de Turén (estado Portuguesa), bajo cultivo de maíz; Borie et al. (1999), en un estudio realizado en suelos chilenos, obtuvieron valores de C-BM entre 600 y 1.300 µg C g-1 en suelos agrícolas, de 700 µg C g-1 en pradera natural, y de 1.000 µg C g-1 en bosque natural. Para suelos de España, Díaz-Raviña et al. (1993) citan valores entre 282 y 1.614 µg C g-1, y Basu y Behera (1993) señalan valores entre 350 y 850 µg C g-1 en suelos tropicales de la India.
En los suelos lacustrinos, el valor más alto del C-BM se presenta en el suelo bajo vegetación natural (PAV). Sin embargo, no se encontraron diferencias significativas entre los valores del C-BM del suelo testigo PAV y los del suelo GS (sembrado con caña de azúcar y regado con aguas residuales industriales y domésticas). Por otra parte, el C-BM de los suelos PAV y GS difiere significativamente (P<0,05) de los valores encontrados para el resto de los suelos lacustrinos (CR, GL y GP). Entre estos últimos no se encontraron diferencias significativas, independientemente del tipo de cultivo.
FIGURA 1. Carbono en la biomasa microbiana de los suelos estudiados. Las barras que presentan la misma letra corresponden a medias que no son estadísticamente diferentes, según la prueba de medias deTukey (P<0,05); las barras de color negro corresponden a los suelos lacustrinos y las blancas a los suelos aluviales.
El incremento en el C-BM del suelo regado con aguas residuales industriales y domésticas (GS), con respecto a los otros suelos lacustrinos cultivados (CR, GL y GP), podría atribuirse a la incorporación de materiales orgánicos fácilmente biodegradables junto con la aguas, los cuales estimulan la actividad microbiana autóctona del suelo, o a la incorporación de microorganismos exógenos (Perucci, 1992).
Como se especificó anteriormente, para el momento en que se realizó este estudio, el suelo Guacara GS había sido regado por más de 13 años con una mezcla de aguas residuales de una planta de pulpa y papel y de aguas urbanas de un sector de la ciudad de Guacara.
En suelos agrícolas de Alemania, regados por 100 años con aguas residuales (efluentes primarios), también se observó un incremento en el C-BM (medido por ATP) con respecto a los valores encontrados en los suelos de la misma zona regados con aguas tratadas, durante el mismo período. Este incremento en el C-BM se observó aún en suelos en los que el riego con las aguas residuales se había interrumpido desde hacía 20 años (Filip et al., 1999).
En los suelos aluviales los valores más altos del C-BM correspondieron al suelo bajo vegetación natural (SC) y se observaron diferencias significativas entre éste y los suelos cultivados (P<0,05). Estos resultados coinciden con los indicados por Suttner y Alef (1988) para suelos de Alemania. Saviozzi et al. (1999) también encontraron menores valores del C-BM en suelos de Italia cultivados con maíz y trigo en comparación con suelos de la misma área que permanecían bajo vegetación natural.
Resultados similares fueron señalados por Gupta y Germida (1988) para suelos canadienses bajo pasto, en los que el contenido de C-BM se midió en macro y micro agregados, y se encontraron valores menores de C-BM en relación con los de los suelos no alterados de la zona estudiada.
Por otra parte, en suelos tropicales de la India, se observó una disminución entre 52 y 58% en el C-BM, cuando los suelos de bosque se transformaron en pradera o en suelos agrícolas respectivamente (Basu y Behera, 1993). En suelos de bosques nativos de Chile se han encontrado valores mayores del C-BM, en comparación con suelos de praderas cultivadas con avena_ballica (Avena sativa-Lolium multiflorum) (BORIE et al., 1999).
Los suelos aluviales sembrados con caña de azúcar (AG y JO) mostraron mayores valores del C-BM que los suelos con cultivo de banano (SD y PN) (Figura 1).
A pesar de ser regados con aguas de diferente origen, los suelos SD y PN no mostraron diferencias significativas en el C-BM, independientemente de que el agua residual utilizada para su riego hubiese sido sometida o no a tratamiento (Cuadro 1). Tampoco se observaron diferencias entre los suelos aluviales sembrados con caña de azúcar (AG y JO) relacionadas con el origen del agua de riego.
Cuando se comparan todos los suelos sembrados con caña de azúcar, tanto lacustrinos como aluviales, se observa que los suelos GP, GL, AG, JO no presentan diferencias significativas (P<0,05) en cuanto a su C-BM. En cambio, el suelo GS, que también está sembrado con caña de azúcar y es regado con una mezcla de aguas residuales industriales y domésticas, muestra un valor de C-BM que es aproximadamente el doble de los que presentan los suelos antes mencionados (Figura 1).
Esta diferencia también se observa respecto a la fertilidad de esos suelos y a los rendimientos del cultivo. En los suelos aluviales AG y JO los rendimientos de caña de azúcar son de aproximadamente 90-100 ton ha_1, y en los suelos lacustrinos GP y GL (regados con agua de pozo y de lago, respectivamente) son alrededor de 140 ton ha-1 , mientras que en el suelo GS (regado con las aguas residuales industriales y domésticas) los rendimientos son de 170 ton ha_1 (Méndez, 1998).
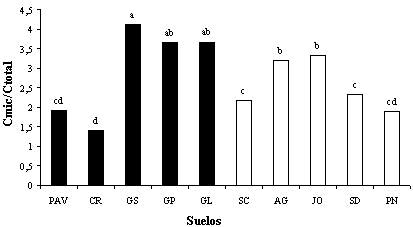
Las medidas de la biomasa microbiana indican que entre el 1 y el 5% del carbono orgánico total del suelo se almacena en los tejidos vivos (Alef y Nannipieri, 1995). En el caso de los suelos estudiados, la relación C-BM * 100/COT varió entre 1,40 y 4,12% (Figura 2), con un valor promedio para los suelos cultivados de 2,95%, y para los suelos bajo vegetación natural de 2,04%.
Estos valores corresponden a los indicados para suelos agrícolas, y concuerdan con los valores obtenidos por INSAM (1990) en suelos de Norteamérica de distintas regiones climáticas, con un promedio de 2,3% para suelos con monocultivo permanente y 2,9% para suelos bajo rotación de cultivos. Los valores también son similares a los encontrados por Chander et al. (1998) en suelos de la India, comprendidos entre 3,68 y 4,00%, y por Anderson y Joergensen (1997) para suelos forestales de Alemania, entre 0,8 y 3,3%.
En la Figura 2 se observa que los suelos con vegetación natural PAV y SC presentaron valores relativamente bajos del cociente C-BM * 100/ COT y no presentaron diferencias significativas (P<0,05) con los valores obtenidos en los suelos bajo banano (CR, SD, PN), pero sí se evidenciaron las diferencias con respecto a los suelos sembrados con caña de azúcar (GS, GP, GL, AG, JO) los cuales presentaron los valores más altos.
Los resultados de distintas investigaciones coinciden con esta tendencia de presentar mayores valores de este índice en suelos cultivados que en suelos bajo vegetación natural. Así lo revelan algunos estudios realizados en suelos de Italia (Saviozzi et al., 1999), de Dinamarca (Powlson et al., 1987) y de la región de Murcia, España (Pascual, 1996).
Los suelos que presentan valores relativamente bajos de la relación C-BM*100/COT, deben contener una considerable proporción de carbono orgánico total muy humificado y por tanto difícilmente utilizable por los microorganismos (Pascual, 1996).
FIGURA 2. Relación C biomasa microbiana * 100/ C orgánico total en los suelos estudiados. Las barras que presentan la misma letra corresponden a medias que no son estadísticamente diferentes, según la prueba de medias de Tukey (P<0,05); las barras de color negro corresponden a los suelos lacustrinos y las blancas a los suelos aluviales.
Los suelos lacustrinos y aluviales que se encuentran bajo caña de azúcar (GS, GP, GL, AG y JO) son sometidos a quema antes de la cosecha. Está demostrado que esta práctica ocasiona una pérdida del carbono orgánico total del suelo (Dominy et al., 2002) porque conduce a una reducción drástica de los aportes de materia orgánica por parte del cultivo, y si a esto se suma la remoción total de la parte aérea de la planta, que se traslada fuera del campo, se infiere que el principal aporte de materia orgánica en este caso proviene prácticamente de las raíces.
Además tienen lugar otros cambios que comúnmente se producen en los suelos que son deforestados y luego cultivados, como son las modificaciones en la temperatura, el régimen de humedad del suelo y los procesos biológicos que afectan la descomposición de la materia orgánica (Anderson y Flanagan, 1989).
También se conoce que con el cultivo puede reducirse la estabilidad de los agregados del suelo, y al degradarse los agregados se acelera la oxidación del carbono orgánico al exponerse nuevas superficies al ataque microbiano y al cambiar las condiciones redox con la profundidad en el perfil (Roberts y Chang, 1990; Golchin et al., 1995).
Diversas investigaciones han comprobado que existe una relación directa entre la reducción del contenido de carbono orgánico y la disminución del C_BM (Haynes, 2000), que indica que mientras mayor es la pérdida de carbono orgánico de un suelo, más pequeña resulta su biomasa microbiana. La explicación que se ha dado a este hecho se basa en que el C_BM es una de las fracciones lábiles y fácilmente degradables de la materia orgánica, y con mayor susceptibilidad de ser perdida (Hart et al., 1988).
En investigaciones realizadas en suelos de Suráfrica, sembrados con caña de azúcar por períodos desde uno hasta 80 años, en los que se utiliza la quema previa a la cosecha, se encontró que el carbono orgánico total y el C_BM decrecían en forma exponencial a medida que aumentaban los años bajo el monocultivo de caña de azúcar, siendo considerablemente más marcada la disminución del C_BM que la del carbono orgánico total, y menor el efecto en los suelos con mayor contenido de arcilla (Dominy et al., 2002). Además, se evidenció la existencia de una correlación lineal entre el contenido de carbono orgánico total y el C-BM (r = 0,748; P<0,01).
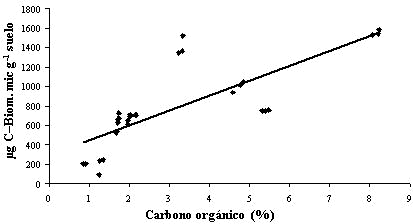
En el presente estudio también se observó menor contenido de carbono orgánico total en los suelos cultivados con caña de azúcar (ver Cuadro ) en comparación con los suelos no alterados de la zona (PAV y SC). Se aprecia que los contenidos de carbono orgánico total de los suelos testigo PAV y SC duplican o triplican los valores encontrados en los suelos bajo caña de azúcar (y en el resto de los suelos cultivados). Igualmente, se encontró una correlación positiva y altamente significativa entre el C-BM y el contenido de carbono orgánico total (r = 0,787; P<0,0001, Figura 3).
Para suelos agrícolas bajo otros cultivos y distintos sistemas de manejo también se han encontrado correlaciones significativas entre el C-BM y el carbono orgánico total (Leita et al., 1999). Theng et al. (1989) obtuvieron relaciones lineales entre esos dos parámetros para diversos suelos de regiones templadas y tropicales.
El C-BM de los suelos estudiados resultó altamente correlacionado con la respiración basal (r = 0,904, P<0,0001) (Ruiz, 2002), lo que concuerda con los resultados encontrados por Pascual (1996) en suelos de la región de Murcia (España). Además, se encontraron correlaciones positivas y significativas entre el C-BM y la amonificación de arginina, y las actividades de las enzimas: fosfomonoesterasa alcalina, fosfomonoesterasa ácida, ureasa, deshidrogenasa, proteasa, y ß-glucosidasa (Ruiz, 2002).
FIGURA 3. Correlación entre el carbono de la biomasa microbiana y el carbono orgánico total en los suelos estudiados.
CONCLUSIONES
- Tanto en los suelos de origen aluvial, como en los de origen lacustrino, los valores más altos del C-BM corresponden a los suelos bajo vegetación natural y en general se observan diferencias significativas entre éstos y los suelos cultivados, lo cual refleja la influencia del cultivo y las características del agua de riego sobre la magnitud de la biomasa microbiana del suelo.
- El C-BM en los suelos estudiados muestra una correlación positiva y significativa con su contenido de materia orgánica.
BIBLIOGRAFÍA
1. ALEF, K. and P. NANNIPIERI. 1995. Microbial biomass. In: Alef, K. and P. Nannipieri. (Eds). Methods in applied soil microbiology and biochemistry. Academic Press. Arcourt Brace and Company, Publishers. p. 375. [ Links ]
2. ANDERSON, J. M. and P. W. FLANAGAN. 1989. Biological processes regulating organic matter dynamics in tropical soils. In: Coleman, D., J. M. Oades, G. Uehara (Eds). Dynamics of soil organic matter in tropical ecosystem. Niftal Project. Department of Agronomy and Soil Science. College of Tropical Agriculture and Human Resources. University of Hawaii. p. 97-122. [ Links ]
3. ANDERSON, J. P. E. and K. H. DOMSCH. 1978. A physiological method for the Quantitative measurement of microbial biomass in soil. Soil. Biol. Biochem. 10:215-221. [ Links ]
4. ANDERSON, T. H. and K. H. DOMSCH. 1993. The metabolic quotient for CO2 (qCO2) as a specific activity parameter to assess the effects of environmental conditions, such as pH, on the microbial biomass of forest soils. Soil Biol. Biochem. 25:393-395. [ Links ]
5. ANDERSON, T. and R. JOERGENSEN. 1997. Relationship between SIR and FE estimates of microbial biomass C in deciduous forest soils at different pH. Soil Biol. Biochem. 29:1.033-1.042. [ Links ]
6. BASU, S. and N. BEHERA. 1993. The effect of tropical conversion on soil microbial biomass. Biol. Fertil. Soils 16:302-304. [ Links ]
7. BORIE, G., S. AGUILERA y P. PEIRANO. 1999. Actividad biológica en suelos. Frontera Agrícola 5:29-32. [ Links ]
8. BROOKES, P. C. 1995. The use of microbial parameters in monitoring soil pollution by heavy metals. Biol. Fertil. Soils 19:269-279. [ Links ]
9. CARTER, M. R., E. G. GREGORICH, D. A. ANGERS, M.H. BEARE, G. P. SPARLING, D. A. WARDLE and R. P. VORONEY. 1999. Interpretation of microbial biomass measurements for soil quality assessment in humid temperate regions. Can. J. Soil. Sci. 79:507-520. [ Links ]
10. CHANDER, K., S. GOYAL, D. P. NANDAL and K. K. KAPOOR. 1998. Soil organic matter, microbial biomass and enzyme activities in a tropical agroforestry system. Biol. Fertil. Soils 27:168-172. [ Links ]
11. DIAZ-RAVIÑA, M., M. J. ACEA and T. CARBALLAS. 1993. Microbial biomass and its contribution to nutrient concentrations in forest soils. Soil Biol. Biochem. 25:25-31. [ Links ]
12. DOMINY, C. S, R. J. HAYNES and R. VAN ANTWERPEN. 2002. Loss of soil organic matter and related soil properties under long-term sugarcane production on two contrasting soils. Biol Fertil Soils 36:350-356. [ Links ]
13. FILIP, Z., S. KANAZAWA and J. BERTHELIN. 1999. Characterization of effects of a long-term wastewater irrigation on soil quality by microbiological and biochemical parameters. J. Plant Nutr. Soil Sci. 162:409-413. [ Links ]
14. FRANZLUEBBERS, A. J. 1999. Introduction to Symposium _ Microbial Biomass: Measurement and role in soil quality. Can. J. Soil Sci. 79:505-506. [ Links ]
15. GOLCHIN, A., P. CLARKE, J. M. OADES and J. O. SKJEMSTAD. 1995. The effects of cultivation on the composition of organic matter and structural stability of soil. Aust. J. Soil Res. 33:975-993. [ Links ]
16. GUPTA, V. and J. GERMIDA. 1988. Distribution of microbial biomass and its activity in different soil aggregate size classes as affected by cultivation. Soil Biol. Biochem. 20:777-786. [ Links ]
17. HART, P.B.S., J. A. AUGUST, C. W. ROSS and J. F. JULIAN. 1988. Some biochemical and physical properties of Tokomaru silt loam under pasture and after 10 year of cereal cropping. New Zealand J. Agric. Res. 31:77-86. [ Links ]
18. HAYNES, R. J. 2000. Labile organic matter as an indicator of organic matter quality in arable and pastoral soils in New Zealand. Soil Biol. Biochem 32:211-219. [ Links ]
19. HERNÁNDEZ, R. 1999. Dinámica de sales y oligoelementos en dos suelos regados con aguas residuales. Trabajo de Grado Magister Scientiarum en Ingeniería Agrícola. Maracay, Ven. Universidad Central de Venezuela. Facultad de Agronomía. 108 p. [ Links ]
20. HERNÁNDEZ, W. 1998. Efecto de tres sistemas de labranza sobre la dinámica poblacional y la actividad microbiológica de un suelo cultivado con maíz. Trabajo de Grado para optar al título de Magister Scientiarum en Ciencia del Suelo. Maracay, Ven. Universidad Central de Venezuela. Facultad de Agronomía. 134 p. [ Links ]
21. INSAM, H. 1990. Are the soil microbial biomass and basal respiration governed by the climatic regime?. Soil Biol. Biochem. 22:525-532. [ Links ]
22. INSAM, H., C. MITCHELL and J. DORMAAR. 1991. Relationships of soil microbial Biomass and activity with fertilization practice and crop yield of three ultisols. Soil Biol Biochem. 23:459-464 [ Links ]
23. LEITA, L., M. DE NOBILI, C. MONDINI, G. MUHLBACHOVA, L. MARCHIOL, G. BRAGATO and M. CONTIN. 1999. Influence of inorganic and organic fertlization on soil microbial biomass, metabolic quotient and heavy metal bioavailability. Biol Fert. Soils. 28:371-376. [ Links ]
24. LIN, Q. and P.C. BROOKES. 1999. An evaluation of the substrate-induced respiration method. Soil Biol. Biochem. 31:1.969-1.983. [ Links ]
25. LÓPEZ, R. y M. LÓPEZ. 1978. El diagnóstico de suelos y plantas. Editorial Mundi-Prensa, Madrid, España. 287 pp. [ Links ]
26. MÉNDEZ, F. 1998. Contribución al estudio sobre el uso de aguas residuales con fines de riego. Trabajo de ascenso. Maracay, Ven. Universidad Central de Venezuela. Facultad de Agronomía. 128 p. [ Links ]
27. PASCUAL, J. A. 1996. Efectividad de los residuos orgánicos en la mejora de la calidad de suelos áridos aspectos biológicos y bioquímicos. Tesis Doctoral. Universidad de Murcia (España). 428 p. [ Links ]
28. PASCUAL, J., C. GARCÍA, T. HERNÁNDEZ and M. AYUSO. 1997. Changes in the microbial activity of an arid soil amended with urban organic wastes. Biol. Fert. Soils. 24:429-434. [ Links ]
29. PERUCCI, P. 1992. Enzyme activity and microbial biomass in a field soil amended with municipal refuse. Biol. Fertil. Soils 14:54-60. [ Links ]
30. POWLSON, D. S., P. C. BROOKES and B. T. CHRISTENSEN. 1987. Measurement of soil microbial biomass provides an early indication of changes in the total soil matter due to straw incorporation. Soil Biol. Biochem. 19:159-164. [ Links ]
31. ROBERTS, W.P. and K. Y. CHANG. 1990. Tillage induced increases in carbon dioxide loss from soil. Soil Tillage Res. 17:143-151. [ Links ]
32. RUIZ, M. 2002. Caracterización de la materia orgánica y la actividad biológica de suelos de la Depresión del Lago de Valencia sometidos a diversas formas de manejo. Tesis Doctoral. Postgrado en Ciencia del Suelo. Maracay, Ven. Facultad de Agronomía. Universidad Central de Venezuela. 257 p. [ Links ]
33. SAVIOZZI, A., A. BIASCI, R. RIFFALDI and R. LEVI-MINZI. 1999. Long-term effects of farmyard manure and sewage sludge on some soil biochemical characteristics. Biol. Fert. Soils 30:100-106. [ Links ]
34. SIMS, J. R. and V. A. HABY. 1971. Simplified colorimetric determination of soil organic matter. Soil Sci. 112:137-141. [ Links ]
35. SRIVASTAVA, S. C. and J. S. SINGH. 1991. Microbial C, N and P in dry tropical forest soils: effects of alternate land-uses and nutrient flux. Soil Biol Biochem 23:117-124. [ Links ]
36. SUTTNER, T. And K. ALEF.1988. Correlation between the arginine ammonification, enzyme activities, microbial biomass, physical and chemical properties of different soils. Zentralbl. Mikrobiol. 143:569-573. [ Links ]
37. THENG, B., K. TATE and P. SOLLINS. 1989. Constituents of organic matter in temperate and tropical soils. In: Coleman, D., J. M. Oades, G. Uehara, (Eds.). Dynamics of soil organic matter in tropical ecosystem. Niftal Project. Department of Agronomy and Soil Science. College of Tropical Agriculture and Human Resources. University of Hawaii. p. 5-32. [ Links ]
38. VILLAFAÑE, R. 1997. Prácticas de riego con aguas residuales en la Cuenca del Lago de Valencia, Venezuela. Situación actual y perspectivas. In: Seminario Internacional sobre uso de Aguas residuales para riego. México, mayo 5-10, 1997. Memorias. p. 145-165. [ Links ]
39. VILORIA, J., C. ALVARADO, C. PINEDA y O. MIQUILENA. 1996. Los suelos de la Finca Torumo, Guacara, estado Carabobo. Estudio con Fines de Diseño y Monitoreo de Riego con Aguas Servidas. Maracay, Ven. Universidad Central de Venezuela. Facultad de Agronomía. 48 p. [ Links ]
40. WALKLEY, A. and I. A. BLACK. 1934. An examination of the Detjareff method for determining soil organic matter and a proposed modification on the chromic acid titration methods. Soil Sci. 37:29-38. [ Links ]