FENOLOGIA DE LA FLORACION EN DOS VARIEDADES DE NÍSPERO1
Norkys Meza* y Dámaso Bautista**
1 Proyecto financiado por el Consejo de Desarrollo Científico Humanístico y Tecnológico de la Universidad Centrooccidental Lisandro Alvarado.
*Investigadora. INIA. Centro Nacional de Investigaciones Agropecuarias del Estado Trujillo. Pampanito. Venezuela.
**Profesor Jubilado. Universidad Centroccidental Lisandro Alvarado Postgrado de Horticultura. Decanato de Agronomía. Apdo. 400, Barquisimeto, estado Lara. Venezuela.
RESUMEN
La fenología de la floración del níspero, Manilkara zapota van Royen, fue estudiada mediante observaciones diarias realizadas en las variedades Santiago y Delfina, desde el inicio de la brotación de las yemas floríferas hasta la antesis. El estudio se realizó sobre 5 ramas de 6 plantas de cada variedad las cuales fueron marcadas para observar y describir las fases evolutivas de la yema floral hasta la antesis. El desarrollo floral se presentó hacia la porción apical del eje ortotrópico y en las ramas plagiotrópicas y la duración fue cronológicamente muy similar en las dos variedades. Junto con la brotación de la yema terminal, los primordios florales y foliares inician su desarrollo simultáneamente desde posiciones subapicales. La floración fue observada mediante técnicas de microscopía de barrido. Acorde con las observaciones, el proceso de floración fue dividido en 5 fases distinguibles. La primera fase se inicia con la entrada en actividad meristemática y culmina cuando se hace visible el botón floral y el primordio foliar alcanza 6 mm , lo que ocurrió en 8 d. Durante la segunda fase se hacen distinguibles el pedúnculo y los sépalos, con una duración de mas o menos 20 d; la tercera fase finaliza cuando, además de los sépalos, pétalos se hace visible también el androceo, con una duración de 3 a 4 d. En la cuarta fase se completan la formación del pedúnculo, los sépalos más externos se observan separados y el estigma queda completamente formado y receptivo, con una duración de 7 d; durante la quinta fase se completa el desarrollo de la flor y se inicia la antesis. La flor presentó receptividad estigmática antes de ocurrir la dehiscencia de polen y su desarrollo se cumplió aproximadamente en 45 d, en las 2 variedades.
Palabras Claves: Manilkara zapota; fenología floral; yema; desarrollo.
SUMMARY
The phenology of sapodilla was studied, by means of daily observations carried out in the varieties Santiago and Delfina, from the initiation of flower bud breaking until antesis. The study was carried out on five branches of six plants of each to variety which were marked to observe and to describe the evolutionary phases of the floral shoots until anthesis. The floral development and the flowering were presented in the extreme apical and orthotropic and in the branches plagiotropic and the duration was chronologically very similar in the two varieties. Together with the breaking of the terminal shoot, the floral primordia and foliar they begin their development simultaneously from positions subapical. The flowering was observed by means of technical of sweeping microscopy. Chord with the observations, the flowering process was divided in five phases. The first phase began with the entrance in activity meristem distinet and it culminates when it becomes visible the floral button and the primordia to foliate reaches 6 mm , what happened in one week. During the second phase distinet the peduncle and the sepals were made, with a duration of but or less 20 days; the third phase concludes when, besides the sepals, petals become visible also the stamens, with a duration of 3 to 4 days. In the fourth phase they are already completed the formation of the peduncle, the most external sepals are observed separate and the stigma was totally formed and receptive, with a duration of seven days; during the fifth phase the development of the flower is completed and the anthesis began. The flower presented exudates stigmatic before happening the dehiscence of pollen and its development was completed approximately in 45 days, in the s two varieties.
Key Words: Manilkara zapota; floral phenology; bud; development.
RECIBIDO: marzo 12, 2004.
INTRODUCCIÓN
El Níspero, Manilkara zapota van Royen, pertenece a la familia Sapotaceae, la cual comprende unos 40 géneros y unas 800 especies (Bailey y Bailey,1976; Pennington, 1990). La planta es un árbol nativo de América tropical y se extiende desde el suroeste de México, América Central y norte de Sur América (Aristiguieta, 1950). La flor, una por axila foliar, es completa y hermafrodita; con pedúnculo verde oscuro y piloso, de longitud similar al del pecíolo foliar (Gilly, 1943; González y Feliciano, 1953). El receptáculo al cual se insertan los verticilos florales, tiene forma de disco (León, 1968).
El cáliz, está formado por 6 sépalos dispuestos en 2 series, una externa de tres sépalos gruesos y ligeramente más cortos que los de la segunda serie. La corola está formada por 6 pétalos fusionados a manera de una estructura tubular con 6 lóbulos erguidos, oblongos o elípticos, blanco amarillentos, muy pubescentes y de tamaño igual o ligeramente mayor al cáliz (León, 1968; Avilán et al., 1992; Pennington, 1990).
El androceo está conformado por una serie externa de 6 petaloides estaminados no funcionales y alternando con éstos, otra serie más interna de seis estambres insertados en la parte alta de la corola; las anteras son ovoides oblongas, de color café amarillentos y abren longitudinalmente (Lindorf et al., 1985; Pennington, 1990).
El gineceo esta formado por el pistilo, el cual presenta un ovario súpero con hasta 12 lóculos, de los cuales cada uno puede contener un óvulo. El estilo normalmente es corto, pero, excede ligeramente la longitud de los estaminoides para el momento de su madurez, lo que favorece la polinización cruzada, el estigma es pequeño de forma globosa y de color marrón oscuro cuando es receptivo (Gilly, 1943; Pennington, 1990).
El desarrollo de las flores así como la floración progresa de manera acrópeta en la rama, por lo que la última flor en formarse también es la última en abrir (Bautista y Meza, 2001). La flor aparentemente presenta protandría y la dehiscencia de polen ocurre a partir del tercer día después que el estigma ha sobresalido de la corola. El polen que descargan las anteras se localiza alrededor del estilo. La receptividad del estigma se aprecia, por el cambio de color del blanco y seco a marrón y húmedo cubierto por una secreción mucilaginosa, lo que ocurre al cuarto día después que el estigma ha sobresalido de la corola, el proceso de maduración estigmática ocurre de las 8:00 a.m. a las 5:00 p.m. La apertura floral ocurre al día siguiente y se inicia a las 3:00 a.m., quedando las flores completamente abiertas a la 1:00 p.m., después de aproximadamente 9 horas de duración del proceso; polinizadas o no, las flores vuelven a cerrase a las 72 horas siguientes a la apertura (González y Feliciano, 1953).
La flor hermafrodita del níspero aparentemente presenta el fenómeno de la autoincompatibilidad, lo que favorece también la polinización cruzada; sin embargo este fenómeno ha sido muy poco estudiado (Knight y Campbell, 1993).
Estudios sobre fenología de la floración en las Sapotaceas y en especial en el cultivo de níspero son pocos conocidos o nulos en el país; sin embargo, en frutales tropicales como aguacate (Salazar-García, 1988); en mango (Aubert y Lossois, 1972) y en cítricos (Krajewski y Rabe, 1995), estos procesos han sido ampliamente estudiados. El objetivo de esta investigación consistió en hacerle un seguimiento a la evolución de la diferenciación floral en dos variedades de níspero (Santiago y Delfina) para evaluar los cambios ocurridos durante el desarrollo floral.
MATERIALES Y MÉTODOS
La investigación se llevó a cabo en terrenos de Postgrado de Horticultura del Decanato de Agronomía de la Universidad Centro Occidental Lisandro Alvarado, ubicado en Tarabana, municipio Palavecino, estado Lara, (10º 05` LN; 510 m .s.n.m.).
Metodología para la fenología de la floración
Diez plantas por cada variedad fueron seleccionadas completamente al azar para establecer la secuencia de cambios, y eventos anatomorfológicos que ocurren en el curso del desarrollo de la flor. A cada planta seleccionada, se le marcaron 8 ramas con signos evidentes de desarrollo reproductivo, sometiendo los botones florales a observaciones diarias a lo largo del desarrollo de la flor.
Las observaciones consistieron en medir la longitud del pedúnculo y el diámetro del botón floral. Paralelamente, se recolectaron semanalmente 10 materiales en varios estados de desarrollo para observar el crecimiento interno de cada una de las estructuras florales. En este caso, los materiales florales fueron fijados en una solución de formol- acético- alcohol (FAA), para su estudio posterior en laboratorio. Los materiales ya fijados fueron examinados bajo una lupa óptica; posteriormente, se realizaron cortes longitudinales y transversales, los cuales fueron fijados y llevados al centro de microscopía electrónica para ser observadas mediante la técnica de microscopía de barrido.
Las muestras, antes de ser microfotografiadas fueron colocadas en acetona por espacio de 3 minutos aproximadamente, luego se colocaron sobre bases porta-muestras previamente identificadas; secándose más tarde mediante la técnica de punto crítico en un equipo SSPC marca BALTEC, modelo CPD-030 computarizado. Este procedimiento se usa para procesar muestras blandas prefijadas con glutaraldheido y osmio para evitar el colapso si son secadas por los métodos convencionales, siguiendo las técnicas recomendadas por Castillo (1999).
Luego las muestras fueron metalizadas para posteriormente ser observadas en el microscopio Philips MEB (XL-20) en el Centro de Microscopía Electrónica de la Facultad de Agronomía (CENMEFA), Maracay. Los datos se analizaron estadísticamente, utilizando la prueba de t de Student para establecer las diferencias entre los tratamientos.
RESULTADOS Y DISCUSIÓN
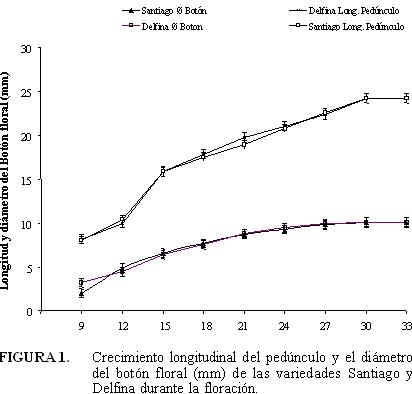
Desarrollo de la yema floral. La Figura 1 muestra el desarrollo expresado en la longitud del pedúnculo y del diámetro del botón floral en las variedades Santiago y Delfina. El pedúnculo y el diámetro de la flor alcanzaron sus mayores valores entre los 28 y 33 d, no mostraron diferencia significativa por lo que se considera como variedades muy similares en morfología y cronológicamente en cuanto a su desarrollo floral.
Las ramas laterales ortotrópicas en crecimiento paralizado pero con capacidad de floración, presentan en el ápice una yema en reposo con 7 a 8 primordios (Figura 2A y 2B), los cuales corresponden a primordios foliares de forma alargada y con abundante pubescencia.
En la axila de cada uno de estos primordio, se forma otro mucho más pequeño redondeado y muy piloso el cual se corresponde con el primordio floral ( Figura 2C ). Cuando la yema entra en actividad los primordio foliares y florales iniciaran simultáneamente el crecimiento desde posiciones subapicales de la yema (Figura 2B).El desarrollo del primordio foliar fue mucho más rápido e intenso que el floral (Figura 2C ), al punto que a los 8 días después que inicio su crecimiento el foliar medía 20 mm , mientras que el floral midió solo 6 mm .
La prefoliación de primordios en la yema terminal para la época de paralización del crecimiento, se corresponde de manera similar con los eventos de formación de yemas en otras especies; tal es el caso del durazno (Warriner et al., 1985), manzana (Pratt, 1984) y vid (Srinivasan y Mullins, 1981). Después de desarrolladas las estructuras preformadas, el meristemo apical continua normalmente formando nuevas estructuras de manera similar al caso del Quercus petrea (Fontaine et al., 1999).

FIGURA 2. Micrografía electrónica de barrido donde se muestra el inicio del desarrollo floral. (A) Primordios en estado de reposo, (B) brotación de la yema y (C) desarrollo de la yema foliar y floral.
La aparición de flores en la rama ortotrópica progresa de manera acrópeta (Figura 3A); mientras que sobre la rama plagiotrópica, la floración aparece desde el extremo apical hacia la base (Figura 3B). Una situación constractante se presenta en el caso de la floración del guayabo, la cual ocurre de manera lateral sobre la rama plagiotrópica. En este caso, la floración se presenta sólo en los nudos, 2, 3 y 4 de manera acrópeta, sobre el actual flujo de crecimiento (Añez y Bautista,1994).
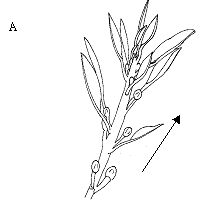
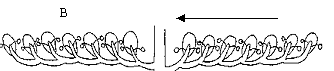
Figura 3. Posición ortotrópica de los ápices de crecimiento donde se iniciará la floración (A), Vista frontal del verticilio donde se ubicarán los brotes florales. (B) Detalle del inicio de la floración en uno de los ejes ortrotópicos Nota: La flecha indica la dirección de la floración.
Fenología floral. La fenología floral del níspero se estudió desde el momento en que se inició la brotación de la yema hasta la maduración estigmática y la antesis (Figura 4), la cual fue similar para las dos variedades y quedó definida para Santiago en cinco fases que se describen a continuación:
Fase 1. Para el momento de iniciarse la brotación de la yema, el primordio foliar se presentó como una estructura alargada y de mayor tamaño que la floral, la cual se presentó como una estructura redondeada y ubicada en la axila del anterior. Esta primera fase culmina cuando en el botón floral se comenzó a observar la formación del pedúnculo y el botón alcanzó 8 mm de diámetro, lo cual sucedió aproximadamente en 8 d desde inicio de la floración de la yema (DIB) (DIF) (DDF).
Fase 2. El pedúnculo se hace completamente visible y el verticilo más externo de los sépalos queda completamente formado y las suturas entre ellos quedan plenamente marcadas. Al corte longitudinal, el estilo ya ha iniciado su desarrollo y ocupa una pequeña parte de la cavidad floral (Figura 5A). Para este momento han transcurrido aproximadamente 28 DIF.
Fase 3. El botón floral completa su desarrollo. El pedúnculo tiene una longitud de 25 mm y se va tornando a una coloración rojiza, mientras que el diámetro del botón floral alcanza 10 mm . Hasta este momento han transcurrido aproximadamente 29 a 31 DIF.
Fase 4. Los sépalos externos comienzan a separarse por las suturas y los internos han alcanzado su tamaño final, mientras tanto el desarrollo del estilo y el estigma hace que esta estructura comience a sobresalir por la parte apical de la flor. El estigma, una vez afuera del botón floral, le aparece una sustancia viscosa transparente que lo recubre y permanece así durante aproximadamente 3 d, período durante el cual el estigma se considera receptivo (Figura 5B) y el estilo presenta una longitud de 7,40 mm y ecuatorialmente mide 2,36 mm . La base donde se inserta el ovario es un disco aplanado de 2,3 mm y presenta abundantes tricomas; el ovario, cuando esta completamente desarrollado, es de forma esferoidal y tiene un diámetro de 2,69 mm . Para este momento han transcurrido aproximadamente 42 DIF de la yema.
Fase 5. Durante esta fase el cáliz y la corola se abren y ocurre la dehiscencia de las anteras; este período tiene una duración de 5 DIF, después de los cuales se cierra y ya no vuelve abrir; mientras tanto el estigma se torna marrón o negruzco indicando que ha terminado el tiempo de receptividad. La antesis ocurre a los 46 días en promedio desde el inicio del desarrollo.

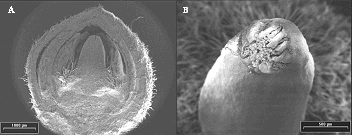
FIGURA 5. (A) Corte longitudinal del botón floral, (B) Comienzo de la receptividad estigmática.
Después de la antesis, las flores de níspero permanecen abiertas por un período de 72 h hasta que se fecundan o absisan y la duración de apertura, al parecer está controlada por los ritmos diarios de luz, temperatura y humedad (Essau,1977). El botón floral se desarrolla a lo largo de un período de 45 a 47 d, en ambos cultivares DIF hasta la antesis.
De acuerdo con Bailey y Bailey ( 1976); y estas observaciones, la flor del níspero es hermafrodita, completa, con perianto doble o diclamídeo y cáliz dialisépalo, biseriado, de tres sépalos en cada uno de los verticilos de posición imbricada, de color verde oscuro y más pubescente el externo que el interno el cual es verde claro. La corola es gamopétala, tubular cilíndrica, de color blanco-rosado, con simetría actinomorfa, con lóbulos generalmente en número igual a los sépalos. Los estambres son 6, libres entre sí, opuestos a la corola y su tamaño es tal que no alcanzan a sobresalir del perianto; por su adnación al perianto se consideran epipétalos. Los estaminoides en número de 6 están insertos en un simple verticilo.
El gineceo está conformado por un ovario súpero que tiene entre 3 a 12 lóculos, por lo que se le considera pluricarpelar. En la base del ovario se encuentran abundantes discos nectaríferos fusionados en forma anular y están cubiertos por abundantes tricomas que impiden ser visualizados.
El tiempo desde que emerge el botón floral para hacerse visible hasta la antesis, es variable en los diferentes frutales perennes y este es afectado por las condiciones climáticas; en la lechosa es de aproximadamente de 43 a 46 d (Storey, 1986), Chadha y Pandey (1982) realizaron un estudio similar y concluyeron que el desarrollo floral del guayabo ocurre a través de 8 fases, desde que la yema floral es visible hasta cuando ocurre la apertura floral.
CONCLUSIONES
-No se encontraron diferencias ni morfológicas, ni cronológicas apreciables en el desarrollo de la floración en ambas variedades.
-El primordio floral se desarrolla simultáneamente con el foliar en el meristemo apical de la rama.
-La floración progresa de manera acrópeta en el eje ortotrópico de la rama plagiotrópica.
-El botón floral se desarrolla a lo largo de un período aproximadamente de 46 DIF hasta la antesis, en ambas variedades.
BIBLIOGRAFÍA
1. Añez, M. y D. Bautista. 1994. Características de la floración y fructificación de cinco clones de guayaba (Psidium guajava L). Revista UNELLEZ de Ciencia y Tecnología 12(2):166-124. [ Links ]
2. Aubert, B. and P. Lossois. 1972. Consideration sur la phenologie des especes fruitires arbustivs. Fruts 27(4):269-286. [ Links ]
3. Aristiguieta, L. 1950. Frutas comestibles de Venezuela. Sociedad Botánica Venezolana de Ciencias Naturales. 13(76):57-104. [ Links ]
4. Avilán, L., F. Leal y D. Bautista. 1992. Manual de Fruticultura. Principios y Manejo de la Producción. Tomo 2. 2da Edición. Edición América. Caracas – Venezuela. pp 1.353-1.367. [ Links ]
5. Bailey, H. and E. Bailey. 1976. Hortus Third. Mcmillan Cormell University. Publishing. Company N.Y.600 p. [ Links ]
6. Bautista, D. y N. Meza. 2001. Caracterización del crecimiento del níspero desde plantación en campo hasta inició de floración. Proceeding of the Interamerican Society for Tropical Horticulture. 43:130-134. Lima – Perú. [ Links ]
7. Castillo, J. 1999. Universidad Central de Venezuela–Maracay. Microscopia Electrónica de Barrido. Guía Teórica. 30 p. [ Links ]
8. Chandha, K. and M. Pandey. 1982. Psidium guajava L. In: Handbook of flowering. M.H. Haley (Ed.) Boca de Raton, Florida, USA. Volumen V: 287-294. [ Links ]
9. Essau, K .1977. Anatomy of Seed Plants. New York. John Wiley and Sons. Inc. 420 p. [ Links ]
10. Fontaine, F., H. Chaar, F. Colon, C. Clement, M. Burrus and J. Druelle. 1999. Preformation and neoformation of growth units on 3-year-old seedlings of Quercus petraea. Canadian Journal of Botany 77:1.623-1.631. [ Links ]
11. Gilly, C. 1943. Studies in the sapotaceae. II. The sapodilla-níspero complex. Tropical Woods. 7(3):1-22. [ Links ]
12. González, L. and P. Feliciano. 1953. The blooming and fruiting habits of the sapota Philippine Agriculturist 27(7):384-398. [ Links ]
13. Knight, R. and C. Campbell. 1993. Pollination requirement for successful fruiting of tropical fruit species. Proceeding of the Interamerican Society for Tropical Horticulture. 37:167-170. [ Links ]
14. Krajewski, A. and E. Rabe. 1995. Citrus Flowering a Citrical Evaluation. J. Hort. Sci. 70 (3):357-374. [ Links ]
15. León, J. 1968. Fundamentos botánicos de los cultivos tropicales. Costa Rica. Instituto Interamericano Ciencias Agrícolas. 400 p. [ Links ]
16. Lindorf, H., L. Parisca y P. Rodríguez. 1985. Botánica. Clasificación, Estructura y Reproducción. Caracas. Edic. Bibl. UCV. 700 p. [ Links ]
17. Pratt, C. 1984. Apple flower and fruit: Morphology and anatomy. Horticultural Review 10:273-308. [ Links ]
18. Pennington, T. 1990. Flora-Neotropica Sapotaceae. Bronx, New York. The New York Botanical Garden. 384 p [ Links ]
19. Salazar-García, E., M. Lord and C. J. Lovatt. 1988. Inflorescence and flower development of the `Has´avocado (Persea americana Miller) during on and off crop year. J, Amer. Soc. Hort. Sci. 123(4):537-544. [ Links ]
20. Srinivasan, C. and M. Mullins. 1981. Physiology of flowering in the grapevine-A. Review Armerican Journal Enology Viticulture. Vol 32(1):47-63. [ Links ]
21. Storey, W. B. 1986. Carica papaya. C.R.C. Handbook of flowering. Vol IV. Edit. Abraham H. Halevy. C.D.R. Press. Inc. Boca Ratón. Florida. 600 p. [ Links ]
22. Warriner, C., J. Johnson and M. Smith. 1985. Cooperation of the initiation and development of 'Redhaven' peach flower in standard and meadow orchard tress. J. Amer. Soci. Hort. Sci.110(3):379-383. [ Links ]
 Citado por SciELO
Citado por SciELO  Accesos
Accesos
 Similares en
SciELO
Similares en
SciELO 


















