Saber
versión impresa ISSN 1315-0162
Saber vol.28 no.4 Cumaná dic. 2016
EFECTO DE L-CARNITINA SOBRE EL PESO, NIVELES DE TRIGLICÉRIDOS Y COLESTEROL DE RATONES SOMETIDOS A DIETAS NORMO E HIPERCALÓRICAS
LUIS OJEDA1,2, NIRZA NOGUERA-MACHADO1,3 , MARÍA CLARAMONTE4, LUIS PÉREZ-YBARRA3, DIANA HERNÁNDEZ1, INGMAR BALDA1, MOISÉS GONZÁLEZ1, GÉNESIS HERNÁNDEZ1
Universidad de Carabobo, Facultad de Ciencias de la Salud,
1 Instituto de Investigaciones Biomédicas “Francisco Javier Triana Alonso” - BIOMED-UC,
2 Escuela de Medicina, Sede Aragua, Departamento de Fisiología y Bioquímica,
3 Escuela de Bioanálisis, Sede Aragua, Departamento de Ciencias Básicas,
4 Escuela de Medicina, Sede Aragua, Departamento de Farmacología y Fisiopatología, Maracay, Venezuela E-mail: lmpy2005@gmail.com
RESUMEN
Se llevó a cabo un estudio experimental para determinar el efecto de la L-carnitina sobre el peso y los niveles de lípidos séricos (triglicéridos y colesterol total) en ratones NMRI. Para ello, se condujo un ensayo con arreglo factorial de tratamientos 22 bajo un diseño completamente aleatorizado. Los factores considerados fueron la dieta (normo e hipercalórica) y la incorporación o no de la L-carnitina como suplemento. Esta fue suministrada por vía oral a razón de 2 mg/día. Se evaluaron el peso [g], las concentraciones séricas de triglicéridos [mg·dL-1] y colesterol total [mg·dL-1]. Se aplicó el análisis de varianza y la prueba de comparaciones de medias de Tukey. No se encontraron diferencias significativas entre el tipo de dieta para el peso (F = 4,00; p = 0,0575) y colesterol (F = 0,09; p = 0,7722), ni para la administración de L-carnitina para el peso (F = 1,08; p = 0,3096) y colesterol (F = 0,13; p = 0,7255). En cuanto a los triglicéridos, se encontraron diferencias significativas entre el tipo de dieta (F = 12,73; p = 0,0016) e interacción significativa entre el tipo de dieta y la administración de L-carnitina (F = 5,95; p = 0,0228). Este efecto sugiere que el aminoácido combinado con una dieta baja en calorías podría considerarse como una alternativa para tratar casos de hipertrigliceridemias.
PALABRAS CLAVE: Aminoácido, dislipidemia, suplemento nutricional.
EFFECT OF L-CARNITINE ON WEIGHT, CHOLESTEROL AND TRIGLYCERIDES LEVELS OF MICE RECEIVING NORMAL AND HIGH CALORIC DIETS
ABSTRACT
An experimental study was conducted to determine the effect of L-carnitine on weight and serum lipid levels (triglycerides and total cholesterol) on NMRI mice. To do so, a factorial arrangement of treatments 22 under a completely randomized design was carried out. Factors considered were the diet (normal and hypercaloric) and the inclusion or not of the L-carnitine supplement. L-carnitine was orally administered at a rate of 2 mg/day. Weight [g], serum triglyceride concentrations [mg·dL-1] and total cholesterol [mg·dL-1] were evaluated. Analysis of variance test and Tukey mean comparisons were applied. Non significant differences were found between the type of diet for weight (F = 4.00; p = 0.0575), and cholesterol (F = 0.09; p = 0.7722), or for the administration of L-carnitine for the weight (F = 1.08; p = 0.3096), and cholesterol (F = 0.13; p = 0.7255). For triglycerides, significant differences between the type of diet (F = 12.73; p = 0.0016), and significant interaction between type of diet and the administration of L-carnitine (F = 5.95; p = 0.0228), were found. This effect suggests that the amino acid combined with a low calorie diet could be considered as an alternative to treat cases of hypertriglyceridemia.
KEY WORDS: Amino acid, dyslipidemia, nutritional supplement.
Recibido: abril 2016. Aprobado: mayo 2016. Versión final: septiembre 2016.
INTRODUCCIÓN
Las enfermedades cardiovasculares (ECV) son la principal causa de muerte en todo el mundo, afectando a ambos sexos por igual. En el año 2012, 17,5 millones de personas murieron por ECV, representando un 30% de todas las muertes registradas en el mundo (WHO 2014). Dentro de los factores de riesgo cardiovascular destaca la hiperlipemia, definida como la elevación del nivel plasmático de colesterol, triglicéridos o ambos (Jordá y Laguna 2012). Cuando un paciente padece de hiperlipemia, la primera recomendación que se le hace es que modifique sus hábitos alimentarios y realice actividades físicas, y si estos cambios no son suficientes para mejorar su condición, se recomienda el uso de algunos fármacos. La L-carnitina destaca dentro de los fármacos de origen natural usados con este fin, ya que se ha descrito que posee capacidad antioxidante, y su incorporación a la dieta podría servir como terapia complementaria en el tratamiento de enfermedades crónicas relacionadas con el estrés oxidativo celular (Cao et al. 2011, Mingorance et al. 2011).
La L-carnitina (ácido -hidroxi--N-trimetilamoniobutírico) es una amina cuaternaria, soluble en agua, anfótera, sintetizada de manera endógena por los animales a partir de dos aminoácidos esenciales: metionina y lisina (Stephens et al. 2007, Strijbis et al. 2010). Posee varias funciones asociadas con el metabolismo de los ácidos grasos: actúa en el transporte de ácidos grasos libres de cadena larga al interior de la mitocondria para llevar a cabo la β-oxidación (Belay et al. 2006), desempeña un papel importante en la cetogénesis por su aporte de acetil-CoA (Stephens et al. 2007), participa en la exportación de acilos no metabolizados hacia el exterior de la mitocondria (Schreiber 2005), entre otras funciones.
En el presente trabajo se planteó un estudio experimental con un modelo animal utilizando ratones NMRI, a fin de determinar el efecto de la L-carnitina sobre el peso y los niveles de lípidos séricos, triglicéridos y colesterol total en animales sanos sometidos a diferentes dietas, a fin de conocer cuál es el efecto del consumo de este aminoácido combinado con un cambio de dieta sobre dislipidemias asociadas con desórdenes alimentarios en pacientes sanos.
MATERIALES Y MÉTODOS
El estudio se realizó en el Instituto de Investigaciones Biomédicas “Francisco Javier Triana Alonso” (BIOMED-UC) de la Universidad de Carabobo, Maracay, Venezuela, con la aprobación del Comité de Bioética de dicha institución. El experimento fue conducido con un arreglo factorial de tratamientos 22 bajo un diseño completamente aleatorizado con siete repeticiones, siendo los animales las unidades experimentales. Se usaron ratones hembras sanas no consanguíneas de la raza NMRI de ocho semanas de edad, con un peso promedio de 35,2 ± 1,7 g, para un total inicial de 28 unidades experimentales, divididas en cuatro grupos que fueron sometidos a diferentes dietas.
El experimento se llevó a cabo en dos etapas, en la primera etapa a dos de los grupos se les suministró una dieta hipercalórica y a los otros dos una dieta normocalórica, durante un lapso de 30 días. Para la dieta normocalórica se usó alimento concentrado para ratones (ratarina), suministrado ad libitum y con libre acceso al agua. La dieta hipercalórica se formuló impregnando el alimento con mantequilla de maní y aceite vegetal de girasol, esta también se suministró ad libitum y con libre acceso al agua.
Finalizado este tiempo, se pasó a la segunda etapa donde a todos los grupos se les suministró una dieta normocalórica por 15 días más y se incorporó la L-carnitina de manera diferencial, definiendo así los grupos del estudio: animales con dieta hipercalórica previa sin L-carnitina, animales con dieta hipercalórica previa con L-carnitina, animales con dieta normocalórica previa sin L-carnitina y animales con dieta normocalórica previa con L-carnitina.
Para la incorporación de este aminoácido se usó la presentación líquida de Levo carnitina (Provicar-Elmor®) de concentración 0,1 g·mL-1y fue suministrada a los ratones a razón de 2 mg diarios por vía oral, calculados en función del peso del animal (Gómez-Campos et al. 2012).
Los ratones fueron pesados en jaulas individuales usando una balanza marca Ohaus. Para obtener el suero se realizaron punciones cardíacas usando la metodología propuesta por Giacopini et al. (2011). Las muestras fueron centrifugadas a 8.000 rpm durante 10 min en una centrifuga clínica marca Sartorius, para así separar el suero y almacenarlo a 4°C hasta su análisis. Para determinar los valores de triglicéridos y colesterol se usaron pruebas enzimáticas-colorimétricas comerciales. Las absorbancias fueron medidas en espectrofotómetro marca Beckman y las concentraciones se determinaron en función de una relación lineal elaborada con curva de estándares.
Análisis estadístico
Los resultados de las variables medidas (peso [g], concentración sérica de triglicéridos [mg·dL-1] y concentración sérica de colesterol total [mg·dL-1]) fueron evaluados mediante un análisis de varianza [ANOVA] y la prueba de comparaciones de medias de Tukey, previa comprobación de los supuestos de normalidad de los residuales y homocedasticidad o igualdad de varianzas de los tratamientos. Para verificar la normalidad de los residuales, se aplicó la prueba de Wilk-Shapiro y para la evaluación de la homocedasticidad, las pruebas de Bartlett y Levene. Cuando alguno de los supuestos no se cumplió, se realizaron transformaciones aplicando logaritmos decimales (base 10). Se trabajó al nivel de significación de 5% y 1%, por lo cual las diferencias fueron consideradas estadísticamente significativas cuando p ≤ 0,05 o p ≤ 0,01, respectivamente. Los datos se procesaron utilizando los programas estadísticos Minitab 16.0 y Statistix 9.0, ambos bajo ambiente Windows.
RESULTADOS
Un ratón del grupo que recibió dieta normocalórica y L-carnitina murió durante el estudio, por tal razón, el análisis de los resultados se realizó con base en 27 animales.
Si bien todas las variables respuesta presentaron residuales normalmente distribuidos según la prueba de Wilk-Shapiro, tanto para los datos originales como para los datos transformados a logaritmos, este no fue el caso para la característica de homocedasticidad. Las variables peso y colesterol total y sus trasformaciones a logaritmos presentaron homocedasticidad al 1% para las dos pruebas; así, el peso mostró homocedasticidad al 5% para la prueba de Bartlett pero no para la prueba de Levene y el colesterol total mostró el comportamiento inverso. Por otra parte, la variable triglicéridos presentó heterocedasticidad al 1% para ambas pruebas; sin embargo, dado que tal variable y su transformación a logaritmos presentaron residuales normalmente distribuidos, se consideró el resultado de la prueba de Bartlett para la transformación, por ser esta dependiente de la normalidad (Correa et al. 2006), y con ello se asumió la presencia de homocedasticidad al 1%. En consecuencia, en este trabajo se analizaron las variables peso y colesterol total con los datos originales y la variable triglicéridos mediante su transformación a logaritmos decimales (Tabla 1).
Tabla 1. Supuestos del ANOVA para las variables en estudio.


Concentración sérica de triglicéridos
El ANOVA mostró diferencias significativas entre los valores de triglicéridos para los grupos sometidos a distintas dietas (F = 12, 73; p = 0, 0016). Así el grupo de ratones que inicialmente recibió dieta hipercalórica mostró un valor más elevado (̅x= 293, 11 mg·dL-1) que el del grupo sometido a dieta normocalórica (̅x= 208, 38 mg·dL-1), no obstante, no hubo diferencias en esta variable al compararla entrelos grupos que recibieron o no L-carnitina (F = 1, 75; p = 0, 1894), siendo las medias x̅ = 270, 6mg·d L1 para los ratones que no recibieron L-carnitina y ̅ = 230, 64 mg·dL-1 para los que la recibieron (Tabla 2).
Tabla 2. Prueba de comparaciones múltiples de Tukey para la concentración sérica de triglicéridos [mg·dL-1] según los factores tipo de dieta y administración de L-carnitina.

Por otra parte, se encontró interacción significativa entre el tipo de dieta y la administración de L-carnitina (F = 5,95; p = 0,0228). Así, los ratones que recibieron L-carnitina presentaron medias homogéneas para ambas dietas, mientras que los ratones que no recibieron
L-carnitina presentaron una concentración mayor de triglicéridos en el grupo sometido inicialmente a la dieta hipercalórica (cambio de dieta) (Fig. 1).
Concentración sérica de colesterol total
El ANOVA no mostró diferencias significativas para el tipo de dieta (F = 0,09; p = 0,7722), ni para la administración de L-carnitina (F = 0,13; p = 0,7255), los resultados de las pruebas de comparaciones de Tukey confirmaron la ausencia de diferencias entre las medias (Tabla 3).
Figura 1. Gráfica de la interacción del tipo de dieta y la administración de L-carnitina para la concentración sérica de triglicéridos [mg·dL-1]. Los valores entre paréntesis corresponden a las medias aritméticas calculadas sobre los valores sin transformar a logaritmos decimales.

Por otra parte, se encontró interacción significativa entre el tipo de dieta y la administración de L-carnitina (F = 7,46; p = 0,0119). Así, la aplicación de L-carnitina ocasionó una disminución en los niveles de colesterol total en aquellos ratones que recibieron inicialmente dieta hipercalórica, siendo este comportamiento contrario en los ratones con dieta normocalórica, en los cuales los niveles tendieron a aumentar con la administración de L-carnitina (Fig. 2).
El ANOVA no mostró diferencias significativas para el tipo de dieta (F = 4,00; p = 0,0575), además, no se encontraron diferencias significativas para la administración de L-carnitina (F = 1,08; p = 0,3096), los resultados de las pruebas de comparaciones de Tukey confirmaron la ausencia de diferencias entre las medias (Tabla 4).
Por otra parte, no se encontró interacción significativa entre el tipo de dieta y la administración de L-carnitina (F = 0,51; p = 0,4843); eso indica que el comportamiento del peso de los animales no se vio afectado por la administración de L-carnitina en ninguna de las dos dietas (Fig. 3).
Figura 2. Gráfica de la interacción del tipo de dieta y la administración de L-carnitina para la concentración sérica de colesterol total [mg·dL-1].

Peso 
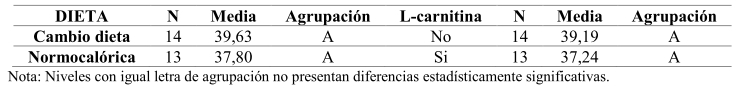
El ANOVA no mostró diferencias significativas para el tipo de dieta (F = 4,00; p = 0,0575), además, no se encontraron diferencias significativas para la administración de L-carnitina (F = 1,08; p = 0,3096), los resultados de las pruebas de comparaciones de Tukey confirmaron la ausencia de diferencias entre las medias (Tabla 4).
Por otra parte, no se encontró interacción significativa entre el tipo de dieta y la administración de L-carnitina (F = 0,51; p = 0,4843); eso indica que el comportamiento del peso de los animales no se vio afectado por la administración de L-carnitina en ninguna de las dos dietas (Fig. 3).
Figura 3. Gráfica de la interacción del tipo de dieta y la administración de L-carnitina para el peso[g].


Tabla 3. Prueba de comparaciones múltiples de Tukey para la concentración sérica de colesterol total [mg·dL-1] según los factores tipo de dieta y administración de L-carnitina.

Tabla 4. Prueba de comparaciones múltiples de Tukey para el peso [g] según los factores tipo de dieta y administración de L-carnitina.

DISCUSIÓN
La disminución de los niveles de triglicéridos observados en esta investigación para los ratones fue similar a la reportada por Miguel (2009) en un estudio con ratas hipertensas que recibieron el aminoácido. Este hecho podría asociarse con el fenómeno conocido del aumento de movilidad de los ácidos grasos de los depósitos corporales cuando se utiliza como suplemento alimentario la L-carnitina (Brass y Hiatt 1998).
En lo que respecta al colesterol total no hubo diferencias significativas entre los tratamientos evaluados. Sin embargo, la Figura 2 demuestra que el suplemento dietario con L-carnitina junto al cambio calórico de la dieta originaron un nivel de colesterol menor si se lo compara con el valor obtenido en el grupo de animales que no recibió el aminoácido. Aun cuando debe considerarse que el tiempo de estudio corto constituye una limitación para el alcance de un resultado más contundente, esta observación concuerda con la registrada previamente por otros autores que emplearon como modelo animal ratas diabéticas (İrat et al. 2003) o ratas hipertensas (Miguel 2009).
Así también, el cambio poco significativo observado en el peso de los animales alimentados o no con L-carnitina podría deberse al corto tiempo de este estudio, pero no debe descartarse la posibilidad de su asociación con el efecto supresor del aminoácido sobre la actividad total de la lipasa sensible a hormona (LPL) en el músculo esquelético, tal como ha sido descrito por Xu et al. (2003). Al disminuir la actividad de la LPL, aumenta la hidrólisis de lipoproteínas de muy baja densidad (VLDL), lo que podría reducir la deposición de grasa en la zona subcutánea (Griffin y Whitehead 1982). Si bien los pesos no presentaron diferencias significativas, los animales que recibieron el cambio de dieta y L-carnitina mostraron un ligero aumento de peso (Fig. 3) y una disminución de los valores de triglicéridos (Fig. 1), lo que sugiere que el suplemento facilitó la oxidación de los ácidos grasos en el músculo, favoreciendo que este tejido utilizara los aminoácidos de la dieta para aumentar su masa muscular. Resultados semejantes fueron descritos por Xu et al. (2003), quienes observaron disminución de grasa subcutánea y aumento en los músculos de aves de corral.
En su conjunto, estos resultados, aun cuando no son concluyentes, encuentran sustento en los hallazgos previos demostrados en otros modelos animales, demostrando su importancia en el esclarecimiento del posible efecto beneficioso del suplemento alimentario con L-carnitina en humanos que sufren alteraciones metabólicas del tipo de las dislipidemias en asociación con el consumo de dietas hipercalóricas.
REFERENCIAS BIBLIOGRÁFICAS
1.BELAY B, ESTEBAN-CRUCIANI N, WALSH CA, KASHEL FJ. 2006. The use of levo-carnitine in children with renal disease: a review and a call for future studies. Pediatri. Nephrol. 21(3):308-317.
[ Links ]
2.BRASS EP, HIATT WR. 1998. The role of carnitine supplementation during exercise in man and individuals with special needs. J. Am. Coll. Nutr. 17(3):207-215. [ Links ]
3.CAO Y, QU HJ, LI P, WANG CB, WANG LX, HAN ZW. 2011. Single dose administration of L-carnitine improves antioxidant activities in health subjects. Tohoku J. Exp. Med. 224(3):209-213. [ Links ]
4.CORREA JC, IRAL R, ROJAS L. 2006. Estudio de potencia de pruebas de homogeneidad de varianza. Rev. Colomb. Estad. 20(1):57-76.
[ Links ]
5.GIACOPINI MI, GUERRERO O, MOYA M, BOSCH V. 2011. Estudio comparativo del consumo de aceite de oliva virgen o seje sobre el perfil lipídico y la resistencia a la oxidación de las lipoproteínas de alta densidad (HDL) del plasma de rata. Arch. Latin. Nutr. 61(2):143-148.
[ Links ]
6.GÓMEZ-CAMPOS R, DE ARRUDA M, PINHEROS-RAMOS F, COSSIO-BOLAÑOS MA. 2012. Efecto de la suplementación de L-carnitina sobre el nivel de fatiga muscular del gastrocnemio de ratas entrenadas y sedentarias. Rev. Bras. Cineantropom. Desempenho Hum. 14(3):324-332. [ Links ]
7.GRIFFIN HD, WHITEHEAD CC. 1982. Plasma lipoprotein concentration as an indicator of fatness in broilers: development and use of a simple assay for plasma very low density lipoproteins. Br. Poult. Sci. 23(4):307-313.
[ Links ]
8.İRAT AM, AKTAN F, OZANSOY G. 2003. Effects of L-carnitine treatment on oxidant/antioxidant state and vascular reactivity of streptozotocin-diabetic rat aorta. J. Pharm. Pharmacol. 55(10):1389-1395. [ Links ]
9.JORDÁ M, LAGUNA J. 2012. Tratamiento farmacológico de las dislipidemias. Farmacología en Nutrición. Editorial Panamericana, México, pp.87-90. [ Links ]
10.MIGUEL JL. 2009. Efecto cardioprotector de la L-carnitina en las ratas hipertensas. Sevilla, España: Universidad de Sevilla, Departamento de Fisiología y Zoología [Disertación Doctorado] pp. 302. Disponible en línea: http://www.tesisenred.net/handle/10803/113784. (Acceso: 20.08.2014).
[ Links ]
11.MINGORANCE C, RODRÍGUEZ-RODRÍGUEZ R, JUSTO ML, ÁLVAREZ DE SOTOMAYOR M, HERRERA MD. 2011. Critical update for the clinical use of L-carnitine analogs in cardiometabolic disorders. Vasc. Health Risk Manag. 7:169-176.
[ Links ]
12.SCHREIBER B. 2005. Levocarnitine and dialysis: a review. Nutr. Clin. Pract. 20(2):218-243. [ Links ]
13.STEPHENS FB, CONSTANTIN-TEODOSIU D, GREENHAFF PL. 2007. New insights concerning the role of carnitine in the regulation of fuel metabolism in skeletal muscle. J. Physiol. 581(2):431-444. [ Links ]
14.STRIJBIS K, VAZ FM, DISTEL B. 2010. Enzymology of the carnitine biosynthesis pathway. IUBMB Life. 62(5):357-362.
[ Links ]
15.WHO (WORLD HEALTH ORGANIZATION). 2014. Global status report on noncommunicable diseases 2014. Geneva. Disponible en línea en: https://cspinet.org/new/pdf/who-global-status-report-on-ncds-2014__1_.pdf. (Acceso 09.07.2014).
[ Links ]
16.XU ZR, WANG MQ, MAO HX, ZHAN XA, HU CH. 2003. Effects of l-carnitine on growth performance, carcass composition, and metabolism of lipids in male broilers. Poult. Sci. 82(3):408-413. [ Links ]












 uBio
uBio 
