Services on Demand
Journal
Article
Indicators
-
 Cited by SciELO
Cited by SciELO -
 Access statistics
Access statistics
Related links
-
 Similars in
SciELO
Similars in
SciELO
Share
Acta Odontológica Venezolana
Print version ISSN 0001-6365
Acta odontol. venez vol.43 no.3 Caracas 2005
Expresión de laminina en la microvasculatura de lesiones premalignas y malignas de la mucosa bucal.
Floribel Cedeño B1. Paola Tonino2
1Profesora Asistente. Cátedra de Histología. Facultad de Odontología, Universidad Central de Venezuela cedenof@camelot.rect.ucv.ve
2
Resumen
Las lesiones premalignas y malignas de la mucosa bucal representan un modelo para el estudio de la progresión tumoral. La degradación de los componentes de la matriz extracelular y de la membrana basal durante los procesos neoplásicos puede activar moléculas que actúan como promotoras o supresoras de la angiogénesis tumoral. La laminina es la glicoproteína estructural más abundante en la membrana basal, la cual esta constituida por tres subunidades polipeptídicas α, β, y γ, unidas por puentes disulfuro en una estructura cruciforme. La laminina en la membrana basal vascular cumple un papel crucial en la progresión del cáncer. En el presente estudio se determinó la expresión de laminina en la membrana basal vascular, en biopsias con diferentes grados de displasia y carcinomas bucales. Los resultados revelaron un aumento en la expresión de laminina en las células epiteliales y tumorales, así como también, alteraciones morfológicas en los vasos sanguíneos con la progresión tumoral. Estos hallazgos sugieren cambios a nivel estructural y funcional que pueden estar relacionados con los procesos de angiogénesis, invasión y metástasis.
Palabras claves: laminina, vasos sanguíneos, mucosa bucal, progresión tumoral, inmunohistoquímica.
Abstract
Premalignant and malignant lesions in the oral mucosa represent a model for the study of tumoral progression. The degradation of the extracellular matrix and basement membrane components during neoplastic process can activate molecules that act as promoters or suppressors of tumoral angiogenesis. Laminin is the most abundant structural glycoprotein of basement membrane, composed by three polypeptides subunits α, β, and γ, disulfide-bonded in a cruciform structure. Laminin in the vascular basement membrane play a crucial role in the cancer progression. In the present study we determined the laminin expression in the vascular basement membrane, in biopsies with differents grade of dysplasia and squamous carcinomas. Results revealed an increase in the expression of laminin in the epithelial and tumoral cells, as well as morphologic alterations in the blood vessels with the tumoral progression. These findings suggest changes at structural and functional level that could be related with the process of angiogenesis, invasion and metastasis.
Key words: laminin, blood vessels, oral mucosa, tumor, progresión,immunohistochemistry
Recibido para arbitraje: 16/04/2004
Introducción
El crecimiento de las neoplasias superior a 1 ó 2 mm requiere del riego sanguíneo, el cual aporta el oxígeno, los nutrientes y los factores de crecimiento necesarios para la proliferación de las células tumorales, y constituye a su vez una ruta para la remoción de los catabolitos producidos por estas células. Esta hipótesis originalmente formulada por Judah Folkman1, ha impulsado dramáticamente el estudio de la angiogénesis en el área oncológica en las últimas tres décadas.
La angiogénesis consiste en la formación de nuevos vasos sanguíneos a partir de las vénulas post-capilares preexistentes. La angiogénesis es un proceso complejo y dinámico que involucra células endoteliales, tumorales, pericitos, los factores u hormonas paracrinas, los receptores, las quinasas, los traductores de señales y la matriz extracelular, así como también, factores proangiogénicos y la reorganización de nuevas estructuras tubulares2, 3.
La degradación de la matriz extracelular y la membrana basal durante los procesos neoplásicos activa moléculas y fragmentos que promueven la angiogenesis, el crecimiento y la invasión tumoral4.
La membrana basal constituye un componente de la matriz extracelular que mantiene separado el tejido epitelial de los tejidos subyacentes, define las superficies epiteliales externas e internas y la estructura de los vasos sanguíneos que constituyen un sustrato para la unión y la cohesión celular, además de estar involucrada en los procesos de diferenciación celular5, 6.
La membrana basal vascular es un importante componente estructural y funcional de los vasos sanguíneos que cumple un papel crucial en la progresión del cáncer7.
Los componentes de la membrana basal incluyen proteínas y macromoléculas, tales como, la laminina, el colágeno IV, proteoglicanos, nidogeno/entactina y otras proteínas7, 8. La laminina es la glicoproteína más abundante en la membrana basal, la cual esta constituída por tres subunidades polipeptídicas α, β, y γ, unidas por puentes disulfuro en una estructura cruciforme5, 6. Existen varias isoformas de laminina y hasta el presente se han identificado cinco subunidades α, tres β y tres γ, las cuales se ensamblan en doce isoformas distintas8.
El colágeno tipo IV y la laminina pueden ejercer una regulación positiva y negativa de la angiogénesis en dependencia de su ensamblaje e integridad estructural7, 8. Los tumores producen componentes de la membrana basal que promueven angiogénesis y se ha sugerido que las células tumorales y las células endoteliales normales responden de forma distinta a señales de la membrana basal7.
En la cavidad bucal se ha descrito un incremento en la densidad vascular y la angiogénesis durante la actividad proliferativa y la transformación de las células epiteliales9-11. Existen evidencias del patrón de distribución de laminina en la membrana basal próxima a las células tumorales en el carcinoma espinocelular bucal12. Sin embargo, hasta el presente la expresión de laminina en la membrana basal microvascular en la progresión del cáncer bucal es muy poco conocida. Por ello, el objetivo del presente estudio fue determinar la expresión de laminina en la membrana basal de los vasos sanguíneos, en lesiones premalignas y malignas de la mucosa bucal y su relación con la progresión tumoral.
Materiales y métodos
Un total de 23 biopsias fueron obtenidas del Archivo del Laboratorio de Histopatología Pedro J. Tinoco S. de la Facultad de Odontología de la Universidad Central de Venezuela. De acuerdo al diagnóstico histopatológico fueron distribuidas en los siguientes grupos: displasia leve (n= 5), displasia moderada (n= 6), displasia severa (n= 6) y carcinoma espinocelular (n= 6). La edad promedio de estos pacientes fue de 58 años, se incluyeron pacientes de ambos sexos y sólo lesiones en mucosa de revestimiento, tales como, paladar blando, mucosa alveolar y carrillo. En ningún caso los pacientes recibieron tratamiento previo, ni se confirmó la presencia de metástasis. Las características clínico-histopatológicas se muestran en el Tabla 1.
Tabla N° 1
Características clínicas-histopatológicas de las lesiones premalignas
| Tipo de lesión | Edad años | Sexo F:M | Sitio de la muestra | ||
| RA | PA | CA | |||
Displasia Leve | 48-70 54.6 | 1:4 | 5 | | |
Displasia moderada | 31-79 57.5 | 5:1 | 4 | 2 | |
Displasia severa | 49-75 63 | 4:2 | 4 | 1 | 1 |
| Carcinomas Espinocelular | 23-71 57.8 | 2:4 | 2 | 2 | 2 |
RA: reborde alveolar; PA: paladar; CA: carrillo.
Las secciones de 4 mm se procesaron mediante la técnica modificada de la inmunoperoxidasa indirecta13 descrita previamente por Tonino y col.11,14. Brevemente, las secciones fueron desparafinadas y rehidratadas. Posterior al bloqueo de la peroxidasa endógena se realizaron las incubaciones con la soluciones del kit LSAB universal (labelled streptavidin biotin peroxidase) de tres componentes (Dako CA, USA). Se empleó el anticuerpo primario policlonal anti-laminina de humano (Dako, CA, USA), dilución 1:50 en tampón fosfato salino (PBS, pH 7,4, 0,1M). La inmunoreacción se detectó con el cromógeno 3-amino-9-etil carbazol (Sigma). El contraste y el montaje se realizó con hematoxilina de Meyer y gelatina glicerinada, respectivamente. Los registros fotográficos se efectuaron en un microscopio Zeiss con cámara adaptable MC63A.
La inmunoreactividad positiva de las células epiteliales y tumorales a la laminina se determinó como leve, moderada e intensa, así como el patrón de distribución en la membrana basal de los vasos sanguíneos se definió como contínua y discontínua.
Resultados
La expresión de laminina en las células epiteliales (Fig. 1,2) y tumorales (Fig. 3, 4) de las distintas patologías estudiadas fue negativo o leve en las displasias leve y moderada, mientras que en las displasias severa y en los carcinomas espinocelulares se observó un patrón granular de la inmunotinción de moderada a intensa. Adicionalmente, se observaron depósitos irregulares con inmunoreactividad positiva a laminina en la matriz extracelular de las displasias severas y carcinomas. Estos resultados sugieren un incremento en la expresión de laminina con la progresión tumoral.
Fig. 1. Expresión de laminina en una lesión de displasia leve. Barra= 10 mm.
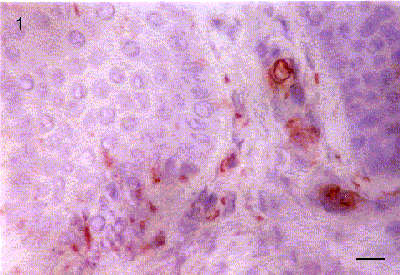
Fig. 2. Expresión de laminina en una lesión de displasia moderada. Barra= 10 mm.

Fig. 3. Expresión de laminina en una lesión de displasia severa. Notese la intensa inmunorreacción en los vasos sanguíneos y células epiteliales. Barra= 10 mm.

En general, la membrana basal de los vasos sanguíneos se evidenció con una inmunoreacción positiva a la laminina. En las displasias leve el 80%, en las displasias moderada el 67% y en las displasias severa el 33 % de los casos, mostraron una membrana basal de forma continua y homogénea (Fig. 1-3), a diferencia de los carcinomas espinocelulares, los cuáles mostraron un patrón de distribución de laminina difuso y discontínuo (Fig. 4). Un resumen de los resultados de la distribución de laminina en las células y la membrana basal vascular de las patologías estudiadas se muestra en la Tabla 2.
Fig. 4. Expresión de laminina con una inmunorrecación intensa en un carcinoma espinocelular. Barra= 10 mm.

Tabla N°: 2
Distribución de la expresión de laminina en lesiones premalignas y malignas de la mucvosa bucal.
N° de displasia leve Dispasia moderada Displasia severa carcinomas
la muestra cel MB/VS CEL MB/VS cel MB/VS cel MB/VS
1 + C + C ++ D ++
2 - C - D ++ C +++
3 + D - D ++ C ++
4 - C + C ++ D +++
5 - C - C ++ D ++
6 - C +++ D +++
Cel. Células epiteliales y/o tumorales. Expresión: negativa(-), Leve (+), Moderada (++), Intensa (+++).
MB/VS: membrana basal de los vasos sanguíneos. Continua (C) Discontínua o difusa (D).
Discusión
En el presente estudio se encontraron distintos grados de alteración en la expresión de laminina, en la membrana basal de los vasos sanguíneos con la progresión de displasias a carcinomas bucales, similar a lo descrito en un estudio in vitro sobre la transición de hiperplasia a neoplasia en islotes pancreáticos en un modelo murino, que demuestra la alteración de la expresión de laminina en los vasos sanguíneos, con un patrón homogéneo y variaciones morfológicas con la progresión tumoral 15. Los cambios estructurales en la membrana basal se han relacionado con la angiogenesis16. Asimismo, se conoce que la vasculatura tumoral presenta una membrana basal irregular, conformada por cantidades variables de laminina, fibronectina y colágeno, en dependencia del grado de maduración de los vasos sanguíneos17. Por otra parte, se ha sugerido que la laminina-1 se encuentra asociada a las etapas tempranas de la angiogénesis, en tanto que el colágeno tipo IV y el perlecano aparecen más tardíamente en la neoformación vascular18.
En este estudio se encontró un incremento en la positividad de la expresión de laminina en las células epiteliales, así como también en la matriz extracelular con la progresión tumoral. La expresión intracelular de distintas isoformas de laminina y sus subunidades se ha observado en diversos tipos tumorales19,20. La subunidad γ2 de la laminina-5 se ha relacionado con la progresión tumoral y un mal pronóstico en el carcinoma esofágico20, de lengua21 y laringeo22. Adicionalmente, se ha determinado que la laminina-1 presenta sitios activos en sus subunidades α-1 y γ-1 (peptidos SIKVAV, VAYI, YVRL) que promueven la angiogénesis, el crecimiento y la malignidad5,8. Tales sitios activos pueden ser liberados a partir de la degradación de la matriz extracelular por la acción de las metaloproteinasas de la matriz extracelular, el cual constituye uno de los primeros pasos que ocurren durante la angiogénesis y la invasión8,23.
En conclusión, la expresión de laminina en lesiones premalignas y malignas de la mucosa bucal permitió evidenciar cambios a nivel estructural y funcional que podrían estar relacionados con los procesos de angiogénesis, invasión y metástasis durante la progresión tumoral.
Agradecimientos
Este trabajo fue financiado por el Consejo de Desarrollo Científico y Humanístico C.D.C.H. de la Universidad Central de Venezuela U.C.V. (N° 03.201.2003).
Bibliografía
1.Folkman J.(1990). What is the evidence that tumor are angiogenesis depedent? J. N. C. I., 82:4-6.
2.Folkman J. (1984). What is the role of endothelial cell in angiogenesis? Lab. Invest., 51: 601-604.
3.Fox S. B., Gatter K. C. and Harris A.L. (1996). Tumor angiogenesis. J. Pathol., 179: 232-237.
4.Liaw L. and Crawford H.C. (1999). Functions of the extracellular matrix and matrix degrading proteases during tumor progression. Braz J. Med. Biol. Res., 32:805-812.
5.Grant D., Kibbey M., Kinsella J., Cid M. and Kleinman H. (1994). The role of basement membrane in angiogenesis and tumor growth. Path. Res. Pract., 190: 845-63.
6.Geneser F. (2000). Histología sobre Bases Biomoleculares. Tercera Edición. Editorial Médica Panamericana. Buenos Aires.
7.Kalluri R. (2003). Basement membrane structure, assembly and role in tumour angiogénesis. Nature Rev., 3:422-433.
8.Engbring J. A. and Kleinman H. K. (2003). The basement membrane matrix in malignancy. J. Pathol., 200: 465-470.
9.Tipoe G., Jin Y. and White F.H. (1996). The relationship between vascularity and cell proliferation in human normal and pathological lesions of the oral cheek epithelium. Oral Oncol. Eur. J. Cancer, 32B: 24-31.
10.Pazouki S., Chisholm D.M., Adi M.M., Carmichael G., Farquharson M., Ogden, G.R., Schor S.L. and Schor A.M. (1997). The association between tumour progression and vascularity in the oral mucosa. J. Pathol., 183: 39-43.
11.Cedeño F. y Tonino P. (2003). Angiogénesis en lesiones premalignas y malignas de la mucosa bucal. Acta Odont. Venez., en prensa.
12.Kumagai S., Kojima S., Imai K., Nakagawa K., Yamamoto G., Kaswahara E. and Nakanishi I. (1994). Immunohistology distribution of basement membrane in oral squamous cell carcinoma. Head Neck, 16:51-57.
13.Hsu S.M., Raine L. and Fanger H. (1981). Use of avidin-biotin peroxidase complex (ABC) in immunoperoxidase techniques: A comparison between ABC and unlabeled antibody (PAP) procedures. J. Histochem. Cytochem., 29: 577-580.
14.Tonino P., Finol H.J., Hidalgo C. y Sosa L. (2001). Angiogenesis y proliferación en tumores malignos del tracto gastrointestinal del humano. Acta Biol. Venez., 21: 1-8.
15.Folkman J., Watson K., Ingber D. and Hanahan D. (1989). Induction of angiogenesis during the transition from hyperplasia to neoplasia. Nature, 339: 58-61.
16.Baluk P., Morikawa S., Haskell A., Mancuso M. and McDonald M.D. (2003). Abnormalities of basement membrane on blood vessels and endothelial sprouts in tumors. Am. J. Pathol., 163: 1801-1815.
17.Kakolyris S., Giatromanolaki A., Koukourakis M., Leigh I.M., Georgoulias V., Kanavaros P., Sivridis E., Gatter K.C. and Harris A.L. (1999). Assessment of vascular maturation in non-small cell lung cancer using a novel basement membrane component, LH39: Correlation with p53 and angiogenic factor expression. Cancer Res., 59(1): 5602-5607.
18.Hagedorn H.G. and Nerlich A.G. (2000). Microvessel density and endothelial basement membrane composition in laryngeal squamous cell carcinomas. Acta Otolaryngol., 120: 891-898.
19.Patarroyo M., Tryggvason K. and Virtanen I. (2002). Laminin isoforms in tumor invasion, angiogenesis and metastasis. Semin. Cancer Biol.,12: 197-207.
20.Yamamoto H., Itoh F., Iku S., Hosokawa M. and Imai K. (2001). Expression of the γ2 chain of laminin-5 at the invasive front is associated with reccurrence and poor prognosis in human esophageal squamous cell carcinoma. Clin. Cancer Res., 7:896-900.
21.Ono Y., Nakanishi Y., Ino Y., Niki T., Yamada T. and Yoshima K. (1999). Clinicopathologic significance of laminin5 gamma2 chain expresion in squamous cell carcinoma of the tongue. Cancer, 85: 2315-2321.
22.Noderman S., Kronenett V., Aver G. and Hogmo A. (2001). Laminin5 as a predictor of invasiveness in cancer in situ lesion of the larynx. Anticancer Res., 21: 509-512 [ Links ]
23.Cox G. and O´Byrne, K. J. (2001) Matrix metalloproteinases and cancer. Anticancer Res., 21: 4207-4220.