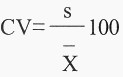Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Agronomía Tropical
versión impresa ISSN 0002-192X
Agronomía Trop. v.52 n.4 Maracay oct. 2002
NOTA
Determinación conductimétrica de cloruros en extractos de saturación de suelos
Armando Carrasquero D.1 y Pedro Castillo2
1Profesor. Universidad Pedagógica Experimental Libertador
Departamento de Química Apdo. 1017. Las Acacias
Maracay 2101, estado Aragua. Venezuela
2Profesor. Universidad Central de Venezuela
Facultad de Agronomía. Instituto de Edafología
Maracay 2101, estado Aragua. Venezuela
RESUMEN
Fueron comparados dos métodos para la detección del punto final en la determinación argentométrica del ión cloruro en extractos de saturación de suelos: a) la detección visual a través de la formación del precipitado rojo de cromato de plata y, b) la titulación conductimétrica. Para tal fin se utilizaron muestras de suelos provenientes de las cercanías al Lago de Valencia, en el estado Carabobo, Venezuela. Al analizar extractos de saturación incoloros por ambos métodos, los resultados no mostraron diferencias estadísticamente significativas cuando fueron comparados a través de una recta de regresión. En los extractos que presentaron una fuerte coloración oscura, no fue posible la aplicación del método visual para la detección del punto de equivalencia. Los porcentajes de recuperación en los extractos coloreados fueron superiores al 95% al ser analizados por la técnica conductimétrica. Se propuso la valoración conductimétrica para aquellos extractos donde la fuerte coloración oscura impidiera el uso del cromato de potasio como indicador.
Palabras Clave: Extractos de saturación; Ión cloruro; valoración; conductimetría; cromato de potasio.
SUMMARY
Two methods for end point detection in argentometric determination of chloride ion in soil saturation extracts were compared: 1) visual detection of red silver chromate precipitate and 2) conductimetric titration. No significant differences were found when both methods were applied to clear extracts and results compared using linear regression. However, the visual method could not be employed for unclear extracts; in this case it was necessary to determine recovery after applying a known amount of chloride as NaCl. Conductimetric titration leads to a recovery rate higher than 95%. It was concluded that conductometric analysis may be used for those extracts where potassium chromate cannot be employed.
Key Words: Saturation extracts; chloride ion; titration; conductmetric determination; potassium chromate.
RECIBIDO: Octubre 04, 2001
INTRODUCCIÓN
El análisis de cloruros en extractos de saturación de suelos es un procedimiento rutinario y muy importante en la caracterización de un suelo con diversos fines. La valoración de precipitación por el método de Mohr (Jander, 1961), en la que se usa nitrato de plata como valorante y cromato de potasio como indicador, ha sido el procedimiento más empleado ya que es sencillo, de una elevada precisión y exactitud. Sin embargo, como cualquier método que se basa en la detección de un color para la identificación del punto final, lo cual se ve afectado negativamente cuando en la solución hay sustancia coloreadas.
Este es el caso de algunos extractos de saturación que presentan coloraciones desde marrón hasta negro oscuro, que enmascaran el color rojo del cromato de plata, de tal manera que no es posible su uso en la valoración. Estas coloraciones pueden estar asociadas a la presencia de materia orgánica coloidal difícilmente de separar por métodos sencillos de filtración y su coagulación implicaría la modificación del pH del extracto y con ello se alterarían los equilibrios iónicos de la solución y a su vez las concentraciones de las sustancias de interés. En ese sentido, es importante disponer de una técnica de titulación que no se vea afectada por la presencia de estas interferencias y produzca resultados de precisión y exactitud equivalentes a los obtenidos con el método de Mohr.
La conductimetría permite seguir el curso de la titulación por los cambios que produce en la conductividad eléctrica (CE) de la solución la adición del titulante. En el caso del análisis de cloruro, la reacción que ocurre antes del punto de equivalencia es la siguiente:
Cl- +AgNO3 AgCl(s)
Los cambios en las concentraciones de las especies iónicas disueltas afectan la CE de la solución, por lo que luego de alcanzar el punto de equivalencia, el exceso de iones plata y nitrato van a provocar un aumento de la CE de la solución y de esta forma se apreciará un cambio en la gráfica de CE contra volumen de titulante que podría ser empleado en la detección del punto final. Esta técnica no se ve afectada por la presencia de sustancias coloreadas en el medio por lo que puede ser aplicada a extractos de saturación incoloros o coloreados.
En este trabajo se comparan los resultados que se obtienen en el análisis de Cl- en extractos de saturación de suelos, se evalúa asimismo la precisión, exactitud y la presencia de errores sistemáticos.
MATERIALES Y MÉTODOS
Las muestras de suelos utilizadas, identificadas con números del 1 al 6, fueron tomadas en zonas cercanas al Lago de Valencia, estado Carabobo, donde se descargan aguas residuales con elevados contenidos de sales sódicas. Los extractos de saturación fueron preparados de acuerdo al procedimiento señalado en el Agriculture Handbook 60 (USDA, 1950).
Se preparó una solución de nitrato de plata 0,01 N, disolviendo 1.699 g de la sal en 1 l de agua destilada. Esta solución fue valorada con una solución patrón de cloruro de sodio 0,01 N, empleando como indicador cromato de potasio al 5%. El indicador fue preparado disolviendo 5 g de KCrO4 en 50 ml de agua destilada. Se agregó gota a gota una solución de AgNO3 1N hasta la aparición de un precipitado rojo de cromato de plata. Se filtró en un balón de 100 ml, llegándose a completar hasta la marca con agua destilada.
Para la valoración del ión Cl- en los extractos de saturación de suelos se tomaron por triplicado alícuotas de 10 ml de cada extracto de saturación, colocándose en vasos de precipitado de 50 ml. Tres gotas del indicador fueron agregados a cada alícuota, para titularse con la solución de AgNO3 hasta la aparición del precipitado rojo de cromato de plata, este procedimiento fue denominado método 1.
Otra serie de alícuotas de igual volumen fueron tituladas con la misma solución de nitrato de plata, midiendo la CE de los extractos, luego de la adición del titulante (método 2). Se graficaron las CE en función al volumen de titulante y el punto final fue identificado como el volumen requerido para provocar un cambio en la pendiente de las rectas.
En cuanto a la determinación del porcentaje de recuperación tres alícuotas de 5 ml de los extractos de saturación M7 y M8 fueron colocadas en vasos de precipitado de 50 ml. Se agregaron sucesivamente 0,5 ml; 1,0 ml y 1,5 ml de la solución de NaCl 0,01 M. Posteriormente se colocó suficiente agua destilada hasta completar 10 ml. Las soluciones fueron tituladas con nitrato de plata, midiendo la CE luego de la adición del titulante.
En todos los casos las conductividades medidas fueron corregidas por el efecto de la dilución, multiplicando por el factor (V+v)/V, donde V es el volumen inicial y v representa el volumen de titulante agregado (Ewing, 1969).
RESULTADOS Y DISCUSIÓN
Las concentraciones de ión cloruro en los extractos de saturación (Cuadro 1) fueron expresadas tomando la media y el intervalo de confianza con un valor de t igual a 2,92 (P<0,10) para tres repeticiones.
Se observa que ambos métodos produjeron resultados equivalentes en los extractos incoloros, donde es posible apreciar la aparición del precipitado rojo de cromato de plata. No obstante, los extractos M7 y M8, presentaron una fuerte coloración negra que impedía la visualización del punto final, haciendo impracticable el uso del cromato de potasio como indicador.
| CUADRO 1. Determinación de cloruro en los extractos de saturación. | ||||
| | ||||
| Muestra | Método | CV | Método 2 | CV |
| | ||||
| M1 | 3,80 ±0,52 | 8,0 | 3,87 ± 0,20 | 3,2 |
| M2 | 1,80 ± 0,17 | 5,6 | 2,00 ± 0,17 | 5,0 |
| M3 | 0,40 ± 0,07 | 10,3 | 0,48 ± 0,03 | 4,2 |
| M4 | 2,80 ± 0,08 | 1,7 | 2,72 ± 0,08 | 1,8 |
| M5 | 0,57 ± 0,09 | 9,3 | 0,59 ± 0,03 | 4,2 |
| M6 | 2,29 ± 0,39 | 10,00 | 2,36 ± 0,09 | 2,2 |
| M7 | N | . | 0,48 ± 0,02 | 2,5 |
| M8 | N | . | 1,90 ± 0,04 | 12 |
| | ||||
N = No pudo analizarse por el método 1.
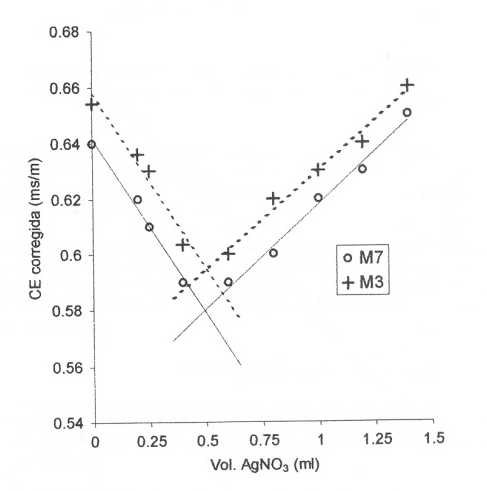
La Figura 1 muestra las gráficas de la valoración conductimétrica del anión cloruro con el catión plata, en un extracto incoloro (M3) y en otro de color negro (M7). La disminución continua de la CE antes del punto final es debida a la formación del AgCl(s), lo que implica la salida del sistema de los iones Cl-, que con una movilidad iónica equivalente de 79 cm2v-1s-1, son sustituidos por aniones nitrato que poseen una menor movilidad iónica (74 cm2v-1s-1) esto según Daniels y Alberty (1961). El aumento lineal que se produce una vez superado el punto de equivalencia es atribuido al exceso de iones plata y nitrato, una vez que se ha consumido totalmente el cloruro presente en la muestra. El hecho de que el comportamiento de la CE sea igual en ambos extractos indica que la presencia de materia orgánica coloidal, no interfiere en la determinación.
FIGURA 1. Gráfica de la valoración conductimétrica Cl- - Ag+ en los extractos M3 y M7.
El punto final de la valoración fue determinado localizando en la gráfica el punto del eje de coordenadas donde ambas rectas se interceptan, este procedimiento produce resultados más precisos que el procedimiento visual, lo que se refleja en los valores más bajos del coeficiente de variación para el método 2.
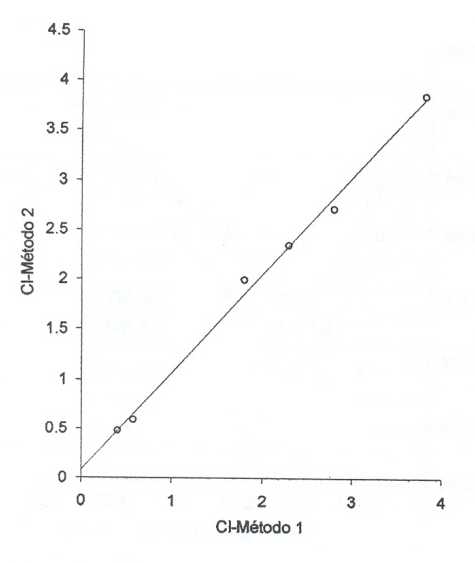
Para comparar ambos métodos se hizo uso de una recta de regresión en la que los valores de cloruro determinados por el método 1 se representaron en el eje de las ordenadas, mientras que los resultados del método 2 fueron ubicados en las abscisas, obteniéndose una línea recta (Figura 2) con un coeficiente de regresión (R2) de 0,995; la ordenada en el origen (a) es de 0,081 y la pendiente (b) es 0,989.
FIGURA 2. Recta de regresión entre los valores de cloruro aportados por ambos métodos.
Para contrastar si a y b difieren significativamente de los valores 0 y 1 respectivamente, se determinaron los límites de confianza a un nivel de significación del 90%, para lo cual se aplicaron las siguientes ecuaciones:
Pendiente = b ± tSb
Ordenada en el origen = a ± tSa
Pendiente = 0,989 ± (2,02)(0,0341) = 0,989 ± 0,0689
Ordenada en el origen = 0,081 ± (2,02)(0,078) = 0,081 ± 0,1576
De estos resultados se desprende que la pendiente y la ordenada en el origen no difieren en forma significativa de los valores ideales de cero y uno, por lo que se puede afirmar que no existen diferencias sistemáticas entre las dos series de resultados.
Para evaluar la exactitud de la valoración conductimétrica en los extractos de color negro, se determinaron los porcentajes de recuperación en las muestras M7 y M8 (Cuadro 2), obteniéndose recuperaciones cercanas al 98%, lo que demuestra que existen pocas interferencias en la determinación del anión.
| CUADRO 2. Determinación de porcentaje de recuperación de Cl-. | |||
| | |||
| Muestra | Cl- presente (meql-1) | Cl- presente (meql-1) | Recuperación (%) |
| | |||
| M7 | 0,98 | 0,95 | 96,9 |
| M7 | 1,48 | 1,44 | 97,0 |
| M7 | 1,98 | 1,94 | 98,0 |
| M8 | 2,40 | 2,35 | 97,8 |
| M8 | 2,90 | 2,87 | 99,0 |
| M8 | 3,40 | 3,39 | 99,7 |
| | |||
CONCLUSIONES
-
La presencia de extractos de saturación con un fuerte color negro limita la aplicación de técnicas volumétricas que se valen de cambios de color o formación de precipitados coloreados para la detección del punto final.
-
El problema de la presencia de extractos de saturación de color negro puede ser resuelto si se sigue el curso de la titulación midiendo la CE de la solución que se está valorando.
-
Se comprueba que en los extractos negros no se producen interferencias, obteniéndose porcentajes de recuperación cercanos al 100%. Mientras que en los extractos incoloros, la titulación conductimétrica produce resultados equivalentes a los que se obtienen cuando se emplea el cromato como indicador.
BIBLIOGRAFÍA
[ Links ]1. Daniels. A. and R. ALBERTY. 1961. Physical Chemistry. 2nd ed. New York. John Wiley and Sons. 744 pp. [ Links ]
2. EWING, G. W. 1969. Instrumental methods of chemical analysis. International Student Edition. 3rd ed. Tokio. Mc. Graw-Hill.627 p. [ Links ]
3. JANDER, G. 1961. Análisis Volumétrico. México. Unión Tipográfica. Editorial Hispanoamericana 1ra. Ed. 400 pp. [ Links ]
4. US DEPARTMENT OF AGRICULTURE (USDA). 1950. Agriculture handbook 60. Diagnosis and improvement of saline and álcali soils. US Department of Agriculture USA. 160 pp.