Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Archivos Latinoamericanos de Nutrición
versão impressa ISSN 0004-0622versão On-line ISSN 2309-5806
ALAN v.56 n.3 Caracas set. 2006
Barra de cereais de elevado teor protéico e vitamínico: estabilidade enzimática e das vitaminas c e e durante armazenamento
Daniela Freitas G. C., Roberto Moretti H.
Departamento de Tecnologia de Alimentos. Faculdade de Engenharia de Alimentos. Universidade Estadual de Campinas (UNICAMP). Campinas, Brasil.
RESUMO
Produtos a base de cereais vêm se tornando um excelente veículo para se incluir ingredientes com alegação funcional no mercado consumidor. Uma tendência emergente são os produtos formulados com proteína de soja, por providenciarem benefícios à saúde. Devido ao grande potencial destes produtos, foi considerado de interesse determinar a estabilidade de barra de cereais à base de proteína de soja, gérmen de trigo e aveia, suplementada de vitamina C (ácido ascórbico) e fortificada de vitamina E (acetato de a -tocoferol 50%), durante o armazenamento. Três filmes (A: PET/PEBD; B: PETMET/PEBD; C: PET/PEBD/AL/PEBD) foram utilizados como embalagens e as barras de cereais foram estocadas em condições de temperatura (25±2°C) e umidade relativa (56%) ambiente por um período de 180 dias. A estabilidade da vitamina C, vitamina E, e a atividade de lipase e peroxidase foram verificadas. Durante o estudo, as barras de cereais embaladas nos três filmes testados apresentaram uma retenção de vitamina C menor que 50%. No entanto, a embalagem estruturada com folha de alumínio (C), proporcionou menor velocidade de reação ao longo do período de armazenagem, k=0,00473 (-dia), e maior tempo de meia vida (146 dias). Os teores de vitamina E (acetato de a -tocoferol) nas barras de cereais apresentaram pequenas variações durante o armazenamento. Houve um aumento significativo (p£0,05) na atividade de peroxidase aos 90 dias de estocagem nas embalagens testadas, enquanto que a atividade de lipase não demonstrou aumento significativo durante o período estudado.
Palavras-chave: barra de cereais, estocagem, lipase, peroxidase, vitamina C, vitamina E.
SUMMARY
Cereal-based products have become an excellent vehicle for delivering tasty functional food ingredients to busy consumers. One emerging trends is food products formulates with soy protein because of its proven health benefits. Because of the potential usefulness of these products, it was considered of interest to determine the stability of cereal bars based on soy protein, wheat germ and oat, enriched with vitamin C (ascorbic acid) and E (acetate of a-tocopherol 50%), during the storage. Three films with different properties of barrier (A: PET/PEBD; B: PETMET/PEBD; C: PET/PEBD/AL/PEBD) were used as packing and the cereal bars were stored at temperature (25±2°C) and relative humidity ambient (56%) for six months. The stability of vitamin C, vitamin E and, its lipase and peroxidase activity was verified. During the study, the cereal bars packed in three tested films presented retention in the vitamin C lesser that 50%. However, packing structuralized with aluminum (C) leaf provided to minor speed of reaction during the storage, k=0,00437 (-day), and greater time of half-life (146 days). The vitamin E (acetate of a-tocopherol) in the cereal bars presented a little variation during the storage. It had a significant (p£ 0,05) increase in the peroxidase activity at 90 days of storage in the packages tested, while that the lipase activity demonstrated no significant increase during the period studied.
Key words: cereal bars, storage, lipase, peroxidase, vitamin C, vitamin E.
High protein and vitamin cereal bars: enzymatic and vitamins C and E stability during storage
RECIBIDO: 10-02-2006
ACEPTADO: 14-07-2006
INTRODUÇÃO
A tendência de consumir mais alimentos nutritivos no lugar de doces e guloseimas tem levado ao aparecimento de novos tipos de produtos tais como barras de cereais diversificadas, com variações como cobertura de chocolate ou incorporação de diferentes frutas e castanhas. Como o consumo de cereais vem se expandindo além do café da manhã para qualquer hora do dia, estes produtos vêm se tornando um excelente veículo para se incluir ingredientes com alegação funcional no mercado consumidor. Os cereais estão crescentemente exercendo papel vital no estilo de vida moderno por causa da conveniente forma os quais podem ser utilizados, incluindo produtos prontos para consumir, instantâneos, barras de cereais e barras energéticas. Uma tendência emergente são os produtos formulados com proteína de soja por promoverem benefícios à saúde. As mulheres, em especial, representam um novo nicho de mercado de produtos desenvolvidos para encontrar necessidades nutricionais específicas (1).
Dentro dos produtos a base de cereais, as barras podem fornecer importante suplementação de calorias e elementos nutritivos como lipídeos, fibras, proteínas, minerais e vitaminas. Entretanto, possuem considerável conteúdo de lipídeos e grande quantidade de ácidos graxos polinsaturados, tornando-os susceptíveis á deterioração oxidativa, que reduz sua estabilidade durante o armazenamento (2). A rancidez oxidativa das gorduras pode resultar no desenvolvimento de produtos tóxicos, mudanças de coloração, de textura e perda de valor nutricional, devido à destruição de vitaminas e ácidos graxos essenciais (3). A oxidação é catalisada por uma série de fatores tais como oxigênio, luz, calor, metais, pigmentos, condições alcalinas, e grau de insaturação das gorduras.
Assim, foi considerado de interesse determinar a estabilidade de vitaminas e a atividade das enzimas peroxidase e lipase em barra de cereais a base de proteína de soja, gérmen de trigo e aveia, suplementada de vitamina C (ácido ascórbico) e fortificada de vitamina E (acetato de a -tocoferol 50%), durante armazenamento de seis meses em três diferentes tipos de embalagens.
Material e Métodos
Preparação das barras de cereais
Os ingredientes utilizados na manufatura das barras de cereais, bem como o processo de fabricação seguem o descrito por Freitas e Moretti (4). A Tabela 1 mostra a formulação e a composição centesimal aproximada da barra de cereais desenvolvida.
Armazenamento
Foram utilizados três filmes de embalagem com diferentes características de espessura, taxa de permeabilidade ao vapor de água (TPVA) e ao oxigênio (TPO2) os quais foram especificados por Freitas e Moretti (4).
As barras de cereais foram embaladas e armazenadas em condições de temperatura (25±2°C) e umidade relativa (56%) ambiente por um período de seis meses. A atividade das enzimas lípase, peroxidase, e determinações das vitaminas C e E foram realizadas durante o armazenamento logo após o processamento, após 45 dias, 90 dias, 135 dias e 180 dias, conforme ASTM (5).
Análise de vitamina C e vitamina E
Foram realizadas as determinações quantitativas de ácido ascórbico pelo método padrão da AOAC (6) modificado por Benassi (7); e de vitamina E por HPLC segundo Leenheer et al. (8). O teor de vitamina E na barra de cereais foi extraído a partir de 2,5 g de amostra de barra de cereais, previamente congelada e reduzida em moinho, em 25,0ml de dimetilsulfóxido (DMSO) em agitação magnética por 20 minutos. Foi utilizada Coluna ODS 2 (150 x 4,6 mm) e detector UV a 280nm . A fase móvel foi metanol 100% a 2,0ml/min. Utilizou-se padrão vitamina E 50% tipo CWS/F (Roche Vitaminas Brasil Ltda).
* Mistura de açúcar cristal e melaço de cana na proporção de 95:5
** O gérmen de trigo teve seu teor de umidade ajustado para 28% e a torração foi realizada em estufa a 180°C por 8 minutos.
*
Freitas e Moretti (2004)*; dados representam média de três replicatas ± estimativa do desvio padrão Proteína, % (N x 5,7)
Teor de carboidratos calculado por diferença.
*
FREITAS, D. G. C.; MORETTI, R. H. Desenvolvimento, caracterização e avaliação sensorial de barra de cereais de alto teor protéico e vitamínico à base de proteína texturizada de soja, gérmen de trigo e aveia. In: FREITAS, D. G. C. Desenvolvimento e Estudo da Estabilidade de Barra de Cereais de Elevado Teor Protéico e Vitamínico. 2005. Tese (Doutor em Tecnologia de Alimentos) – Universidade Estadual de Campinas, Campinas, 2005.Atividade enzimática
A atividade de lipase foi medida através de método usado por Kaur et al. (9). A atividade de peroxidase foi medida por espectrofotometria de acordo com Ekstrand et al. (10). Depois de inversão rápida da cubeta, fez-se a leitura a 420nm. Foram realizadas triplicatas de cada amostra em leituras de 5 minutos.
Previamente às análises, a homogeneização das amostras foi realizada através da desintegração da barra nas soluções tampão indicadas nos respectivos métodos, numa proporção de 1:2 (amostra : solução).
Análise dos dados
Os dados obtidos foram avaliados pelo método de análise de variância (ANOVA) e teste F com comparação de médias pelo teste de Tukey (p£0,05), ambos do software estatístico SAS (11). O modelo matemático para a cinética da reação de degradação de vitamina C, segundo Labuza (12), foi definido pelo método de estimação linearizada (ou não linearizada) no programa Statistica 5.0 (13).
Resultados e Discussão
Cinética de reação de degradação da vitamina C
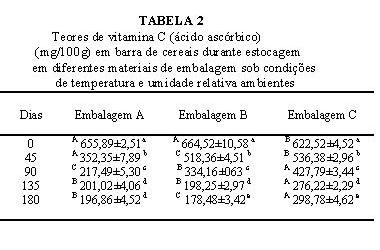
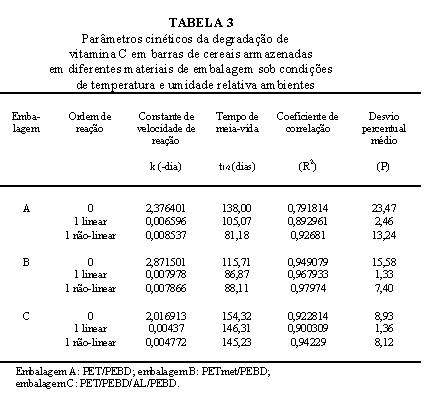
Na Tabela 2 estão descritos os teores de vitamina C nas barras de cereais durante o período de estocagem. A partir destes dados, determinou-se a ordem da reação e os parâmetros da cinética de sua degradação nas barras de cereais embaladas nos filmes A, B e C (Tabela 3).
Dados representam média de três replicatas ± estimativa do desvio padrão
a-e
: Médias com letras minúsculas diferentes, na mesma coluna, diferem entre si estatisticamente (p£ 0,05) durante tempo de estocagemA-C
: Médias com letras maiúsculas diferentes, na mesma linha, diferem entre si estatisticamente (p£ 0,05) entre as embalagensEmbalagem A: PET/PEBD; embalagem B: PETmet/PEBD; embalagem C: PET/PEBD/AL/PEBD.
As reações de degradação da vitamina C se ajustaram ao modelo cinético de primeira ordem, linearizado, para os três filmes de embalagem. Nos alimentos, a maioria das reações que representam importantes perdas de qualidade é caracterizada por modelos de ordem zero (qualidade de alimentos congelados, escurecimento não enzimático) ou modelos de primeira ordem (perda de vitaminas, crescimento ou morte de microorganismos, oxidação da cor, perda de textura em termicamente processados) (14).
Os parâmetros utilizados na determinação do modelo mais ajustado para a reação de perda de vitamina C nas embalagens testadas foram o valor do coeficiente de correlação linear R2 (o mais próximo da unidade), e o valor do desvio percentual médio (P), que é a média da diferença percentual relativa entre os valores experimentais e valores preditos. Lomauro et al. (15) mostraram que valores de P menores que 5 representam bom ajuste do modelo, enquanto que valores de P maiores que 10, um ajuste deficiente do modelo.
Para a cinética da reação de primeira ordem, o cálculo da constante de velocidade de reação (k) é dado pela equação k=(ln A – ln At)/t, onde a linha reta é obtida plotando o logaritmo neperiano da variável versus o tempo da reação. Através da constante de velocidade da reação (k) pôde-se calcular o tempo de meia vida (t1/2) da reação, isto é, o tempo para que a concentração de vitamina C se reduza à metade do valor inicial.
No período de 180 dias, as barras de cereais embaladas nos três filmes testados apresentaram uma retenção de menos que 50%, variando o conteúdo final de ácido ascórbico entre 178,48mg/100g e 298,78mg/100g. A embalagem C, composta com folha de alumínio, proporcionou menor velocidade de reação ao logo do período de armazenagem, k=0,00437 (-dia), e maior tempo de meia vida de 146 dias (Tabela 3). Embora o filme A composto de polietileno e polipropileno tenha apresentado maior taxa de permeabilidade ao oxigênio que o filme B, com estrutura metalizada, proporcionou menor velocidade de degradação da vitamina C nas barras de cereais e maior tempo de meia vida, apresentando uma diferença de 19 dias.
A principal causa da degradação da vitamina C é a oxidação aeróbica ou anaeróbica, ambas levando à formação de furaldeídos, compostos que polimerizam facilmente e formam pigmentos escuros (16). Segundo Nagy (17), após o consumo do oxigênio livre das embalagens, as reações anaeróbicas predominam, entre elas, a degradação de ácido ascórbico, mas em menor velocidade que sob condições aeróbicas. A degradação do ácido ascórbico foi atribuída à reação de oxidação aeróbica, uma vez que ambas as embalagens apresentaram-se permeáveis ao oxigênio. Íons metálicos e as enzimas ácido ascórbico oxidase, citocromo oxidase, fenolase e peroxidase, são catalisadores da reação de oxidação da vitamina C (18), o que justificaria o fato da maior velocidade de reação nas barras de cereais embaladas no filme B, de maior taxa de permeabilidade ao vapor de água, o que proporcionaria a interação da umidade e oxigênio, favorecendo o efeito de catalisadores na reação de degradação.
Estabilidade de vitamina E
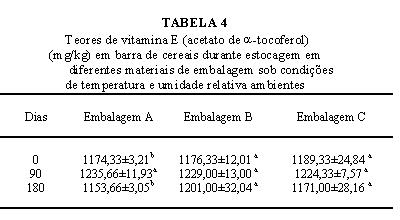
Os teores de vitamina E nas barras de cereais apresentaram pequenas variações durante o armazenamento (Tabela 4), não havendo diferença significativa (p£ 0,05) entre os teores determinados no primeiro e último dia do período analisado, para ambas as embalagens testadas.
Dados representam média de três replicatas ± estimativa do desvio padrão
a-e
: Médias com letras diferentes, na mesma coluna, diferem entre si estatisticamente (p£ 0,05) pelo teste de TukeyEmbalagem A: PET/PEBD; embalagem B: PETmet/PEBD; embalagem C: PET/PEBD/AL/PEBD.
O comportamento da vitamina E adicionada nas barras de cereais confirmou a maior estabilidade dos derivados do tocoferol. Os tocoferóis são lentamente oxidados pelo oxigênio atmosférico. Por outro lado, esta oxidação é acelerada com exposição à luz (radiação UV), calor e álcali e na presença de sais de ferro e cobre. Os ésteres derivados dos tocoferóis, como o acetato de a -tocoferol e succinato de a -tocoferol, apresentam maior estabilidade em relação ao oxigênio, íons metálicos, luz e calor, sendo formas de maior interesse comercial (19,20).
Atividade enzimática
Os valores da atividade das enzimas peroxidase e lipase nas barras de cereais durante o período de estocagem nas diferentes embalagens estão descritos na Tabela 5.
O desenvolvimento de rancidez em cereais e seus produtos tem tomado grande atenção na literatura, pois são conhecidas por alterar flavor, cor, textura e qualidade nutricional de alimentos in natura e processados. O processo é facilitado ou catalisado por diversos fatores. Os principais agentes são, no entanto, as enzimas, particularmente lipase, lipoxigenase e peroxidase, e temperatura (21). As lipases, as quais atacam somente as ligações acil de triacilgliceróis insolúveis, provocam a rancificação hidrolítica que é o resultado desta hidrólise de glicerídeos produzindo características organolépticas indesejáveis ao alimento (22).
A peroxidase, um membro de um extenso grupo de enzimas chamadas oxidoredutases, tem uma relação empírica com "off-flavors" e "off-colors" em vegetais in natura e processados (23). Segundo Bruemmer et al. (24), a enzima é relativamente estável a inativação pelo calor e pode ser regenerada sob certas condições. Burnette (23) afirma que quanto mais curto o tempo de exposição ao calor, maior a porção de enzima subseqüentemente regenerada. O autor reporta que 6 minutos a 121°C é necessário para inativar a peroxidase em ervilhas. Amostras tratadas a 130°C por 36 segundos reduziram em 6% a atividade de peroxidase depois de 1-2 dias de estocagem. Após 5 dias, a atividade aumentou para 10% da preparação original.
Os resultados apresentados na Tabela 5 indicaram que houve um aumento significativo da atividade da peroxidase durante o período de 90 dias de estocagem, provavelmente devido à regeneração. Embora o tratamento de torração do gérmen de trigo tenha sido severo (180°C durante 8 minutos), o processo não dotava de um sistema de homogeneização, o que implicaria na possível inativação incompleta nas camadas inferiores. Segundo Sehyan et al. (21), tratamentos térmicos aplicados por maior tempo que o usual são requeridos para prevenir a regeneração da atividade da peroxidase em alimentos. A regeneração ocorre provavelmente devido à enzima não ser completamente ou irreversivelmente inativada. Os fatores que afetam a regeneração da atividade de peroxidase compreendem método usado para detecção da atividade, a severidade do tratamento térmico combinado com o tempo, e as condições de estocagem da enzima inativada. Aos 90 dias de estocagem, a maior atividade se deu nas barras de cereais embaladas no filme A (PET/PEBD), de maior permeabilidade ao oxigênio (TPO2 0,215cm3/m2.dia.atm), diferindo significativamente (p£0,05) das embalagens B (PETmet/PEBD) e C (PET/PEBD/AL/PEBD) no mesmo período.
Dados representam média de três replicatas ± estimativa do desvio padrão
a-e
: Médias com letras minúsculas diferentes, na mesma coluna, diferem entre si estatisticamente (p£ 0,05) durante tempo de estocagemA-C
: Médias com letras maiúsculas diferentes, na mesma linha, diferem entre si estatisticamente (p£ 0,05) entre as embalagensEmbalagem A: PET/PEBD; embalagem B: PETmet/PEBD; embalagem C: PET/PEBD/AL/PEBD.
A temperatura ambiente durante o armazenamento favoreceu a atividade e regeneração da enzima. Como para todas as enzimas, a atividade de peroxidase aumenta com o aumento da temperatura até aproximadamente 40°C, devido à ação normal da temperatura sobre todas as reações químicas e bioquímicas (21). Em um trabalho com ervilhas que foram branqueadas suficientemente para inativar a atividade da peroxidase original, Burnette (23) reportou que a regeneração usualmente ocorre em poucas horas se o produto é deixado à temperatura ambiente.
Após 90 dias de estocagem, houve um declínio significante na atividade de peroxidase nas barras de cereais, em todas as embalagens testadas. Este fato foi atribuído à diminuição do oxigênio disponível no interior das embalagens, o oxigênio residual do processo de selagem. O aumento na atividade da enzima até o final do período estudado foi atribuído ao oxigênio transferido do ambiente através das embalagens, sendo a atividade da peroxidase mais elevada nas barras embaladas no filme A, de maior taxa de permeabilidade ao oxigênio, diferente estatisticamente dos filmes B e C no mesmo período.
Durante o armazenamento sob condições ambiente, a atividade da lipase se apresentou de maneira muito semelhante nas barras de cereais embaladas nos filmes B e C, sem variações significativas. No filme A, a atividade de lipase se manteve constante até 90 dias de armazenamento, tendendo a um declínio significativo após este período. A atividade de lipase não demonstrou aumento significativo durante os 180 dias de estocagem, o que não acarretaria danos e perdas de qualidade a barra de cereais com relação a rancidez hidrolítica, demonstrando o efeito eficaz do tratamento térmico de torração realizado nos ingredientes gérmen de trigo e aveia, para esta enzima.
Conclusão
As diferentes propriedades dos filmes de embalagem estudados tiveram influência significativa (p£0,05) na estabilidade da vitamina C e atividade da peroxidase nas barras de cereais durante o armazenamento. As barras de cereais embaladas em filme de PET/PEBD/AL/PEBD (C) apresentaram maior preservação da vitamina e estabilidade enzimática, conferindo maior eficiência com relação a estas características. As reações de degradação da vitamina C atribuídas à oxidação aeróbica se ajustaram ao modelo cinético de primeira ordem, linearizado, representando uma retenção menor que 50% durante o período de estocagem. Houve regeneração da enzima peroxidase durante o início do período de estocagem, e a variação na sua atividade foi dependente do conteúdo de oxigênio residual ou transferido do ambiente através das embalagens.
Os teores de vitamina E (acetato de a -tocoferol) e a atividade de lipase nas barras de cereais apresentaram pequenas variações durante o armazenamento nos três filmes de embalagens testados.
Referências
1. Tockman J. Capitalizing on increasing consumer interest in soy protein. Cereal Foods World 2002; 47: 172-174. [ Links ]
2. Estévez AM, Escobar B, Vázquez M, Castillo E, Araya E, Zacarías I. Cereal and nut bars, nutritional quality and storage stability. Plant Food Hum Nutr 1995; 47: 309-317. [ Links ]
3. Dziezak, J. D. Preservatives: antioxidants. The ultimate answer to oxidation. Food Technol. 1986; 40: 94-102. [ Links ]
4. Freitas DGC, Moretti RH. Barras de cereais elaboradas com proteína de soja e gérmen de trigo, características físico-químicas e textura durante armazenamento. Arch Latinoamer Nutr 2005; 55: 299-304. [ Links ]
5. ASTM. American Society For Testing And Material. Standard guide for the shelf life determination of consumer products by sensory evaluation. Philadelphia: ASTM International; 1993. [ Links ]
6. Official Methods of Analysis of AOAC International. 16th ed. 3rd rev. Gaithersburg, MD: AOAC International; 1997. [ Links ]
7. Benassi MT. Análise dos estudos de diferentes parâmetros na estabilidade de vitamina C em vegetais processados. MS Thesis, Faculdade de Engenharia de Alimentos, Universidade Estadual de Campinas, Campinas, BR; 1990. [ Links ]
8. Leenheer AP, Lambert WE, Ruyter MGM. Modern Chromatographic Analysis of the Vitamins. New York: Marcel Decker; 1985. [ Links ]
9. Kaur J, Ramamaurthy V, Kothari RM. Characterization of oat lipase for lipolysis of rice bran oil. Biotechnology Letters 1993; 15: 257-262. [ Links ]
10. Ekstrand B, Gangby I, Akesson G. Lipase activity in oats – Distribution, pH dependence, and heat inactivation. Cereal Chem 1992; 69: 379-381. [ Links ]
11. SAS Institute. SAS Users Guide: statistics. Cary, USA: SAS Inst., 1993. [ Links ]
12. Labuza TP. Shelf life dating of foods. Westport: Food & Nutrition Press Inc; 1982. [ Links ]
13. StatSoft, Inc. Statistica for Windows (Computer program manual). Tulsa, OK: StatSoft, Inc; 1995. [ Links ]
14. Taoukis PS, Labuza TP, Saguy IS. Kinetics of Food Deterioration and Shelf-life Prediction. In: Valentas KJ, Rotstein E, Singh RP. The Handbook of Food Engineering Practice. Boca Raton: CRC Press, pp 361-402; 1997. [ Links ]
15. Lomauro CJ, Bakshi AS, Labuza TP. Evaluation of food moisture sorption isotherm equations. Part I: Fruit, vegetables and meat products. Lebensm Wiss U–Technology 1985; 18: 111-117. [ Links ]
16. Bobbio FO, Bobbio PA. Introdução à Química de Alimentos. 3. ed. São Paulo: Livraria Varela; 2003. [ Links ]
17. Nagy S. Vitamin C content of citrus fruit and their products. A Review. J Agric Food Chem 1980; 28: 8-18. [ Links ]
18. Buss D, Robertson J. Manual of Nutrition. Ministry of Agriculture, Fisheries and Food (MAFF). 8th ed. London: HMSO; 1982. [ Links ]
19. Ames SR. Industrial preparations and production, estimation in foods and foods suplements, occurrence in foods. In: Sebrel Jr WH, Harris RS The Vitamins. 2 ed. New York: Academic Press, pp 225-233; 1972. [ Links ]
20. Machlin LJ. Handbook of Vitamins. New York: Marcel Decker; 1982. [ Links ]
21. Seyhan F, Tijskens LMM, Evranuz O. Modelling temperature and pH dependence of lipase and peroxidase activity in Turkish hazelnuts. J Food Eng 2002; 52: 387-395. [ Links ]
22. Bobbio PA, Bobbio FO. Química do Processamento de Alimentos. 3. ed. São Paulo: Livraria Varela; 2001. [ Links ]
23. Burnette FS. Peroxidase and its relationship to food flavor and quality: a review. J Food Sci 1977; 42: 1-6. [ Links ]
24. Bruemmer JH, Bongwoo R, Bowen ER. Peroxidase reactions and orange juice quality. J Food Sci 1976; 41: 186-189. [ Links ]