Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Archivos Venezolanos de Farmacología y Terapéutica
versión impresa ISSN 0798-0264
AVFT vol.34 no.1 Caracas mar. 2015
Estudio comparativo de la eficiencia terapéutica entre imiquimod crema al 5% y una loción basada en polifenoles en el tratamiento de la queratosis actínica
Comparative study of the therapeutic efficiency between imiquimod 5% cream and lotion based on polyphenols in the treatment of actinic keratosis
Mayerlim Medina, Raquel Cano, Ismael Contreras, Andreina Prado, Clímaco Cano
Centro de Investigaciones Endocrino-Metabólicas Dr. Félix Gómez. La Universidad del Zulia. Facultad de Medicina. Maracaibo-Estado Zulia.
Resumen
La queratosis actínica se presenta en forma de lesiones premalignas confinadas a la epidermis, producidas por la radiación ultravioleta, que pueden evolucionar a carcinoma de células escamosas el cual es altamente metastásico. Los tratamientos actualmente disponibles comprenden escisión quirúrgica, crioterapia, peeling químico, fototerapia, retinoides, 5-fluoruracilo e imiquimod. Aunque logran tasas de remisión significativas, también es cierto que todos tienen el potencial de provocar efectos colaterales indeseables, que perturban la calidad de vida del paciente y que lo inducen a interrumpir el tratamiento. No hay reportes en la literatura científica del uso de los polifenoles en el tratamiento farmacológico de la queratosis actínica por lo que el objetivo del presente estudio fue comparar la eficiencia terapéutica entre imiquimod al 5% crema y una loción basada en polifenoles en el tratamiento de la queratosis actínica. Para ello se seleccionaron 56 pacientes que fueron asignados de forma aleatoria a uno de los siguientes grupos. Grupo I: recibió dos ciclos de tres semanas de aplicación diaria de Imiquimod crema al 5%, con un intervalo de descanso de 3 semanas, más protector solar diario durante 16 semanas ininterrumpido. Grupo II: recibió loción polifenólica al 5% dos aplicaciones diarias durante 16 semanas más crema protectora solar con polifenoles. Los resultados indican que los polifenoles son tan eficientes como el imiquimod en el tratamiento de la queratosis actínica. El 30% de los pacientes tratados con imiquimod abandonó el tratamiento siendo la razón principal sus efectos adversos, a diferencia del preparado polifenólico que fue bien tolerado por todos los pacientes. En conclusión los polifenoles son una nueva, muy eficiente y segura alternativa para el tratamiento de la queratosis actínica.
Palabras Clave: Queratosis actínica, Polifenoles, Imiquimod, Carcinoma de células escamosas.
Abstract
Actinic keratosis (AK) presents as premalignant lesions confined to the epidermis, produced by ultraviolet rays, which can evolve to a highly metastatic cancer such as squamous cell carcinoma. Available treatments include surgical excision, criotherapy, chemicals peeling, phototherapy, retinoids, 5-fluoruracil and imiquimod. Even though they achieve significant remission rates, it is also certain that they have the potential to provoke undesirable side effects. There are no reports in previous scientific studies about the use of polyphenols in pharmacological treatment of actinic keratosis. The main objective of this study was to compare the therapeutic efficiency between 5% imiquimod cream and a lotion based on polyphenols in actinic keratosis treatment. For this a total of 56 patients were selected and assigned randomly to one of the following groups. Group I: received two three weeks cycles of a daily application of 5% Imiquimod cream with a 3 week resting period, + a daily application of sun protector during 16 weeks uninterrupted. Group II: received two daily applications of a 5% polyphenolic lotion during 16 weeks. Our results show that the polyphenolic lotion as efficient as imiquimod in the treatment of AK. The 30% of patients treated with imiquimod withdrew from treatment because of undesirable side effects; instead polyphenol treatment was well tolerated by all patients. The polyphenolic preparation was well tolerated by all the patients. In conclusion polyphenols are a new and safe alternative in the treatment of AK.
Keywords: Actinic keratosis, Imiquimod, Polyphenols, Squamous Cell Carcinoma.
Recibido: 20/10/2015 Aceptado: 21/11/2015
Introducción
El territorio Venezolano por su posición geográfica, es fuertemente impactado por la radiación ultravioleta, que es el más importante factor de riesgo en la aparición de queratosis actínica, especialmente entre la población con fototipo cutáneo I-III según Fitzpatrick1,2.
Las lesiones típicas de la queratosis actínica aparecen en zonas de exposición crónica al sol, especialmente en la cara, frente, cuero cabelludo, orejas, cuello, escote, brazos, dorso de las manos. El diagnóstico se fundamenta en los aspectos clínicos típicos y la biopsia es necesaria cuando las características clínicas sean dudosas o cuando formas especiales de tratamiento sean consideradas. Puede evolucionar a cáncer de células escamosas el cual es altamente metastásico, circunstancia que puede impactar de manera significativa el curso de la vida del individuo y su grupo familiar por las implicaciones emocionales y económicas que ocasiona su tratamiento3,4.
Hay muchos tratamientos efectivos disponibles y la elección de uno u otro depende de las características individuales del paciente, así como del tamaño, número y localización de las lesiones. Además de la escisión quirúrgica, se ha empleado crioterapia, curetaje, electrocoagulación, peeling químico, terapia con láser, terapia fotodinámica5 y el 5-fluoruracilo tópico6. Recientemente se están observando buenos resultados con inmunomoduladores tipo imiquimod, retinoides tópicos y ácido salicílico7,8.
Son múltiples los estudios que han demostrado la efectividad del Imiquimod en el tratamiento de la Queratosis Actínica y ha sido aprobado su uso por la FDA9. El mecanismo de acción exacto por el cual activa al sistema inmune no está muy claro, sin embargo, se cree que lo hace a través de los receptores tipo Toll 7 (TLR7), involucrados comúnmente en el reconocimiento del patógeno, sobre la superficie celular10. Presenta una tasa de remisión de un 85%, pero puede causar reacciones cutáneas de moderadas a intensas consistentes en eritema, quemaduras y fiebre, con una tasa de recaída de un 46% 6,11.
Estudios epidemiológicos sugieren un efecto protector de los vegetales y frutas contra el cáncer y la enfermedad cardiovascular12. Varias hipótesis se han planteado para explicar este fenómeno y una de las más validadas es que ese efecto protector se debe a la presencia de grandes cantidades de polifenoles, que además de tener una gran capacidad antioxidante, exhiben otras propiedades como regular el óxido nítrico, aumentar la movilización de leucocitos, inducir apoptosis, inhibir la proliferación celular y la angiogénesis y exhiben actividad fitoestrogénicas13,14. Después de su absorción los polifenoles son metabolizados en hígado a compuestos metilados, glucuronizados y sulfatados. Esto puede influenciar su bioactividad, pero hay pocos estudios al respecto.
Por otro lado, la inflamación crónica se considera que es un proceso de duración prolongada (semanas o meses), en la que se pueden observar simultáneamente signos de inflamación activa, de destrucción tisular y de intentos de curación. Con frecuencia se inicia de forma insidiosa como una respuesta solapada de baja intensidad y a menudo asintomática. En efecto, éste último tipo de respuesta de inflamación crónica se observa en enfermedades más frecuentes e incapacitantes del ser humano, como son la aterosclerosis, la tuberculosis, las neumopatías crónicas y enfermedades autoinmunes como la artritis reumatoide, el lupus eritematosos sistémico la queratosis actínica y la psoriasis, entre otras.
El uso de tratamientos quirúrgicos y farmacológicos actualmente disponibles, aunque muchos de ellos eficaces, puede ir acompañado de efectos adversos que inducen al paciente a interrumpirlos, hecho que justifica el estudio de los polifenoles como nuevos medicamentos eficaces sin efectos adversos y de fácil adquisición en tratamiento de la queratosis actínica.
Pacientes y métodos
En el presente estudio fueron incluidos 56 pacientes que acudieron a la consulta de la Sanidad del Estado Zulia y al Centro de Investigaciones Endocrino – Metabólicas Dr. Félix Gómez (CIEM), de la Facultad de Medicina de la Universidad del Zulia, Maracaibo, Venezuela. Los pacientes fueron de ambos géneros, adultos mayores de 18 años, con lesiones clínicamente sugestivas de queratosis actínica en frente, cara, cuello, escote, brazos, antebrazos y dorso de manos. A todos los pacientes se les realizó la historia clínica por un dermatólogo. Fueron causa de exclusión los siguientes criterios: Embarazo, lactancia, alcoholismo, alergia al imiquimod o a los excipientes de las cremas, alergia a los salicilatos o a los polifenoles, uso de medicamentos inmunosupresores, inmunomoduladores, interferón, drogas citotóxicas, corticosteroides orales o tópicos 90 días antes del estudio e imiquimod 30 días previos al estudio. Todos los pacientes debieron consignar por escrito su consentimiento para participar voluntariamente en la investigación.
Los pacientes fueron asignados de forma aleatoria a uno de los siguientes grupos:
Grupo I. Imiquimod crema al 5%. Constituido por 20 pacientes que recibieron una aplicación diaria de Imiquimod crema al 5% sobre las lesiones, durante 2 ciclos de 3 semanas con un intervalo de 3 semanas sin tratamiento, acompañado de una aplicación diaria de protector solar durante las 16 semanas.
Grupo II. Loción polifenólica al 5%. Constituido por 36 pacientes quienes recibieron dos aplicaciones diarias de la loción polifenólica al 5%, sobre las lesiones, durante 16 semanas acompañado de una aplicación diaria de crema protectora solar con polifenoles.
Los pacientes acudieron a consultas sucesivas en la 3a, 6a, 9a y 16a semanas para evaluar la evolución (progresión, persistencia o regresión) de las lesiones y la aparición de reacciones adversas.
Evaluación de la eficacia del tratamiento
El parámetro de eficacia principal empleado fue la enumeración por parte del investigador de todas las lesiones de queratosis actínica visibles y/o palpables en cada visita.
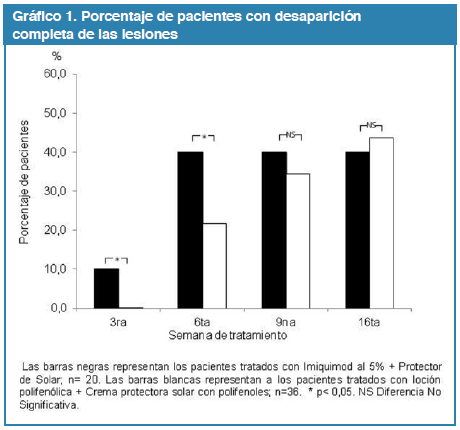
El indicador principal de eficacia fue la evaluación de la tasa de desaparición completa de lesiones, definida como la proporción de sujetos con un recuento de cero lesiones.
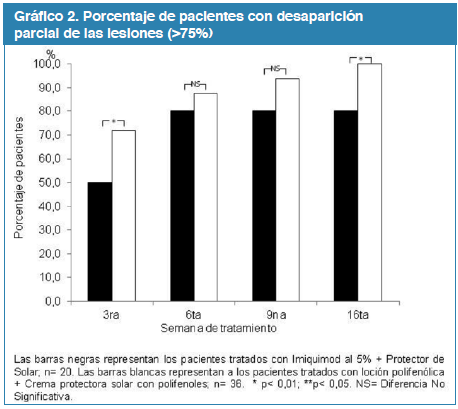
El indicador secundario de eficacia fue la evaluación de la tasa de desaparición parcial de lesiones, definida como la proporción de pacientes con reducción del 75% o más lesiones de queratosis actínica en cada visita, comparada con la observada antes de iniciar el tratamiento.
Evaluación de la seguridad del tratamiento
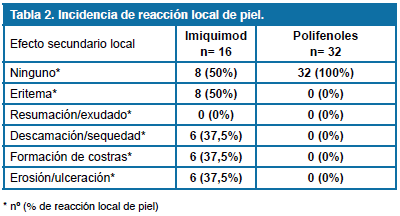
La seguridad del tratamiento se evaluó en cada visita a través del registro de efectos adversos y la evaluación por parte del investigador de la reacción local de piel, definida como el conjunto de efectos adversos locales (eritema, resumación/ exudado, descamación/sequedad, formación de costras, erosión/ulceración). En cada visita, la reacción local de piel se calificó como presente o ausente.
Análisis estadístico
Para el análisis estadístico se utilizó el programa SPSS versión 17.0 para Windows. Para comparar los resultados obtenidos entre los diferentes grupos de pacientes con queratosis actínica antes de iniciar el tratamiento y luego de 3, 6, 9 y 16 semanas de tratamiento, se utilizó la prueba U de Mann- Whitney. Para comparar los resultados obtenidos en cada grupo entre sí, antes del tratamiento y luego 3, 6, 9 y 16 semanas de tratamiento, se utilizó el modelo general lineal de medidas repetidas. El Test exacto de Fisher fue usado para comparar la proporción de pacientes que respondieron al tratamiento. Los datos fueron expresados como promedio ± EE. Se consideraron diferencias significativas cuando la p < 0,05.
Resultados
Características de los pacientes
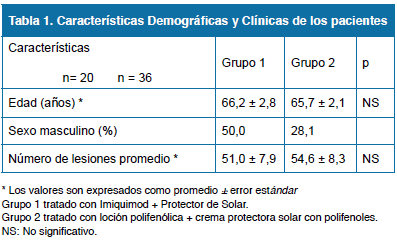
Fueron seleccionados 56 pacientes que asistieron a la consulta del Centro de Investigaciones Endocrino – Metabólicas Dr. Félix Gómez de la Facultad de Medicina de la Universidad del Zulia, Maracaibo, Venezuela, y a la Unidad Sanitaria del Estado Zulia durante el periodo de marzo a noviembre de 2011. Las características demográficas y clínicas de los individuos en estudio están descritas en la tabla 1.
El grupo I (Imiquimod), quedó conformado por 20 pacientes con diagnóstico clínico y por biopsia de queratosis actínica; con una edad promedio de 66,2 ± 2,8 años y el porcentaje de hombres fue de 50,0%. Presentaron un promedio de lesiones de 51,0 ± 7,9 antes de iniciar el tratamiento.
El grupo II (Polifenoles), quedó conformado por 36 pacientes con diagnóstico clínico y por biopsia de queratosis actínica; con una edad promedio de 65,7 ± 2,1 años y el porcentaje de hombres fue de 28,1%. Presentaron un promedio de lesiones de 54,6 ± 8,3 antes de iniciar el tratamiento.
Evaluación de la Eficacia
Semana 0 a 3. Al evaluar los pacientes durante la 3a semana de tratamiento, en el 10% de los pacientes del grupo I se evidenció desaparición completa de las lesiones, mientras que ninguno de los pacientes del grupo II tratado con los polifenoles presentó desaparición completa de las lesiones (p< 0,05). Una desaparición parcial de las lesiones fue observado en el 71,8% de los pacientes del grupo II y 30% en los pacientes del grupo I, encontrándose diferencias significativas al comparar el grupo I con el grupo II (p<0,05).
Semana 3 a 6. Durante la 6a semana de tratamiento, un 40% de los pacientes del grupo I, presentó desaparición completa de las lesiones, mientras que en el 21,8% de los pacientes del grupo II se observó desaparición completa de las lesiones, (p<0,05). Una desaparición parcial de las lesiones fue observada en el 87,5% de los pacientes del grupo II, contra el 80% de los pacientes del grupo I, no observándose diferencias significativas al compararlos.
Semana 6 a 9. Durante la 9a semana de tratamiento, un 40% de los pacientes que recibió del grupo I, presentó desaparición completa de las lesiones, mientras que en el 34,5% de los pacientes del grupo II se observó desaparición completa de las lesiones, no encontrándose diferencias significativas entre los grupos. Una desaparición parcial de las lesiones fue observada en el 93,7% de los pacientes del grupo II, contra el 80% de los pacientes del grupo I, no encontrándose diferencias significativas al compararlos.
Semana 9 a 16. Durante la 16a semana de tratamiento, un 40% de los pacientes del grupo I, presentó desaparición completa de las lesiones, mientras que en el 43,7% de los pacientes del grupo II se observó desaparición completa de las lesiones, no encontrándose diferencias significativas entre los grupos. Una desaparición parcial de las lesiones fue observado en el 100% de los pacientes del grupo II, contra el 80% de los pacientes del grupo I, encontrándose diferencias significativas al compararlos (p<0,05).
Evaluación de la seguridad
Cuatro pacientes, del grupo tratado con Imiquimod, se retiraron durante el tratamiento por razones diferentes a los efectos adversos y no fueron incluidos en el análisis de la seguridad. Los efectos secundarios y las interrupciones como resultado de los efectos adversos están resumidos en la tabla 2.
Discusión Los resultados del presente estudio indican que los polifenoles son tan eficientes como el imiquimod en el tratamiento de la queratosis actínica, al no observarse diferencias significativas en los porcentaje de mejoría, pero con el agravante de los efectos adversos del imiquimod, que motivó al 50% de los pacientes del estudio a interrumpir el tratamiento, de los cuales el 30% lo hizo por efectos adversos y el restante 20% por causas desconocidas.
De acuerdo a las pautas para el manejo de la queratosis actínica de la Asociación Británica de Dermatología5 el imiquimod en crema al 5%, es una opción de primera elección para el tratamiento de la queratosis actínica localizada en cuero cabelludo, pabellones auriculares, mejillas, nariz, frente, regiones perioral y periorbital. En el presente estudio después de 16 semanas de tratamiento se observó una mejoría del 83% de las lesiones en los pacientes que lograron concluir su tratamiento con imiquimod crema al 5%, mientras que los tratados con la loción polifenólica se observó una mejoría en el 95% de las lesiones, comparado con sus respectivos estados basales.
Desafortunadamente, inflamación inespecífica y eritema fueron observados durante el tratamiento con imiquimod, sobre todo cuando la piel estaba traumatizada por el rascado. Escaras, dolor y malestar fueron observados durante el tratamiento de las lesiones precancerosas con imiquimod, en especial en aquellos pacientes con lesiones muy extensas. Es importante resaltar que en aquellos pacientes que permanecieron en el estudio, a pesar de los efectos adversos antes señalados, la piel se recuperó sin dejar cicatrices. Los otros efectos secundarios, descritos en la literatura científica producidos por el Imiquimod, tales como cefalea, dolor de espalda, mialgias, cansancio, adenomagalias y diarrea no fueron observados en la presente investigación15-17.
Nuestro estudio es 100% original, pues no existen en la literatura científica publicaciones similares. Durante el tratamiento con polifenoles, bien sea en forma de loción o como crema protectora solar, los pacientes no manifestaron efectos adversos. Comparado con su estado basal, las mejorías a la tercera, sexta, novena y décimo sexta semana de tratamiento, tanto con imiquimod como con los polifenoles, fueron altamente significativas, lo que indica que los polifenoles constituyen una eficiente y segura alternativa para el tratamiento de la queratosis actínica y el cáncer de piel.
Investigaciones previas de nuestro laboratorio, demuestran que los polifenoles son altamente eficaces en el control de enfermedades autoinmunes que afectan la piel como la psoriasis (datos no publicados), así como enfermedades autoinmunes que afectan el sistema endocrino como la enfermedad de Graves y la diabetes tipo 1, por lo que intuimos que su mecanismo de acción farmacológico está relacionado con la inmunomodulación, pero sea cual fuere el mecanismo molecular de acción, el potencial de los polifenoles en la prevención del cáncer de piel es enorme, pues la prevalencia en los Estados Unidos para el año 2004 fue estimada en 39,5 millones con un costo anual de 1,04 billones de dólares, mientras que en Australia afecta entre 40 y 50% de la población mayor de 40 años18.
Por otro lado, este hallazgo además de ser una contribución al arsenal farmacológico involucrado en la prevención y tratamiento del cáncer de piel, constituye un paso importante en la lucha contra la dependencia científico-tecnológica en materia de medicamentos, pues además de ser los primeros en reportar tales efectos, las técnicas de aislamiento y purificación de las diversas fracciones polifenólicas obtenidas del aceite de oliva extravirgen y de otras fuentes del reino vegetal, así como la creación de las fórmulas utilizadas en la elaboración de las diversas presentaciones farmacéuticas utilizadas en el presente estudio, son producto de años de investigación en este campo del conocimiento.
Otro factor que probablemente esté mediando los efectos terapéuticos de los preparados farmacéuticos utilizados en el presente estudio, es el alto poder antioxidante de las mezclas polifenólicas utilizadas, que combinan las capacidades de penetración a las diferentes estructuras subcelulares de polifenoles derivados del estilbeno, flavonas y flavonoles presentes, tanto en la loción como en la crema protectora solar.
Conclusiones
Los polifenoles son tan eficaces como el imiquimod al 5% en el tratamiento de la queratosis actínica.
Los polifenoles, tanto en forma de loción como de crema protectora solar, no produjeron efectos adversos durante las 16 semanas de tratamiento de la queratosis actínica.
El 50% de los pacientes tratados con imiquimod crema al 5% abandonaron el tratamiento por los efectos adversos del mismo y por causas desconocidas.
El tratamiento con medicamentos basados en polifenoles constituye una alternativa segura y económica para la queratosis actínica.
Referencias
1. Duncan OK, Geisse JK. Epithelial precancerous lesions. In: Wolff K, Goldsmith LA, Katz SI, Gilchrest BA, Paller AS, Leffell DJ, editors. Fitzpatricks dermatology in general medicine. 7th ed. New York: McGraw-Hill; 2007. pp. 1007–1028. [ Links ]
2. Fenske NA, Spencer J, Adam F. Actinic keratoses: past, present and future. J Drugs Dermatol. 2010 May;9(5 Suppl):s45-49. [ Links ]
3. Neidecker MV, Davis-Ajami ML, Balkrishnan R, Feldman SR. Pharmacoeconomic considerations in treating actinic keratosis. Pharmacoeconomics. 2009;27(6):451-64. [ Links ]
4. Quatresooz P, Piérard-Franchimont C, Paquet P, Hubert P, Delvenne P, Piérard GE. Crossroads between actinic keratosis and squamous cell carcinoma, and novel pharmacological issues. Eur J Dermatol. 2008 Jan-Feb;18(1):6-10. [ Links ]
5. Stockfleth E, Kerl H; Guideline Subcommittee of the European Dermatology Forum. Guidelines for the management of actinic keratoses. Eur J Dermatol. 2006 Nov-Dec;16(6):599-606. [ Links ]
6. Moore AY. Clinical applications for topical 5-fluorouracil in the treatment of dermatological disorders. J Dermatolog Treat. 2009;20(6):328-35. [ Links ]
7. Shoimer I, Rosen N, Muhn C. Current management of actinic keratoses. Skin Therapy Lett. 2010 May;15(5):5-7. [ Links ]
8. Swanson N, Abramovits W, Berman B, Kulp J, Rigel DS, Levy S. Imiquimod 2.5% and 3.75% for the treatment of actinic keratoses: results of two placebo-controlled studies of daily application to the face and balding scalp for two 2-week cycles. J Am Acad Dermatol. 2010 Apr;62(4):582-90. [ Links ]
9. Yuchi C., Chang MD, et al. Current and Potential Uses of Imiquimod. Southern Medical Journal. Volume 98, Number 9, September 2005. Pags. 913-919. [ Links ]
10. Hemmi, H., et al. Small anti-viral compounds activate immune cells via the TLR7 MyD88-dependent signaling pathway. Nat Immunol. 2002 3(2):196-200. [ Links ]
11. Gaspari A, Tyring SK, Rosen T. Beyond a decade of 5% imiquimod topical therapy. J Drugs Dermatol. 2009 May;8(5):467-74. [ Links ]
12. Law MR, Morris JK. By how much does fruit and vegetable consumption reduce the risk of ischaemic heart disease?. Eur J Clin Nutr 1998;52: 549 – 56. [ Links ]
13. Higdon JV, Frei B. Tea catechins and polyphenols: health effects, metabolism, and antioxidant functions. Crit Rev Food Sci Nutr 2003;43: 89 – 143. [ Links ]
14. Yang CS, Landau JM, Huang MT, Newmark HL. Inhibition of carcinogenesis by dietary polyphenolic compounds. Annu Rev Nutr 2001;21: 381– 406. [ Links ]
15. Sauder D.N. Imiquimod: modes of action. British Journal of Dermatology, 2003; 149(Suppl. 66):5-8. [ Links ]
16. Miller R.L., et al. Imiquimod applied topically: a novel immune response modifier and a new class of drug. Int J Immunopharmacol. 1999 Jan;21(1):1-14. [ Links ]
17. Zeichner JA, Stern DWK, Uliasz A, Itenberg S, Lebwohl M. Placebocontrolled, double-blind, randomized pilot study of imiquimod 5% cream applied once per week for 6 months for the treatment of actinic keratoses. J Am Acad Dermatol 2009;60:59-62. [ Links ]
18. Roewert-Huber J, Stockfleth E, Kerl H. Pathology and pathobiology of actinic (solar) keratosisan update. Br J Dermatol 2007;157(Suppl 2): 18-20. [ Links ]