Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de la Facultad de Ingeniería Universidad Central de Venezuela
versión impresa ISSN 0798-4065
Rev. Fac. Ing. UCV v.23 n.3 Caracas sep. 2008
Estudio de la corrosión de una aleación Ti6Al4V utilizada como biomaterial.
SONIA CAMERO1, IVÁN TALAVERA1, GEMA GONZÁLEZ2, ROBERTO RÉQUIZ3, ADALBERTO ROSALES3, MARIBEL SUÁREZ1, JOSÉ LEÓN1, WILFRIDO GONZÁLEZ4
1 Universidad Central de Venezuela, Escuela de Ingeniería Metalúrgica y Ciencia de los Materiales, Venezuela.
2 Instituto Venezolano de Investigaciones Científicas (IVIC), Caracas, Venezuela
3 Universidad Simón Bolívar, Departamento de Materiales. Caracas, Venezuela
4 Universidad Simón Bolívar, Departamento de Tecnología Industrial. Caracas, Venezuela.
RESUMEN
En el presente trabajo se evaluó el comportamiento corrosivo de una aleación Ti6Al4V, a través de resistencia a la polarización lineal y curvas de polarización potenciodinámicas, obtenidas a partir de muestras que fueron expuestas previamente a 0, 180 y 360 horas de inmersión en una solución que simula el fluido corporal (FCS). Además, las muestras se caracterizaron mediante microscopía electrónica de barrido (M.E.B.) y microanálisis químico por espectroscopia de rayos X por dispersión en la energía (E.D.X.), en su condición de entrega y luego de ser ensayadas, de manera de evaluar los productos de corrosión formados y el daño generado. La caracterización microestructural reveló la presencia de una microestructura bifásica constituida por una matriz rica en Al (fase ![]() ) y una rica en V (fase
) y una rica en V (fase ![]() ), distribuida en los bordes de grano. Los resultados de los ensayos electroquímicos indican la disminución en el valor de la resistencia a la polarización lineal de las muestras expuestas durante 180 horas y 360 horas, así como la presencia de una doble película pasiva. La caracterización del daño por corrosión sobre las muestras ensayadas, indica el ataque preferencial de la fase a través de corrosión por picadura con respecto a la fase
), distribuida en los bordes de grano. Los resultados de los ensayos electroquímicos indican la disminución en el valor de la resistencia a la polarización lineal de las muestras expuestas durante 180 horas y 360 horas, así como la presencia de una doble película pasiva. La caracterización del daño por corrosión sobre las muestras ensayadas, indica el ataque preferencial de la fase a través de corrosión por picadura con respecto a la fase ![]() y corrosión microgalvánica.
y corrosión microgalvánica.
Palabras clave: Aleación Ti6Al4V, Polarización potenciodinámica, Fase ![]() , Fase
, Fase ![]() , Biomateriales.
, Biomateriales.
Corrosion study of Ti6Al4Valloy used such as biomaterial.
ABSTRACT
In the current work the corrosion behavior of a Ti6Al4V alloy was evaluated by linear polarization resistance and potentiodynamic polarization curves, in samples previously exposed to a solution of simulated body fluid (SBF) for 0, 180 and 360 h. The samples were characterized by scanning electron microscopy (S.E.M.) and energy dispersive X-ray spectroscopy (E.D.S.) in order to evaluate the corrosion products and the generated damage. The microstructural characterization revealed the presence of a two-phase microstructure, consisting of an aluminum phase ( phase ![]() ) and a vanadium phase ( phase
) and a vanadium phase ( phase ![]() ) located at the grain boundaries. Electrochemical tests showed decrease in the value of the linear polarization resistance in the samples exposed for 360 and 180 h and the presence of a double passive film. The characterization of the corrosion products in the tested samples indicated a preferential attack of the phase compare respect to phase
) located at the grain boundaries. Electrochemical tests showed decrease in the value of the linear polarization resistance in the samples exposed for 360 and 180 h and the presence of a double passive film. The characterization of the corrosion products in the tested samples indicated a preferential attack of the phase compare respect to phase ![]() by pitting corrosion and microgalvanic corrosion.
by pitting corrosion and microgalvanic corrosion.
Keywords: Ti6Al4V alloy, Potenciodynamics polarization, Phase ![]() , Phase
, Phase ![]() , Biomaterials.
, Biomaterials.
Recibido: abril de 2008 Recibido en forma final revisado: mayo de 2008
INTRODUCCIÓN
Las aleaciones de titanio ofrecen ventajas para el desarrollo de nuevas tecnologías, debido a sus excelentes propiedades mecánicas, alta resistencia a la corrosión, baja densidad especifica, elevado punto de fusión, etc. Esto ha permitido su utilización en la fabricación de implantes ortopédicos y prótesis dentales. La aleación Ti6Al4V combina una excelente resistencia mecánica con una gran capacidad de conformado, producto de su microestructura bifásica constituida por las fases α (rica en Al) y β (rica en V), donde la fase ofrece poca plasticidad y tiende a exhibir propiedades mecánicas y físicas anisótropicas, mientras que la fase β presenta buena conformabilidad debido a su alta ductilidad. Es por esto que la aleación Ti6Al4V es considerada la aleación estándar, contra la cual las demás aleaciones deben ser comparadas para una aplicación específica (Tamiselvi, 2006).
La compatibilidad biológica de un implante metálico está íntimamente vinculada a la respuesta tisular tolerante o intolerante, desencadenada por la alteración química que supone la inclusión y permanencia en el interior del organismo del implante y/o los productos corrosión. Es por ello que la presente investigación tiene como objetivo estudiar el comportamiento a la corrosión de la aleación Ti6Al4V bajo condiciones que simulen el cuerpo humano, con la finalidad de predecir la biocompatibilidad y la velocidad de corrosión en estas condiciones. Lo antes expuesto ha motivado la realización de diversos estudios (Pérez, 2004; Williams, 1990) en soluciones que simulan fluidos corporales, utilizando ensayos electroquímicos y los resultados han indicado que la resistencia a la corrosión se relaciona con la formación de una película pasiva estable, la cual al ser expuesta a un fluido corporal simulado interactúa formando una película de apatita (Pérez, 2004).
METODOLOGÍA EXPERIMENTAL
Preparación y caracterización microestructural de las muestras
El material ensayado en este estudio corresponde a muestras de una aleación Ti6Al4V en forma de barras, con un diámetro 1,27 cm en su condición de entrega (laminada en caliente, recocida y enfriada al aire). A dichas muestras, se realizaron cortes transversales para obtener discos de 1 cm de altura. Con la finalidad de corroborar la composición química de la aleación en estudio, se determinó el porcentaje en peso de los elementos Ti, Al, y V, mediante la técnica de espectrometría de emisión óptica con plasma acoplado inductivamente (ICP-OES), determinando el porcentaje en peso de los elementos antes mencionados. Para la caracterización microestructural mediante M.E.B., se siguió la preparación metalográfica convencional: las muestras se desbastaron con papel de carburo de silicio (No. 180, 240, 320, 400, 600, 1200 y 2000), posteriormente fueron pulidas con alúmina de 1 mm, 0,3 mm y 0,05 mm, sobre paños de tela sintética y por último, se atacaron por inmersión en el reactivo Krolls.
Resistencia a la polarización
La resistencia a la polarización y las curvas de polarización potenciodinámicas se obtuvieron con un potenciostato/ galvanostato de barrido, marca Gamry. Se utilizó un electrodo de calomelano saturado (ECS) como electrodo de referencia y de grafito de alta pureza como contraelectrodo. Las muestras fueron ensayadas, luego de ser sometidas a inmersión en una solución FCS cuya composición fue: NaCl 7,996g/L, NaHCO3 0,350 g/L, KCL 0,224 g/L, K2PO4.3H2O 0,228 g/L, MgCl2.6H2O 0,305g/L, CaCl2 0,278 g/L NaSO4 0,071 g/L, (CH2OH)3CNH2 6,057 g/L, durante 0, 180 y 360 horas, controlando la temperatura durante el ensayo mediante un baño termoestático. Las muestras con tiempo de exposición de 0 hora, se introdujeron directamente en la celda de trabajo a una temperatura de 37 °C y se midió el potencial de corrosión a circuito abierto (Eoc) por un lapso de 1 hora, antes de proceder a realizar los ensayos electroquímicos. Las muestras con tiempos de exposición de 180 y 360 horas, se introdujeron en la celda de trabajo con solución fresca a una temperatura de 37 °C, esperando un lapso de 10 min para estabilizar el Eoc, antes de aplicar las técnicas de polarización. Estos ensayos se realizaron por triplicado para cada una de las muestras esperando 10 min entre cada uno para permitir la estabilización del Eoc.
Los ensayos de resistencia a la polarización (Rp) se efectuaron, usando como referencia el procedimiento descrito en la norma ASTM G59-97 (ASTM G59-97, 1997), realizando el barrido con un potencial de -10mv a +10 mV con respecto al potencial (Eoc), con la finalidad de crear una menor perturbación, como es recomendado por Pérez (2004).
Los ensayos de polarización potenciodinámica se realizaron por triplicado, aireados a una temperatura de 37°C, para cada uno de los tiempos de exposición de las muestras en la solución SBF (0, 180 y 360 horas), el potencial inicial se estableció en E = -300 mV vs Eoc y el potencial final en E = 1600 mV vs ECS. La velocidad de barrido de potencial correspondió a 0,334 mV/s. Posteriormente, se realizó la caracterización de las superficies de las muestras ensayadas mediante M.E.B.
Caracterización de los productos de corrosión
Para determinar la morfología de los productos de corrosión, las muestras ensayadas fueron analizadas con un microscopio electrónico de barrido, marca Hitachi y para el microanálisis químico se empleó un espectrómetro de rayos X por dispersión en la energía marca EDAX, acoplado al microscopio electrónico. Posteriormente se evaluó el daño generado sobre la superficie, previa remoción de los productos formados durante los ensayos electroquímicos, utilizando el reactivo Krolls durante un intervalo de tiempo de 1- 2 min.
RESULTADOS Y DISCUSIÓN
Microestructura y análisis de fases
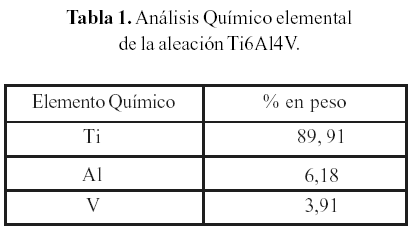
La tabla 1 presenta los resultados del análisis químico realizado a la aleación de Ti6Al4V mediante la técnica Espectrometría de Emisión Óptica con Plasma Acoplado Inductivamente (ICP-OES). Este análisis permitió determinar el porcentaje en peso de los elementos: titanio (Ti), aluminio (Al) y vanadio (V). A partir del mismo, se pudo corroborar que la aleación en estudio corresponde a una aleación designada como Ti6Al4V, la cual puede ser utilizada como biomaterial, siguiendo la especificación del porcentaje en peso de los elementos Al y V, descrita en la norma ASTMF136- 84 (ASTM 1984).
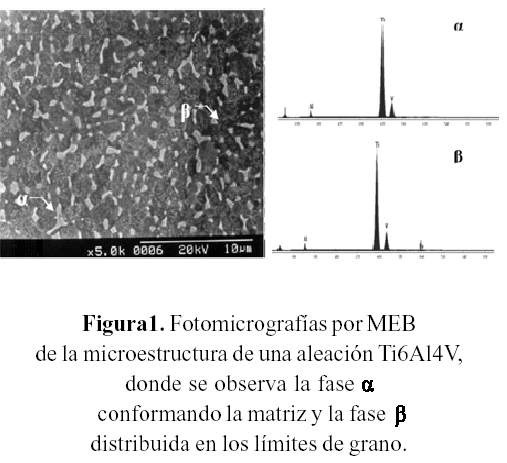
La caracterización microestructural por M.E.B.- EDX confirma la microestructura bifásica, constituida por una matriz de fase α (rica en Al) y con β (rica en V), ésta última distribuida en los bordes de grano, como se observa en la figura 1.
Peters et al. (1982), clasifican las aleaciones comerciales bifásicas (α + β) de titanio de acuerdo al arreglo geométrico de estas fases en: laminar, equiaxial y mixta (laminar y equiaxial), la cual es conocida como bimodal. Las estructuras laminares son controladas mediante tratamientos térmicos, en contraste con las estructuras equiaxiales y bimodales, las cuales requieren procesos de deformación adicional y subsecuentes aplicación de tratamientos de recocido.
Por otra parte, se debe destacar que la estructura bifásica es la que proporciona las mejores propiedades mecánicas a la aleación Ti6Al4V, requeridas para ser utilizadas como biomateriales (Rodríguez, 1996; Nylon, 1983; Rack, 2006). Sin embargo, es importante resaltar que estas estructuras son desarrolladas a partir de estructuras laminares, cuando se someten a tratamientos termomecánicos posteriores, los cuales deben ser rigurosamente controlados, con la finalidad de garantizar la homogeneidad y el tamaño de grano, además de la presencia de las dos fases.
El análisis microestructural por M.E.B. de la aleación, indica que ésta ha sido sometida a un proceso de deformación en caliente y luego a un tratamiento de recocido (700 ºC), seguido de un enfriamiento al aire, como así lo revela la microestructura de grano equiaxial y homogénea, con un tamaño de grano de de aproximadamente de 2,75 m, obtenida en la aleación analizada (Rodríguez, 1996; Peters, 1982). De acuerdo al análisis químico elemental realizado sobre las fases α y β, se revela la presencia de los elementos estabilizadores de cada una de estas fases: Al y V, respectivamente.
Resistencia a la polarización
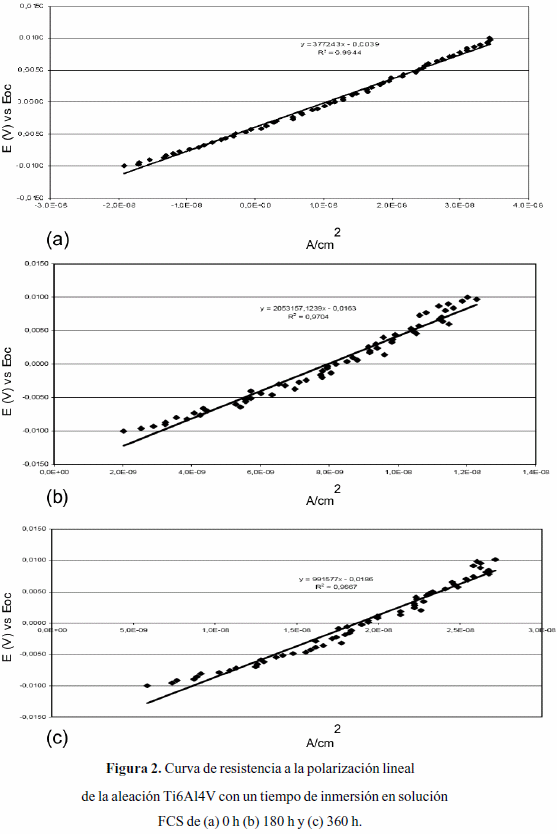
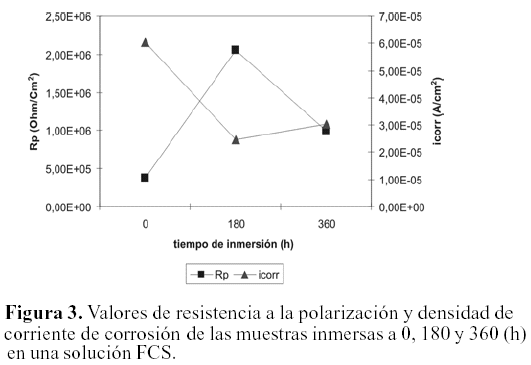
Las curvas de la resistencia a la polarización para cada una de las condiciones experimentales se pueden observar en la figura 2 y en la tabla 2 donde también se presentan los valores extraídos de estas curvas. Se puede observar que a medida que aumenta el tiempo de inmersión aumenta la resistencia a la polarización, y posteriormente disminuye para un tiempo de 360 horas. La disminución en el valor de la resistencia a la polarización entre las muestras expuestas durante 180 horas y 360 horas, se observa más claramente en la figura 3. Este efecto se asocia con la disolución del óxido de vanadio inducida por la presencia de iones Cl-, provenientes de la solución FCS, ocasionando la generación y difusión de vacancias en la película pasiva de la aleación (Metikos-Hukovic, 2003). De esta manera el fluido es capaz de penetrar y atacar la matriz constituida por la fase α, produciendo corrosión por picadura.
Polarización potenciodinámica
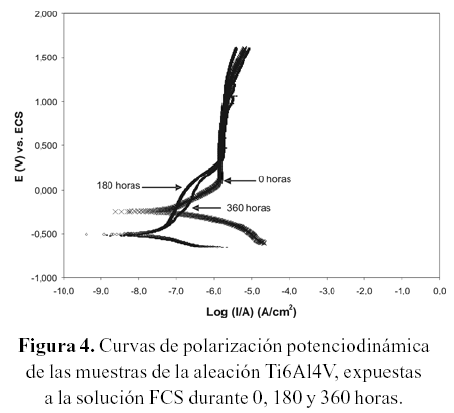
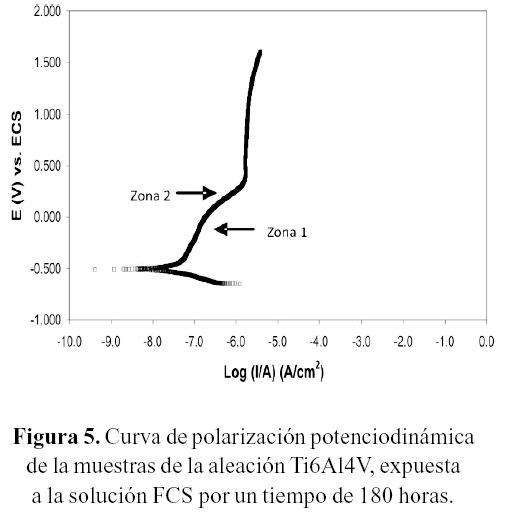
La figura 4, corresponde a las curvas de polarización potenciodinámica de las muestras expuestas a una solución de fluido corporal simulado (FCS) durante 0, 180 y 360 horas, respectivamente. De las curvas se observa que para los tiempos de inmersión de 0 hora, ésta presenta una zona activa hasta un potencial de aproximadamente 0,05V, a partir de este punto la curva presenta un valor de densidad de corriente relativamente constante, independientemente del incremento de potencial, asociado a la formación de una capa de óxido de titanio estable. Para los tiempos de exposición de 180 y 360 se observa un cambio en la forma de la curva presentando dos zonas bien definidas, en un intervalo de potenciales de 0,050V y 0,3V, como se observa en la figura 5. La zona 1 estaría relacionada a la formación y presencia de una película de apatita, producto de la interacción de la solución con la película de óxido de titanio, pudiendo considerarse como una región pasiva y la zona 2 se relaciona con la disolución de esta película, la cual corresponde a la corrosión del metal (zona activa) antes de que se genere la película pasiva de óxido de titanio (figura 5). Esta interpretación es coherente con los resultados presentados en los estudios de González (1999), en los cuales proponen como mecanismo de corrosión en aleaciones comerciales de titanio, la formación de una doble película de productos, donde la película más externa corresponde a una película porosa de apatita y la más interna corresponde a una película de óxido de titanio.
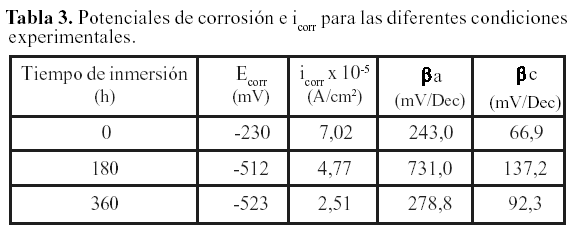
Considerando las curvas de polarización potenciodinámicas obtenidas a 0, 180 y 360 horas de exposición en la solución de fluido corporal simulado (figura 4), se observa que el potencial de corrosión de las muestras expuestas a 180 y 360 horas varía, desplazándose a valores más negativos a medida que aumenta el tiempo de inmersión en la solución FCS, como se puede observar en la tabla 3. El comportamiento corrosivo de la aleación estudiada se puede atribuir a la disolución inicial de la fase α rica en aluminio, la cual desplaza el potencial de corrosión (Ecorr) a valores más negativos. Además, se tiene que en las tres condiciones de ensayo (0, 180, 360 horas), los potenciales de corrosión (Ecorr) son significativamente menores a los medidos en el potencial a circuito abierto (Eoc). Por otra parte, icorr disminuye con respecto al tiempo de inmersión de las muestras en FCS, obteniendo el valor mayor para las muestras expuestas durante 0 hora; icorr = 7,025 x 10-8 A/cm2 y el menor valor para las muestras expuestas durante 360 horas; icorr = 2,51 x 10-8 A/cm2. Tanto en las Rp como las curvas de polarización se pudo observar que para los tiempos de inmersión de 180 como para las 360 horas el icorr es menor que a 0 hora. Este comportamiento se puede atribuir a un engrosamiento de la película pasiva durante el tiempo de inmersión de las muestras, antes del inicio de los ensayos electroquímicos. Las muestras previamente expuestas durante 0 hora a la solución FCS presentarían un estado pasivo con una película delgada de óxido de titanio, alcanzando un mayor valor de icorr en la solución (tablas 2 y 3).
Es importante resaltar, que para la condición de 360 h de inmersión la Rp disminuye considerablemente, con respecto a la condición de 180 h, mostrando un aumento en el icorr, lo que parece indicar que la capa de apatita que se formó es una capa porosa, la cual permite el paso de la solución a través de la misma.
Caracterización de los productos de corrosión
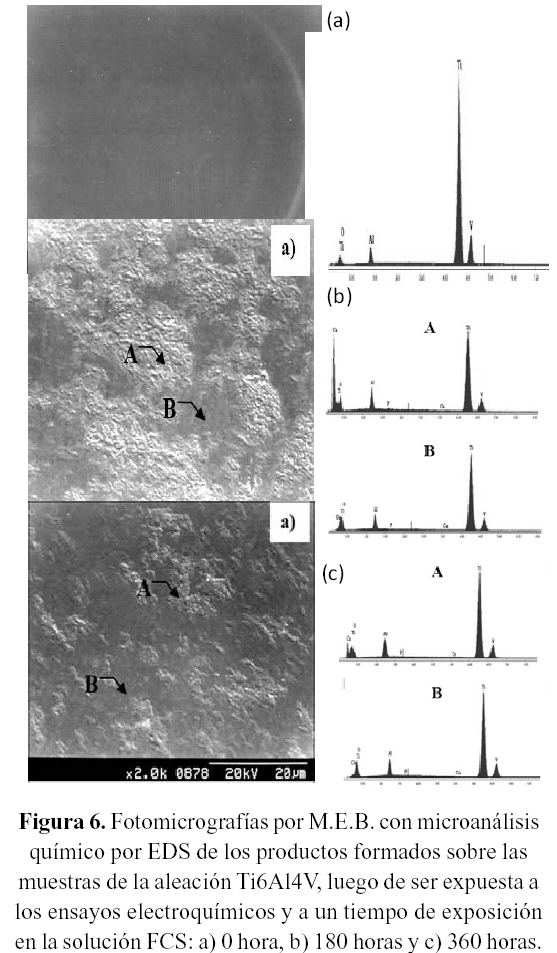
La figura 6, corresponde a las fotomicrografías obtenidas por M.E.B., de las muestras Ti6Al4V, después de un tiempo de exposición en la solución FCS y posterior a los ensayos electroquímicos. A 0 hora (figura 6a), se observa una superficie constituida por una película de productos de corrosión densos y homogéneos, la cual se presenta sobre toda la superficie ensayada. Como ha sido mencionado anteriormente (Tamiselvi, 2006), esta película que transfiere una alta resistencia a la corrosión, es producto de las reacciones anódicas que suceden durante los ensayos de polarización potenciodinámicos. Este fenómeno favorece la formación de diferentes tipos de óxidos (TiO, TiO2 y Ti2O3), siendo más probable la formación del TiO2 (De Assis, 2006).
La figura 6b, corresponde a una muestra después de un tiempo de exposición en la solución FCS de 180 horas y posterior a los ensayos electroquímicos. En dicha figura se resaltan zonas claramente diferenciadas, las zonas oscuras, corresponden posiblemente al óxido de titanio formado durante los ensayos electroquímicos y las zonas claras, tienden a describir las segregaciones de apatita, debido a la interacción de la solución FCS con el óxido de titanio (Elagli, 1967; Tamiselvi, 2006; Metikos-Hukovic, 2003), confirmado con los resultados de E.D.X. cuyos % Ca y %P se encuentran asociados a la disolución de apatita, promovido con la polarización aplicada, deduciéndose que estamos detectando los residuos de la misma.
La figura 6c, corresponde a una muestra de Ti6Al4V, después de 360 horas y posterior a los ensayos electroquímicos, se puede observar que al igual que en el caso de 180 horas, existen zonas claramente definidas, siendo las zonas oscuras óxido de titanio y las zonas claras segregaciones de los productos de apatita, formados por la interacción de la película de óxido de titanio con la solución FCS.
Al comparar el comportamiento de la aleación de las muestras expuestas a 180 y 360 horas, se observa una menor cantidad de productos segregados en las muestras expuestas durante 360 horas con respecto a las de 180 horas. Este hecho sugiere que la película de productos formados es inestable y para tiempos de exposición más prolongados, puede llegar a disolverse. Estos resultados concuerdan con los obtenidos por Tamilselvi (2006), quien observó la presencia de Ca y P en muestras expuestas a la solución de Hanks durante 240 y 360 horas, asociando la presencia de estos elementos a la interacción de la solución con la película de óxido de titanio formada en las superficies de las muestras.
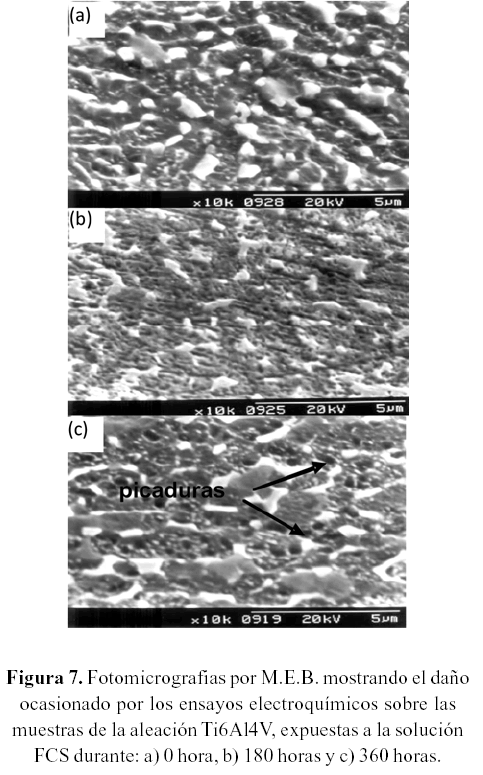
Cuando se compara la microestructura de la muestra en condición de entrega (figura 1), con la microestructura de la muestra ensayada electroquímicamente (figura 7), se puede observar que la fase α es atacada preferencialmente con respecto a la fase β. Según diversos estudios (Tamiselvi, 2006), el óxido de vanadio formado sobre la superficie de la aleación, tiende a disolverse por la presencia de iones Cl-, por lo que una disolución preferencial se esperaría de la fase β, que corresponde a la fase rica en vanadio. Sin embargo, esta disolución ocurre una vez formada la película pasiva de la aleación Ti6Al4V, mientras que la disolución de la fase α ocurrirá antes y después de la formación de la película pasiva.
Las figuras 7b y 7c correspondientes a los ensayos de 180 y 360 horas, permiten diferenciar las zonas donde hay restos de la película y otras zonas donde se resalta el daño generado sobre la superficie. De lo anterior, resulta necesario destacar las picaduras observadas y su distribución en la matriz, este ataque puede describirse como corrosión localizada (picaduras y corrosión microgalvánica). Este proceso es activado por la disolución del óxido de vanadio (Metikos- Hukovic, 2003) presente en la película pasiva, generando porosidades en ésta, las cuales permiten el paso de la solución FCS que contiene iones Cl-, así como por la diferencia de potenciales existentes entre las fases, acelerando la disolución de la fase más activa.
CONCLUSIONES
El mecanismo de corrosión observado en las muestras de aleación Ti6Al4V corresponde a un ataque preferencial de la fase , manifestándose como picaduras y corrosión microgalvánica, debido a la microestructura bifásica de la aleación, lo cual generó una diferencia de potencial entre las fases presentes.
Las técnicas electroquímicas de polarización estudiadas permiten inferir la tendencia corrosiva del material, siendo mayor con el incremento del tiempo de inmersión.
La película pasiva de la aleación Ti6Al4V, tiende a ser inestable en presencia de iones cloruros, incidiendo en la disolución preferencial del vanadio.
La aleación Ti6Al4V forma agregados de apatita en su superficie por interacción de la película de óxido de titanio con la solución de fluido corporal simulado (FCS), durante largos periodos de exposición.
AGRADECIMIENTOS
Los autores desean agradecer al Fondo Nacional de Ciencia y Tecnología, FONACIT, por el soporte financiero al proyecto de Grupo G-2001000900 y al Centro de Microscopia Electrónica de la Facultad de Ingeniería, Universidad Central de Venezuela por el apoyo prestado en la caracterización microestructural y productos de corrosión.
REFERENCIAS
1. ASTM-G59-97. Standard Test Method for Conducting Potentiodynamic Polarization Resistance Measurements. Annual book of ASTM standards. [ Links ]
2. ASTM-F136-84. Standar Specification for Wrought Ti-6Al- 4V Alloy for surgical implant Aplications. Annual book os ASTM standars. [ Links ]
3. CAMERO, S., RODRÍGUEZ, C., YÉPEZ, U. (1996). Tratamientos Térmicos y relación microestructura-dureza en una aleación Ti-4,5Al-3V». Rev. Fac. Ingeniería-UCV, Vol.13, No. 2, (1998). ISSN 0798-4065. [ Links ]
4. DE ASSIS, S.L., WOLYNEC, S., COSTA, I. (2006). Corrosion characterization of titanium alloys by electrochemical techniques. Electrochimica Acta, 51, 1815–1819. [ Links ]
5. ELAGLI, K., TRAISNEL, M., HILDEBRNAD, H.F. (1993). Electrochemical behavior of titanium and dental alloys artificial saliva. Electrochemica Acta, 38, 1769-1774. [ Links ]
6. GONZÁLEZ, J., ROSCA, J. (1999). Study of the corrosion behavior of titanium and some of its alloys for biomedical and dental implant applications. J. Electroanal. Chem., 471, 109. [ Links ]
7. METIKOS-HUKOVIC, M., KWOKAL, A., PILJAC, J. (2003). The influence of niobium and vanadium on passivity of titanium-based implants in physiological solution. Biomaterials; 24, 3765. [ Links ]
8. NYLON, D., FROES, F.H., GARDINER, R.W. (1983). Developments in Titanium Alloy Casting Technology. Journal of Metals, February, 35-45. [ Links ]
9. PEREZ, N. (2004). Electrochemistry and Corrosion Science. Kluwer Academic Publishers. Boston. 27-40, 167-185. [ Links ]
10. PETERS, M., LÜTJERING, G., ZIEGIER. G. (1982). Control of Microstructures of ( + ) - Titanium Alloys. Eingegangenam, 12, Julio. [ Links ]
11. RACK, H. J. & QAZI, J.I. (2006). Titanium alloys for biomedical applications. Materials Science and Engineering C, 26, 1269-1277. [ Links ]
12. SHUKLA, A. K., BALASUBRAMANIAM, R., BHARGAVA, S. (2005). Properties of passive film formed on CP titanium, Ti–6Al–4V and Ti–13.4Al–29Nb alloys in simulated human body conditions. Intermetallics, 13, 631–637. [ Links ]
13. TAMILSELVI, S., RAMAN, V., RAJENDRAN, N. (2006). Corrosion behaviour of Ti–6Al–7Nb and Ti–6Al–4V ELI alloys in the simulated body fluid solution by electrochemical impedance spectroscopy. Electrochimica Acta, 52, 839–846. [ Links ]
14. WILLIAMS, D. (1990). Concise encyclopedia of medical and dental materials. 1ra ed., Pergamon Press, New York. [ Links ]