Servicios Personalizados
Revista
Articulo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Accesos
Accesos
Links relacionados
-
 Similares en
SciELO
Similares en
SciELO
Compartir
Revista de la Facultad de Ingeniería Universidad Central de Venezuela
versión impresa ISSN 0798-4065
Rev. Fac. Ing. UCV v.24 n.2 Caracas jun. 2009
Oxidación electroquímica de compuestos orgánicos de un efluente proveniente de una planta procesadora de productos lácteos
María E. Méndez, José I. Briceño, Aura M. González
Universidad de los Andes, Facultad de Ingeniería, Estado Mérida – Venezuela
e-mail: mendezme@ula.ve
RESUMEN
La descontaminación de efluentes líquidos por vía electroquímica es un procedimiento alternativo y complementario empleado frecuentemente en la actualidad. En Venezuela, el desarrollo de las industrias lácteas viene acompañado de un incremento en los efluentes caracterizados por altos valores de demanda química de oxígeno (DQO). La presente investigación plantea un método electroquímico para la reducción por degradación del contenido orgánico de las corrientes provenientes de la producción quesera (suero). Se analizan comparativamente los efectos sobre la descontaminación de la técnica oxidativa (potencial cíclico y potencial constante) y la hidrodinámica (con y sin agitación). La descontaminación es monitoreada mediante la medición en el tiempo de la DQO y del porcentaje de nitrógeno proteico. La remoción de materia orgánica tiene lugar mediante dos mecanismos simultáneos consistentes en oxidación electroquímica sobre la superficie del electrodo de platino y oxidación química por el par redox Cl-/Cl2. Entre las técnicas de tratamiento evaluadas la correspondiente a potencial constante resultó más eficiente que la efectuada a potencial cíclico. La agitación incluida en el reactor incrementó la degradación general de compuestos orgánicos pero perjudicó la transformación proteica motivado a que parte de las sustancias nitrogenadas son eliminadas por precipitación.
Palabras clave: Tratamiento de efluentes líquidos, Descontaminación, Electroquímica, Industria láctea, Reactor electroquímico, Electroxidación.
Electrochemical oxidation of organic compounds in effluents from a milky process plant
ABSTRACT
Liquid effluents treatment by electrochemical oxidation is an alternative method actually used. In the present investigation, the aim is to deplete the chemical oxygen demand (COD) and protein nitrogen values in waste water from dairy industry. The method consists in oxidation processes of milk serum using constant and cyclic potential and, in rest and stirred condition. Part of protein nitrogen is separated as solid precipitate and agitation affects nitrogen compounds diminution. In general a stirred system benefits depletion of COD and constant potential treatment is the most efficient for electrochemical oxidation.
Keywords: Liquid effluents treatment, Electrochemical oxidation, Milky process plant, Electrochemical Reactor, Electroxidation.
Recibido: octubre de 2007 Recibido en forma final revisado: febrero de 2009
INTRODUCCIÓN
El tratamiento electroquímico de aguas residuales es una tecnología fundamentada en la degradación oxidativa de compuestos químicos a través de reacciones anódicas. En los últimos años, uno de los campos de la ingeniería electroquímica que se está desarrollando es el tratamiento de efluentes industriales, por su gran atractivo para dar solución a los problemas medioambientales. Ya que la mayoría de las sustancias son electroquímicamente activas, la electrólisis se presenta como una opción viable para el tratamiento de descontaminación tanto en efluentes líquidos y sólidos, como en gaseosos.
La electroquímica como técnica de tratamiento permite tanto la eliminación como la regeneración de especies, y utiliza como materia prima del proceso, un reactivo limpio: la energía eléctrica o vector de descontaminación ambiental. El proceso electroquímico permite tratar una gran variedad de efluentes industriales (incluso de alta toxicidad) y es especialmente efectivo en los poco o nada biodegradables donde realiza disminuciones de la DQO de hasta el 95% (Pletcher, 1984; Cominellis, 1993, 1994; Szpykowicz, 2001).
En muchos de los procedimientos de oxidación electroquímica la degradación puede completarse por vía química cuando se está en presencia de un par redox, usualmente Cr(IV)/Cr(II), Ce(IV)/Ce (III), Cl(-I)/Cl2. En general, los efluentes presentan un alto contenido de cloruro de sodio disuelto, aprovechando esta característica y bajo condiciones oxidativas apropiadas, se genera el cloro gaseoso en el medio produciendo la desinfección del efluente. Por otro lado, esta tecnología cuando se aplica parcialmente a corrientes no biodegradables puede hacerlas biodegradables, lo que permite su conexión a tratamientos biológicos (Crites, 2000; Díaz, 2003).
Durante los últimos tiempos las industrias Lácteas venezolanas se han desarrollado en gran escala, y el suero siempre ha sido uno de sus desechos más problemáticos, es por ello que todos los esfuerzos se han concentrado en su tratamiento y/o aprovechamiento para generar productos de mayor valor agregado, disminuyendo así los problemas de contaminación ambiental generados por su descarga a los cuerpos hídricos (Grasselli, 1997).
TÉCNICAS EXPERIMENTALES
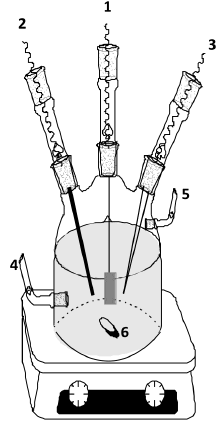
El presente estudio está centrado en la selección y caracterización de un efluente (Suero) proveniente de Lácteos Santa Rosa (estado Mérida, Venezuela). Posteriormente el efluente es sometido a un tratamiento de electrooxidación usando dos procedimientos separados, uno mediante ciclos oxidativos y el segundo a potencial constante. Como otra variante del proceso se incluyó la agitación de la solución durante el tratamiento para evaluar su efecto sobre la eficiencia de la oxidación. La finalidad de ambos tratamientos es la degradación de compuestos orgánicos que de otra manera irían a engrosar la cantidad de contaminantes en las corrientes hídricas. El proceso es llevado a cabo en un equipo elaborado en vidrio, de forma cilíndrica con capacidad para 250 ml de muestra, integrado por tres electrodos sólidos, uno de platino (ánodo), uno de grafito (cátodo) y el de plata/ cloruro (referencia). Esta unidad posee un ducto para el suministro de cualquier gas inerte que se necesite en el proceso (figura 1). Los programas de potencial empleados fueron aplicados mediante un Potenciostato EG&G modelo 273 acoplado a un ordenador con el programa EG&G PAR 270.
Figura 1. Esquema del reactor electroquímico. (1) Electrodo de trabajo: lámina y alambre de platino (2) Contraelectrodo: barra de grafito (3) Electrodo de referencia: Ag/AgCl no comercial. Todos los electrodos empotrados en vidrio y unidos a su respectivo conductor de cobre. (4) y (5) Entrada/Salida para fluidos. (6) Agitador magnético.Entrada/Salida para fluidos. (6) Agitador magnético.
Las técnicas y métodos usados en la caracterización del efluente (suero lácteo), son las que se emplean de manera rutinaria en la evaluación de efluentes industriales según los métodos estándar para el análisis de aguas residuales y los procedimientos descritos en los manuales de procesamiento de productos lácteos (Apha, 1994; Daufin, 1974; Grasselli, 1997; Lugo, 1996; Metcal, 1995; Nemerow, 1977).
El suero fue recolectado, filtrado al vacío y caracterizado mediante la determinación del pH (pH- meter- Hanna Instruments H19321), la conductividad eléctrica (Metrohm Conductometro 644) y la concentración de cloruros determinada mediante el método de precipitación empleando nitrato de plata (Merck 96 %) en la preparación de la solución valorante. Posteriormente el suero fue refrigerado para evitar su degradación. Las variables de operación consideradas en el análisis y el monitoreo del proceso oxidativo fueron: la demanda química de oxigeno (DQO) y el contenido de nitrógeno proteico (% p/p N). La DQO se determinó por oxidación con acido sulfúrico concentrado (Fluka 98%), dicromato de potasio (Fluka – 1º), una solución digestora (Fluka 98 %) y empleando un Reactor Hach Cod y un Espectrofotómetro Hach. El porcentaje de nitrógeno se determinó mediante el método Kjeldahl usando en las soluciones de ese análisis acido sulfúrico concentrado (Fluka 98%) y NaOH (Merck 98%).
RESULTADOS Y DISCUSIÓN
El efluente empleado corresponde al suero producido luego de la elaboración del queso Bonzalú, queso de pasta blanda y coagulado vía enzimática por lo que se clasifica el efluente como lactosuero del tipo dulce. En la tabla 1 se muestran los datos correspondientes a la caracterización del mismo.
Tabla 1. Caracterización del lactosuero estudiado.

Conocida la concentración de cloruros en el efluente seleccionado, se preparó una solución con la misma concentración (2,75 % p/p NaCl) y pH (5,8), con la finalidad de definir el rango de potenciales oxidativos para el tratamiento cíclico y a potencial constante. Inicialmente se realizó una voltametría cíclica entre 0,00 V y 2,75 V (vs Ag/AgCl). La selección de estos valores de potencial se fundamenta en que ellos garantizan los siguientes procesos electroquímicos en el ánodo de platino:
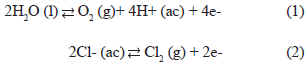
Los gases generados son participantes activos en reacciones de oxidación química.
Oxidación cíclica de compuestos orgánicos contenidos en el lactosuero
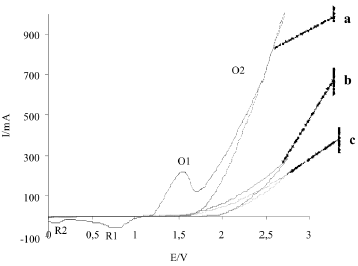
En la figura 2, curva "a" se representa el resultado de la voltametría cíclica realizada a la solución en reposo de concentración 2,75 % p/p NaCl. Las señales O1 a 1,5 V y R1 a 0,75 V corresponden a los procesos de adsorción y desorción del oxígeno sobre la superficie de platino; mientras que O2 representa los procesos combinados de evolución gaseosa del oxígeno y del cloro, R2 es la desorción de cloruros (Morales, 1992). El efecto de la agitación sobre el sistema se muestra en la curva "a" de la figura 3, los procesos oxidativos del agua y de los cloruros se ven incrementados mientras que los reductivos disminuyen su intensidad. La razón de tal fenómeno es que los gases generados (O2 y Cl2) son rápidamente disipados por la turbulencia de la superficie del electrodo, desplazando el equilibrio hacia los productos en las reacciones correspondientes. Ambas reacciones (ecuaciones (1) y (2)) son paralelas a su vez a la degradación electroquímica de algunos compuestos orgánicos (RE) como proteínas, azúcares y ácidos presentes en el lactosuero, a especies con mayor estado de oxidación (OX) (ecuación (3)) (Szpyrkowicz, 2001).
![]()
Figura 2. Corriente I/mA vs. potencial E/V del tratamiento oxidativo cíclico sin agitación, entre 0 V y 2,75V vs Ag/AgCl no comercial, velocidad de barrido: 50 mV/s. Se incluye el tratamiento de una solución de concentración 2,75 % p/p NaCl, pH=5,8 (a), el primer (b) y último(c) ciclo efectuado al suero lácteo.
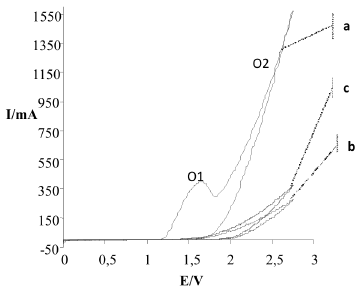
Figura 3. Corriente I/mA vs. potencial E/V del tratamiento oxidativo cíclico con agitación, entre 0 V y 2,7V vs Ag/AgCl no comercial, velocidad de barrido: 50 mV/s. Se incluye el tratamiento de una solución de concentración 2,75 % p/p NaCl, pH=5,8 (a) y el primer (b) y ultimo (c) ciclo efectuado al suero lácteo.
En las curvas "b" y "c" de las figuras 2 y 3 se muestran el primer y último ciclo de oxidación en reposo y agitado del efluente (suero lácteo), respectivamente. Debido al bloqueo del electrodo por parte de las moléculas orgánicas presentes, se observaron disminuida la intensidad de la corriente y suprimida la respuesta superficial del platino. En el sistema en reposo, la obstrucción superficial del electrodo persistió acentuándose con el tiempo ocasionando un decremento progresivo en la corriente (curva "c", figura 2); las interferencias pueden ser causadas tanto por acumulación en las cercanías del electrodo de las especies orgánicas originales como de los productos de las reacciones. El efecto de la agitación sobre el proceso oxidativo se manifiesta en el registro de una intensidad de corriente superior y siempre en aumento en comparación a la observada en el sistema en reposo (curvas "b" y "c", figura 3). Al igual que en el sistema con sólo cloruro de sodio a pH 5,8 la agitación mejora el transporte de los productos de las reacciones favoreciendo así las transformaciones electródicas (ecuaciones (1), (2) y (3)).
Oxidación a potencial constante de compuestos orgánicos contenidos en el lactosuero
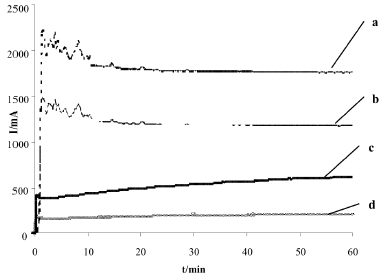
El potencial de oxidación empleado para la degradación de las sustancias orgánicas presentes se obtiene directamente de la voltametría cíclica realizada a la solución con 2,75 % p/p NaCl, este valor garantiza la completación de las reacciones correspondientes a las ecuaciones (1), (2) y (3). En la figura 4 se muestran las curvas derivadas de la electrólisis, las curvas "a" y "b" de la misma figura representan el tratamiento a potencial constante de la solución con 2,75 % p/p NaCl con y sin agitación, respectivamente. La señal correspondiente al sistema agitado presenta mayores intensidades de corriente debido a que la turbulencia moviliza los productos de las reacciones desplazando los equilibrios de las ecuaciones (1) y (2) hacia los productos. En ambos casos para los tiempos iniciales se aprecia una señal irregular producto de la evolución de los gases O2 y Cl2, que es más intensa antes de la formación de óxidos de platino sobre la superficie. Las curvas "c" y "d" de la figura 4 representan el resultado de los procesos con y sin agitación del suero, respectivamente; de manera análoga al sistema anterior, el tratamiento agitado exhibe un valor de corriente mayor. Cuando se procesa el suero lácteo la intensidad de las corrientes disminuye considerablemente motivado al bloqueo superficial por parte de las moléculas orgánicas y a la mayor viscosidad del medio que incide directamente en el transporte de las especies.
Figura 4. Corriente I/mA tiempo t/s del tratamiento oxidativo con y sin agitación a potencial constante 2,75V vs Ag/AgCl no comercial, tiempo de proceso: 60 min. Se incluye el tratamiento de una solución de concentración 2,75 % p/p NaCl, pH=5,8 con (a) y sin (b) agitación y, del suero lácteo con (c) y sin (d) agitación.
Oxidación química acoplada a los procesos de electrodegradación de compuestos orgánicos
Cuando ocurre generación de Cl2 en sistemas acuosos, es característica la siguiente reacción química:
![]()
En la que el ácido clórico (I) puede actuar como oxidante químico de las especies orgánicas (RE) a otros compuestos orgánicos de mayor estado de oxidación (OX) según:
![]()
La degradación química conseguida a partir de la reacción anterior, requiere bajos valores de pH para su consecución, de manera que la neutralización del medio afecta el mecanismo químico de oxidación (Szpyrkowicz, 2001). La transformación de las sustancias orgánicas en condiciones apropiadas tiene lugar paralelamente a la electroquímica.
La descomposición de las especies orgánicas presentes en el lacto suero por vía química y electroquímica fue monitoreada mediante la medición de la variación con el tiempo de parámetros (C) como demanda química de oxígeno (DQO) y porcentaje de nitrógeno proteico (% p/p N). Los valores correspondientes fueron normalizados respecto a los valores iniciales (Co), mediante la relación C/Co. Los resultados de los procedimientos a potencial cíclico y constante se muestran en las figuras 5 y 6, respectivamente. En ambos tratamientos oxidativos a partir de los 30 min de operación se observó la precipitación de un sólido blanco nebuloso, el análisis de nitrógeno proteico reveló un promedio de 6,22 % p/p N. Las pruebas cualitativas de solubilidad determinaron que las proteínas precipitadas pertenecen al grupo de las albúminas, el cual está conformado por la α-lactoalbumina, la β-lactoglobulina y la Seroalbumina; demostrándose que parte de los compuestos nitrogenados son separados del suero por efecto de la precipitación proteica (Daufin, 1974; Guzmán, 1988). Lo anteriormente expuesto se ve reforzado por el comportamiento de la variación del % N p/p proteico durante la oxidación (figuras 5 y 6), en donde se ve una abrupta disminución del mismo en el suero lácteo a partir de los 30 minutos de proceso.
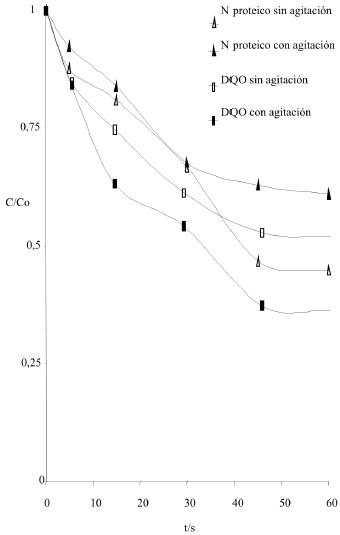
Figura 5. Concentraciones normalizadas DQO/DQOo y Porcentaje N/Porcentaje No en función del tiempo t/s obtenidas de un tratamiento oxidativo con potenciales cíclicos en condiciones de reposo y agitada.
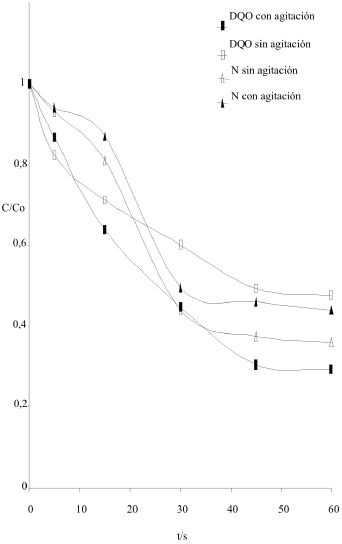
Figura 6. Concentraciones normalizadas DQO/DQOo y %N/%No en función del tiempo t/s obtenidas de un tratamiento oxidativo con potencial constante en condiciones de reposo y agitada.
En la figura 5 se representan los resultados obtenidos del tratamiento de oxidación cíclica, los valores correspondientes a la DQO corroboran que la agitación favorece la degradación general de compuestos orgánicos, este tipo de fenómeno evidencia que el mecanismo de oxidación electroquímico predomina sobre el químico. En contraposición, la descomposición de sustancias nitrogenadas ocurre en mayor grado en sistemas en reposo que en los agitados, ya que los primeros mantienen las condiciones óptimas de pH y concentración de cloro activo en las cercanías del ánodo para llevar a cabo una oxidación química eficiente. Aunado a lo anterior, la precipitación proteica es un fenómeno principalmente dependiente del pH, aparentemente, el sistema invierte aproximadamente 30 minutos para acondicionar las inmediaciones del ánodo para que la coagulación ocurra. Es evidente que la turbulencia del medio introduce alteraciones en los perfiles de concentración de H+ que afectan la precipitación.
En la figura 6, se muestran los resultados obtenidos del tratamiento a potencial constante, en general la degradación de compuestos orgánicos bajo estas condiciones fue superior a la conseguida por la oxidación cíclica motivado a que el ambiente oxidativo se mantuvo durante todo el tratamiento sin experimentar fluctuaciones. Por otro lado la evolución gaseosa permanente garantizó la generación del cloro activo necesario para llevar a cabo la oxidación química. En la figura 7 se incluyen los porcentajes de remoción de DQO y % p/p N, en ella se destaca que el proceso a potencial constante involucra los rendimientos más altos para la degradación y que la remoción de compuestos orgánicos es superior cuando la hidrodinámica del reactor corresponde a sistemas en reposo. La degradación general de sustancias orgánicas (DQO) se ve favorecida cuando se incluye la agitación en el medio.
Figura 7. Gráfico comparativo de los porcentajes de remoción de DQO y Nitrógeno proteico en función de las variantes del tratamiento oxidativo
Se ha demostrado que son posibles los procesos de oxidación directa e indirecta de los compuestos orgánicos y que los electrones intercambiados en las reacciones anódicas involucran varias combinaciones químicas además del bloqueo superficial del platino producto de la naturaleza del efluente (Szpyrkowicz, 2001). Con base a lo anterior, resulta difícil proponer un balance que modele por separado los factores antes expuestos, por esa razón, para describir las variables consideradas en el proceso (% p/p N y DQO) se plantea una ecuación para cada parámetro en función de una constante aparente (kN y kDQO) y un pseudo orden de reacción (nN y nDQO) :
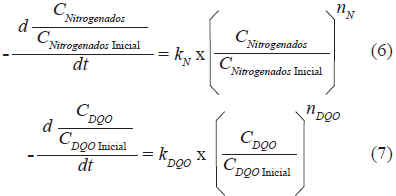
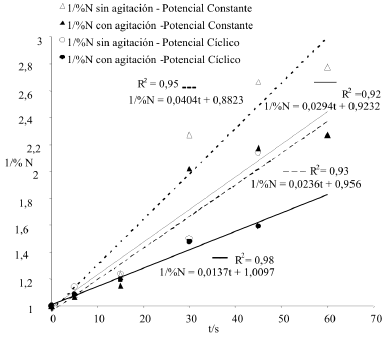
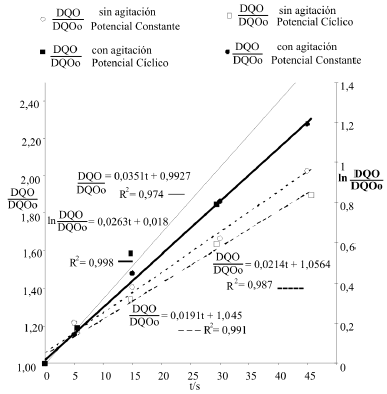
A partir de los datos experimentales correspondientes a la variación del porcentaje de nitrógeno proteico se construye la figura 8. En ella se representan los resultados obtenidos de los procesos a potencial constante y variable, con y sin agitación. De la manipulación de los datos efectuada se obtiene que la cinética de la degradación del nitrógeno proteico obedece a un pseudo segundo orden (nN) y el valor de la pseudo constante de reacción (kN) se ve afectado por las variables del proceso (agitación y condiciones de oxidación). De manera análoga, los resultados obtenidos de la variación de la DQO con el tiempo fueron representados en la figura 9 evidenciándose un pseudo segundo orden de reacción para los tratamientos a potencial variable agitado y sin agitar. En el caso del proceso a potencial constante, el sistema en reposo mostró un pseudo segundo orden mientras que en presencia de agitación las restricciones de la degradación de compuestos orgánicos disminuyeron presentando un pseudo primer orden.
Figura 8. Efecto del tratamiento oxidativo sobre la pseudoconstante de reacción de la remoción de nitrógeno proteico (ecuación (6)) obtenida en cada uno de los tratamientos. Pseudorden de reacción nN≈2.
Figura 9. Efecto del tratamiento oxidativo sobre la pseudoconstante y el pseudorden de reacción de la remoción de DQO (ecuación 7) obtenidas en cada uno de los tratamientos.
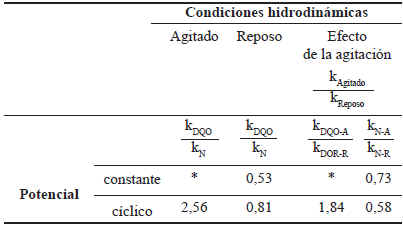
En la tabla 2 se muestra la relación entre las constantes de pseudo segundo orden de reacción para la remoción de DQO (kDQO) y nitrógeno proteico (k%N) a diferentes condiciones hidrodinámicas y programas de potencial oxidativo. Cuando la oxidación es cíclica, la relación relativa kDQO/kN, aporta información sobre la selectividad del reactor para la degradación general de sustancias orgánicas (DQO) en comparación con la remoción de compuestos proteicos (% p/p N); encontrándose que en sistemas agitados predomina la remoción de DQO sobre la de las proteínas de manera que si se desea descomponer compuestos nitrogenados no es conveniente introducir turbulencia en el medio. Por otra parte, el efecto de la hidrodinámica y el programa de potencial sobre la relación absoluta para cada parámetro kAgitado/kReposo demuestra que la agitación perjudica la degradación de las sustancias proteicas pero beneficia la remoción general de compuestos orgánicos (DQO). En todos los casos el tratamiento a potencial constante incrementó el valor de la pseudo constante de reacción.
Tabla 2. Relación entre las constantes de pseudo segundo orden de reacción para la remoción de nitrógeno proteico y DQO según las variantes del tratamiento oxidativo.
CONCLUSIONES
El sistema de degradación electroquímica presentado es un método de alta eficiencia para la remoción de sustancias orgánicas por combinar la oxidación directa e indirecta.
De las técnicas evaluadas, la oxidación a potencial constante resultó más eficiente que la llevada a cabo a potencial variable. Los potenciales de remoción reportados corroboran este hecho.
El efecto de la agitación fue beneficioso para la oxidación electroquímica en general. La turbulencia en el reactor propició una remoción adicional de la DQO en comparación con el sistema en reposo. Por el contrario, la degradación de sustancias orgánicas nitrogenadas disminuyó su intensidad con la agitación del reactor ya que una porción importante de compuestos de naturaleza proteica es removida por precipitación (fenómeno altamente dependiente del pH del medio que se ve afectado por la hidrodinámica del reactor).
De los análisis cinéticos del proceso, efectuados a partir de los datos experimentales se deduce que a potencial constante en sistemas agitados la remoción de la DQO experimenta una disminución en las restricciones para la degradación. La evidencia de lo anterior es el cambio en el orden de reacción aparente (nD.Q.O.) que varía de 2 a 1 en comparación con el tratamiento en reposo. A la oxidación cíclica en reposo y agitada siempre le correspondieron órdenes aparentes de reacción de aproximadamente 2; lo anteriormente expuesto demuestra que en la degradación general de compuestos orgánicos (DQO) predomina el mecanismo electroquímico sobre el químico, ya que la agitación promueve el transporte de las especies y un potencial constante intensifica las condiciones oxidativas en el ánodo.
Dependiendo de la finalidad del proceso, las condiciones de operación pueden ajustarse para disminuir de manera preferencial la DQO o para recuperar las albuminas precipitadas.
REFERENCIAS
1. Apha, L.M. (1994). Métodos estándar para el examen de agua y aguas de desecho. Undécima Edición, Editorial Interamericana. p. 302.
2. Comninellis, C. (1994). Electrocatalysis in the electrochemical conversion/combustion of organic pollutants for waste-water treatment. Electrochimica Acta. 39(11-12): 1857-1862.
3. Comninellis, C. & Pulgarin, C. (1993). Electrochemical oxidation of phenol for wastewater treatment using Sn anodes. Journal of Applied Electrochemistry. 23(2) : 108-112.
4. Crites, R. (2000). Tratamiento de aguas residuales en pequeñas poblaciones. Santa Fé de Bogotá: McGraw Hill. p. 776.
5. Daufin, G. (1974). Industrial Láctea. Barcelona - España: Quinta Edición.
6. Derek, P., Walsh, F. (1989). Industrial Electrochemistry. New York: Chapman and Hall. p. 653.
7. Grasselli, M. (1997). Que hacer con el suero del queso. Ciencia de Hoy. 8(43): 12-17.
8. Guzmán, P.J. (1988). Elaboración de quesos. Principios técnicos. Caracas: Editorial Espasande. p. 219.
9. Lugo, D. (1997). Manual de análisis químico-sanitario de efluentes residuales. Trabajo de ascenso para optar al mérito de profesor Asociado. No publicado. Facultad de Medicina. Universidad de Los Andes. Mérida-Venezuela.
10. Metcal & Eddy (1995). Ingeniería de agua Residuales. Vol. I. Tercera Edición. España: McGraw -Hill., p. 642.
11. Morales, C. (1992). El Suero de Quesería en la Industria. Alimentación, equipos y Tecnología. 11(6): 45-49.
12. Nemerow, N.L. (1977). Aguas residuales industriales: teorías aplicadas y tratamiento. Madrid: Editorial Blume. p. 572.
13. Romero, J. (1996). Acuiquímica. Santa Fé Bogotá: Editorial Presencia, p. 225.
14. Szpyrkowicz, L., Kelsall, G. H., Kaul, S. N., DeFaveri, M. (2001). Performance of electrochemical reactor for treatment of tannery wastewaters. Chemical Engineering Science . 56 (4): 1579-1586. [ Links ]