Serviços Personalizados
Journal
Artigo
Indicadores
-
 Citado por SciELO
Citado por SciELO -
 Acessos
Acessos
Links relacionados
-
 Similares em
SciELO
Similares em
SciELO
Compartilhar
Revista de la Facultad de Ingeniería Universidad Central de Venezuela
versão impressa ISSN 0798-4065
Rev. Fac. Ing. UCV vol.29 no.4 Caracas dez. 2014
Estudio comparativo de producción de nanopartículas de hierro por ablación láser en solución y gas inerte
Yosmery Vitta Brito, Vincent Piscitelli Spinielo, Mayrelis Flores Limpio, Alberto Fernández Cuervo, Jimmy Castillo
Escuela de Química, Facultad de Ciencias, Universidad Central de Venezuela. Paseo Los Ilustres Urb. Valle Abajo. Código Postal 1040. Caracas-Venezuela. e-mail: yosmery.vitta@ciens.ucv.ve
RESUMEN
En este trabajo se presenta una metodología para la producción de Nanopartículas de hierro, Nps Fe, por ablación láser en gas inerte (ALAGI): éstas se producen en un recipiente sellado y se transportan hacia el solvente utilizando una corriente de gas inerte (argón). Las propiedades de estas partículas fueron comparadas con otras del mismo material, obtenidas por ablación láser en solución (ALES). La producción de partículas se realizó por ablación consecutiva por períodos de 10 min, dejando enfriar por intervalos de 5 min entre cada irradiación, hasta alcanzar los 30 min; utilizando un haz láser Nd:YAG (30 mJ, 10 Hz, 9 ns,1064nm). En ambos sistemas, se obtienen Nps de Fe con un tamaño promedio (Tp) entre 8 -10 nm y una banda de resonancia de plasmon superficial (RPS) entre 300 y 380 nm. Se evaluó el efecto de la longitud de onda de irradiación del láser (532 nm y 1064 nm) sobre las características de las partículas; para la ALES, se observó a 532 nm, un aumento en el tamaño de partícula y una disminución en la absorbancia. Esto se atribuye a que en solución a mayor fluencia del láser, las partículas removidas son de mayor tamaño y los efectos de dispersión de la luz predominan sobre la absorción. Mientras que en ALAGI el uso de las dos longitudes de onda no influye sobre las Nps obtenidas, debido a que las partículas se arrastran de forma continua y su tamaño final dependerá del proceso de agregación dentro del solvente. La metodología desarrollada es de gran utilidad en el caso de las preparaciones de Nanopartículas en solventes orgánicos.
Palabras clave: Nanopartículas, Ablación láser, Gas inerte, Resonancia plasmónica, Solventes Orgánicos.
Comparative study of production of iron nanoparticles by laser ablation in solution and inert gas
ABSTRACT
In this work, we present a methodology of production for iron nanoparticles (iron Np) in organic solvents, by laser ablation. Using an inert gas stream the particles are blowing into solvent (LAiGS). The nanoparticles produced by this method were compared with nanoparticles produced by direct laser ablation in metal plate immersed in solvent (LAiS). The ablation procedure was performed in 10 minutes steps by triplicate with cooling periods of 5 minutes between ablations. Comparatively particles were obtained under continuous ablation iron plate at different ablation times, 10, 20 and 30 min. The same procedure was utilized in both cases, LAiS and LAiGS. Nps of size ranging between 8 -10 nm were obtained by both methods. The particles exhibited a Resonance Plasmon Surface (RPS) band between 300 and 380 nm, typical of Fe NP in acid medium. In LAiS, an increment of particle size and in consequence a lower absorbance was observed when an irradiation wavelength of 532 nm was used. In LAiGS no dependence was observed between particles properties and irradiation wavelength, due to plasma plume is less dense. LAiSG method will be used to prepare NP in organic flammable solvents for obtaining good NP dispersions. This fact is useful in experiments where the presence of water is undesirable.
Keywords: Nanoparticles, Laser ablation, Inert gas, Plasmonic Resonance, Organic Solvents.
Recibido: febrero 2014 Recibido en forma final revisado: mayo 2014
INTRODUCCIÓN
Las Nps de Fe, son de gran interés debido a su elevada reactividad, magnetismo, bajo costo y toxicidad (Nurmi et al. 2005; Hurber, 2005). Estas poseen importantes aplicaciones biomédicas: agente de contraste para imágenes de resonancia magnética y vehículo para el suministro de drogas farmacéuticas (Schweiger et al. 2011; Schleich et al. 2013; Yilmaz et al. 2013; Liong et al. 2008); también en remediación ambiental para la separación de contaminantes orgánicos: compuestos clorados, y contaminantes inorgánicos: arsénico y metales pesados, entre otros (Tang et al. 2013; Zhang et al. 2003, Kanel et al. 2005; Kanel et al. 2006; Cundy et al. 2008; Trantyek & Johnson, 2006; Ramos et al. 2009; Morgada et al. 2009; Comba et al. 2011). Los métodos preferidos de producción, son los denominados Bottom-up, auto-ensamblaje por vía química (Gao, 2004), estos poseen un control eficiente del tamaño y alto rendimiento en la síntesis, no obstante requieren elevado consumo de reactivos y tiempo, ocurre la formación de productos secundarios y son de fácil oxidación y aglomeración (Wilcoxon & Provencio, 1999; Mohanraj & Chen, 2008; Ju-Nam & Lead, 2008; Chen et al. 2010; Sun & Zeng, 2002). También se usan los métodos Top Down, miniaturización de materiales macizos (Niemeyer, 2001; Gao, 2004), son técnicas más limpias, pero poseen poco control del tamaño y son de costo elevado (Wang et al. 2012). Una técnica alternativa en la producción de Nanopartículas de hierro y de otros metales, es la Ablación Láser en solución, ALES (Amendola & Meneghetti, 2009). Esta es una técnica verde que se rige por los parámetros del láser y las propiedades del entorno, es altamente versátil: independiente del sustrato y del medio: gas y/o líquido, ligados, entre otros, posee control sobre el tamaño de la partícula, es rápida y de fácil empleo. El proceso consiste en la irradiación de un láser pulsado a alta energía sobre el sustrato metálico, que absorbe la energía del láser, produce la vaporización del metal y posteriormente la formación de un plasma. La formación de Nanopartículas empieza con su nucleación durante el enfriamiento del plasma, a temperaturas inferiores al punto de fusión del metal, seguido por el crecimiento del núcleo y coalescencia. La ALES permite obtener disoluciones coloidales de Nanopartículas de hierro estables, con una distribución de tamaño angosta y de tamaño promedio por debajo de los 10 nm (Liu et al. 2008; Vitta et al. 2011; Franzel et al. 2012) lo que las hace más atractivas en sus aplicaciones. En algunos casos es conveniente obtener dichas partículas por ablación en una cámara sellada, bien sea haciendo pasar a) una corriente de gas inerte y b) una corriente de gas reactivo (aire u oxígeno); esto según la composición final de las partículas a obtener (Ullmann et al. 2002; Zeng et al. 2005). Recientemente se ha ensayado la recolección posterior de partículas de hierro en un medio líquido que permite estabilizarlas, éstas se obtienen previamente por evaporación del material en fase gaseosa por láser pulsado (Chen et al. 2013). Los mecanismos propuestos de ablación láser para la obtención de nanopartículas están bien documentados, no obstante, hay poca información respecto a los efectos que pueden tener la ablación de un mismo sustrato metálico en diferentes entornos: gas inerte y solución, sobre las propiedades ópticas, magnéticas y de tamaño de las partículas. En este trabajo se plantea realizar la obtención de Nanopartículas de hierro por ablación láser en una cámara sellada con atmósfera de gas inerte y su posterior re-colección en solución; de forma comparativa se realizará la ablación en solución, y así poder evaluar los efectos del método ablativo sobre las partículas.
MATERIALES Y MÉTODOS
Las Nps Fe fueron obtenidas por dos métodos de Ablación Láser pulsada: 1) por arrastre de gas inerte: ALAGI y 2) en solución: ALES. En ALAGI la ablación se realizó dentro de una cámara sellada con atmosfera de gas Argón (flujo = 50 ml/ min), la entrada y salida del gas se realiza por conductos de vidrio unidos a ambos lados de la cámara, el de la salida está colocado dentro un recipiente con solvente, en el cual se soplan las partículas producidas. En la ALES, la ablación se realiza directamente sobre la placa de hierro inmersa en solución. En ambos casos, una placa de hierro puro (1,0 x 0,5 cm) se irradió por triplicado y de forma consecutiva, con un haz de láser Nd:YAG (30 mJ, 10 Hz, 9 ns,1064nm), por intervalos de 10 minutos hasta un tiempo total de 30 minutos, dejando enfriar la placa por un lapso de 5 minutos entre cada intervalo. Se evaluó el efecto del flujo del gas y de la longitud de onda del láser sobre las propiedades ópticas y de tamaño de las partículas. La distribución de tamaño de las partículas se midió con un equipo diseñado en el laboratorio basado en la técnica de dispersión dinámica de la luz. Mientras que las propiedades ópticas fueron seguidas por espectroscopia UV Visible.
RESULTADOS Y DISCUSIÓN
PRODUCCIÓN DE NANO-PARTÍCULAS POR ABLACIÓN LÁSER EN SOLUCIÓN Y EN GAS INERTE
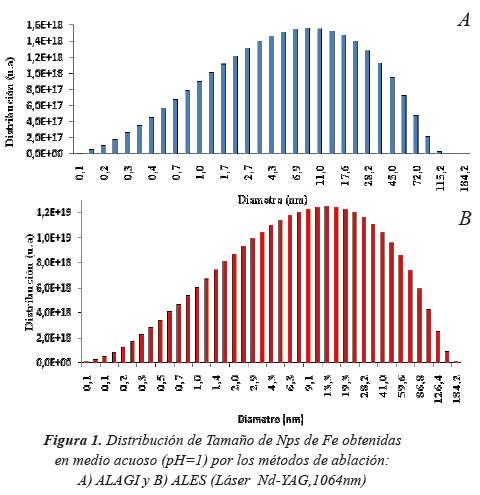
En la Figura 1 se presenta la distribución del tamaño de partículas obtenidas por los métodos de ablación a) ALAGI y b) ALES. Se observa que la distribución del tamaño de partículas para la ablación en solución es relativamente más ancha (0,1-184,2 nm) con respecto a ALAGI (0,1-115,2 nm), el diámetro promedio de partículas fue de 10,94nm y de 13,26 nm en ALAGI y ALES, respectivamente. Por otro lado, la producción de partículas en ALES es mayor en un orden de magnitud que en ALAGI. En ambos métodos, se produce un plasma a alta temperatura y presión que se confina sobre el sustrato irradiado, alrededor del plasma se forma una pluma expandida que consiste de átomos ionizados, átomos metálicos y clústeres (Gouriet et al. 2009; Liu et al. 2008). En presencia de pulsos de láser largos (nano-segundos) estas especies pueden absorber parte de la energía incidente del láser, lo cual incrementa la temperatura del plasma y favorece la atomización del material contenida en la pluma (Amendola & Meneghetti, 2009). Por otro lado, el proceso de ablación puede ser menos efectivo debido a que menor energía del láser incide sobre la muestra por efectos del apantallamiento óptico de la pluma del plasma. Este doble efecto compite en la eficiencia de la ablación. El medio sobre el cual se produce la ablación del metal influye directamente en los procesos de interacción del láser con la pluma del plasma y en consecuencia en la formación de las Nanopartículas.
Cuando la ablación del metal se produce en atmósfera inerte, los efectos de amortiguación del medio son menos importantes que en líquidos, por tanto la pluma del plasma es menos densa, las especies se encuentran distribuidas libremente a través de todo el plasma y existe baja probabilidad de colisiones entre sí, en consecuencia disminuye la coalescencia entre las partículas y el proceso de nucleación es más lento, luego el crecimiento de las Nanopartículas se produce en el líquido por agregación entre ellas. El mecanismo de formación de partículas en la fase gas y las pérdidas por transporte hacia al líquido, hacen que el proceso de recolección y agregación de las partículas en el líquido sea poco eficiente y la cantidad de partículas sea baja (Figura 1 A). En la ALES, la extinción del plasma es ultra-rápida, un orden de magnitud mayor que en gases y en el vacío (Liu et al. 2008), lo que favorece la ablación en una región mayor al área irradiada, debido a los efectos de conducción de calor por el solvente, incrementando así la cantidad de partículas en el medio (Figura 1 B).
EFECTOS DEL MÉTODO DE ABLACIÓN
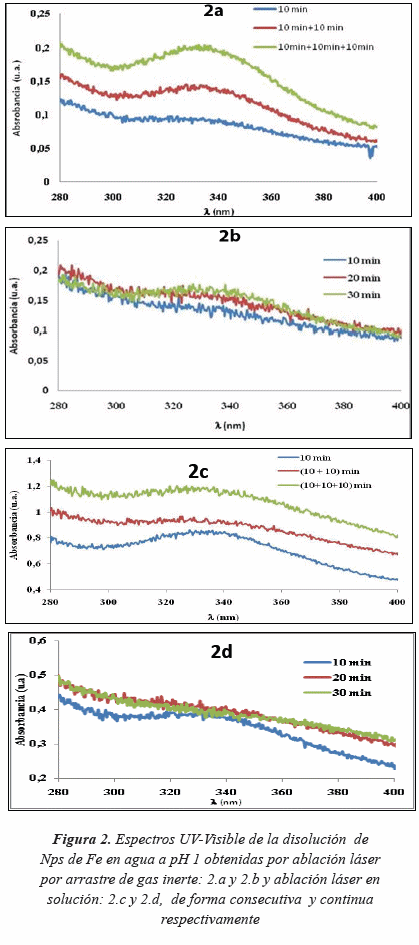
En la Figura 2, se presenta los espectros UV-Visible de las Nps de Fe en medio acuoso a pH=1, obtenidas por ALAGI (Figuras 2.a y 2.b) y por ALES (Figuras 2.c y 2.d), utilizando los métodos de ablación consecutiva y ablación continua, respectivamente. Se observa un máximo de absorción entre 300 y 360 nm, que se atribuye a la banda de resonancia de Plasmón superficial (RPS) típica de Nps de hierro en medio ácido (Vitta et al. 2011). En ALES se observa que hay un incremento en la intensidad del máximo de absorción a 330nm, cuando las partículas se obtienen con ablación consecutiva, mientras que en ALAGI tanto en ablación continua como en ablación consecutiva la intensidad permanece constante. Una análisis estadístico de prueba t pareada, para el valor de absorbancia al máximo de 330 nm, aporta como resultado que existen diferencias estadísticamente significativas entre la ablación consecutiva y la ablación continua para la ALES (texp=5,73 > t crítico(2,0.05) =4,30), mientras que para ALAGI la forma de ablación no influye sobre el valor de la absorbancia (texp=0,0833 < t crítico(2,0.05) =4,30). El mismo análisis estadístico se realizó para comparar ALES y ALAGI utilizando el método de ablación consecutiva encontrando texp=10,43 > t crítico (2,0.05) =4,30 , con lo cual se evidencia que la absorbancia para ALES difiere de la obtenida en ALAGI, lo cual se exhibe a priori en los espectros presentados.
En el método de ablación consecutiva, el sistema se deja reposar después de haber transcurrido los 10 min, cambiando así el gradiente de concentración de las especies producidas, de forma tal que disminuye el efecto de apantallamiento óptico sobre el láser.
Por lo tanto, en la ablación posterior el láser interacciona de forma efectiva con las partículas producidas y con el sustrato, en consecuencia la concentración de las partículas aumenta y esto ocurre de forma progresiva cuantas veces se repita el proceso de re-ablación. Este efecto se evidencia experimentalmente en ALES, puesto que durante la ablación de forma continua, se observa que se producen ondas de choque sobre el medio líquido, que hacen que el solvente salte hacia la superficie del lente de enfoque y se acumule sobre él, lo cual impide la transmisión efectiva del haz láser y su interacción con la muestra. Es necesario detener el experimento, limpiar el lente y comenzar de nuevo la ablación (Kebede et al. 2011). En ALAGI, las partículas producidas por la ablación se arrastran de forma continua por la corriente del gas y en consecuencia el plasma interactúa con el sustrato, bajo las mismas condiciones superficiales, de allí que no hay un efecto importante en el cambio de absorbancia utilizando ablación continua o ablación consecutiva.
EFECTO DE LA LONGITUD DE ONDA
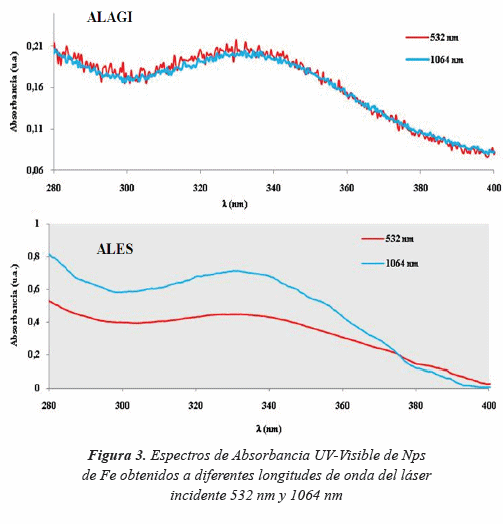
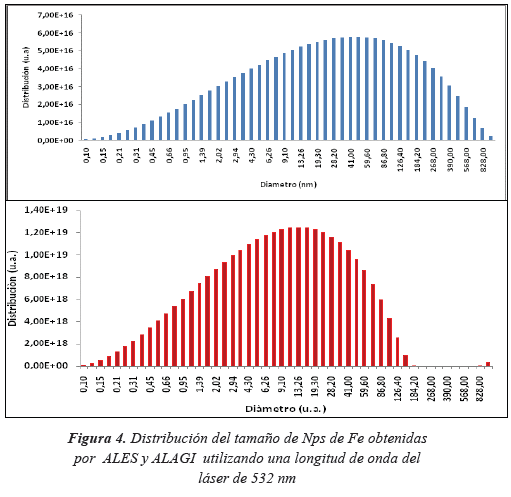
En las Figuras 3 y 4, se presenta el efecto de la longitud de onda sobre la intensidad del máximo SPR y el diámetro promedio de las Nanopartículas de Fe obtenidas, respectivamente. EN ALES, se observa que hay una disminución en la eficiencia de la ablación cuando se utiliza la longitud de onda del láser incidente más baja a 532 nm. Mientras que en ALAGI, no hay un efecto notable sobre las propiedades de las partículas. Para la ALES, se observa una incremento en el diámetro de la partícula cuando se utiliza la longitud de onda corta (532 nm), esto se atribuye a que a mayor fluencia del láser los fragmentos del material eyectado del sustrato son más grandes, excepto cuando la longitud de onda del láser puede ser re-absorbida por las Nanopartículas, produciendo fotofragmentación (Mafune et al. 2002). En este estudio, las Nps de Fe no pueden absorber la energía del haz láser incidente (532 nm) dado su resonancia plasmon a 330 nm, por lo que no pueden ser foto-calentadas y fragmentadas en partículas más pequeñas, con lo cual su tamaño promedio (42,5 nm) es alto. Por otro lado, una mayor intensidad en la absorción del máximo RPS (0,712 u.a.) se observa cuando se utiliza λ= 1064 nm (Figura 2). Esto se explica por la descripción de la resonancia plasmon en nano-partículas esféricas, utilizándola aproximación de dipolo y la teoría cuasi estática propuesta por Mie, según la cual la sección transversal de absorción de una Np esférica es directamente proporcional al volumen de la partícula, mientras que la dispersión dependen del cuadrado del volumen (Boren et al. 1983). Por lo tanto en partículas pequeñas la absorción predomina sobre el plasmón superficial mientras que para partículas grandes predomina la dispersión (Brongersma & Kik, 2007). En ALAGI, se observa que la intensidad del máximo SPR no se ve afectado por el uso de dos longitudes de onda diferentes del láser: 532 nm y 1064 nm. Así también el tamaño promedio de las partículas, de 8,7nm y 10,94 nm, fue similar para ambas longitudes de onda. No obstante, en la Figura 4, se observa un ligero incremento en la producción de Nps de Fe, λ=532 nm, esto se debe a que a mayor energía hay mayor cantidad de átomos metálicos evaporados desde el sustrato metálico, por lo tanto la pluma del plasma se hace más densa, lo que determinara la cantidad final de partículas.
CONCLUSIÓN
En este trabajo se obtienen disoluciones coloidales estables de Nps de Fe en medio acuoso con tamaño promedio inferior a los 15 nm y banda plasmón entre 350 y 380 nm, para los métodos de ablación utilizados: ALES y ALAGI. La ablación en gas inerte resulta una metodología alternativa para la producción de partículas de hierro en solventes orgánicos, dado que se evitan los efectos de pirólisis por alta reactividad del solvente a alta temperatura, los cuales afectan la bio-compatibilidad, estabilidad y disponibilidad de sitios de adsorción superficial en las Nanopartículas, bajos riesgos de inflamabilidad del solvente por efecto de la energía del haz láser, partículas de mayor pureza, mayor versatilidad en el sustrato y el solvente, mejor control sobre las propiedades del tamaño, entre otros. La principal limitación es la baja producción de las partículas debido a los efectos de interacción en el plasma y las pérdidas por transporte hacia el líquido. Un incremento controlado en la energía del haz incidente pudiese contribuir a mejorar la eficiencia de síntesis de las partículas de hierro por ALAGI, sin comprometer su estabilidad y tamaño. El método de ALES es preferible para la obtención de las partículas en solventes acuosos dado su alto rendimiento y control adecuado de sus propiedades ópticas y de tamaño.
AGRADECIMIENTOS
Los autores agradecen al Consejo de Desarrollo Científico y Humanístico de la Universidad Central de Venezuela, Proyecto: PG-03-8805-2013/1 y al Fondo Nacional de Ciencia, Tecnología e Innovación, adscrito al Ministerio del Poder Popular para la Ciencia, Tecnología e Innovación.
REFERENCIAS
1. Amendola, V. & Meneghetti, M. (2009). Laser Ablation Synthesis in Solution and Size Manipulation of Noble Metal Nanoparticles. Phys. Chem. Chem. Phys, 11; pp. 3805-3821. [ Links ]
2. Bohren, C. F. & Huffman, D. R. (1983). Absorption and Scattering of Light by Small Particles. John Wiley& Sons; New York.
3. Brogersma, M. & Kik, P. (2007). Surface Plasmon Nanophotonics.Chapter Two.Near-Field and Far-Field Properties of Nanoparticle Arrays.pp. 11-19.
4. Springer. Chen, Z., Zhan, P., Dong, W. (2010). Bottom-up fabrication approaches to novel plasmonic materials. Chinese Sci Bull. 55(24), pp. 2600–2607.
5. Chen, S., Zhang, Y., Han, W., Wellburn, D., Liu, C. (2013). Synthesis and magnetic properties of Fe2O3 nanocomposite using pulsed laser gas phase evaporationliquid phase collecting method. Applied Surface Science,283,pp.422-429.
6. Cundy, A., Hopkinson, L., Whitby, R. (2008). Use of iron-based technologies in contaminated land and groundwater remediation. Environ. Sci. Technol. 400; pp. 42-51.
7. Comba, S., Di Molfetta, A., Sethi, R. (2011). A Comparison between Field Applications of Nano, Micro, and Millimetric Zero-Valent Iron for the Remediation of Contaminated Aquifers . Water air and soil pollution - water air soil pollut ,215,(1); pp. 595-607.
8. Franzel, L., Bertino, M. F., ,Huba, Z. J., Carpenter, E. E. (2012). Synthesis of magnetic nanoparticles by pulsed laser ablation.Applied Surface Science. 261, pp. 332– 336.
9. Gao, G. (2004). Nanostructures and nanomaterials. Synthesis, Properties and Applications. London: imperial College Press.
10. Gouriet, K., Zhigilei, L. V., Itina, T. E. (2009). Molecular dynamics study of nanoparticles evolution in a background gas under laser ablation conditions. Applied Surface Science. 255, pp. 5116-5119.
11. Huber, D. L. (2005). Synthesis, properties, and applications of iron nanoparticles.Small;1(5):482-501.
12. Ju-Nam, Y. & Lead, J. (2008). Manufacture Nanoparticles: An overview of their chemistry, interactions and potential environmental implications .Scien. Tot. Environm., 400, pp. 396-414.
13. Kanel, S., Grenche, J., Choi, H. (2005). Arsenic (III) Removal from groundwater using nanoscale zero valent iron as a colloidal reactive barrier material. Environ. Sci. Technol. 39 (5); pp. 1291-1298.
14. Kanel, S., Grenche, J., Choi, H. (2006) Arsenic (V) Removal from groundwater using nanoscale zero valent iron as a colloidal reactive barrier material. Environ. Sci. Technol. 40(6); pp.2045-2050.
15. Kebede, A., Gholap, A. V., Rai, A. K. (2011). Impact of Laser Energy on Synthesis of Iron Oxide Nanoparticles in Liquid Medium.World Journal of Nano Science and Engineering, 1, pp 89-92.
16. Liong, M., Lie, J., Kovochich, M., Xia, T., Ruehm, S. G., Nel, A. E., Tamanoi, F., Zink, J. I. (2008). Nano 2; 889; 500.
17. LIU, P., CAI, W., ZENG, H. (2008). Fabrication and Size- Dependent Optical Properties of FeO Nanoparticles Induced by Laser Ablation in a Liquid Medium.J. Phys. Chem. C, 112, pp. 3261-3266.
18. Mafuné, F., Kohno, J., Takeda, Y., Kondow, T. (2002). Growth of Gold Clusters into Nanoparticles in a Solution Following Laser-Induced Fragmentation.J. Phys. Chem. B, 106 (34), pp 8555–8561.
19. Mohanraj, V. & Chen, Y. (2008). Nanoparticles- A Review. Nanoscale Res. Lett, 3; pp: 397–415.
20. Morgada, M., Levy, I., Salomone, V., Farías, S., López, G., Litter, M. (2009). Arsenic (V)removal with nanoparticulatezerovalent iron.Catalysis Today, 143; pp. 261-268.
21. Niemeyer, C. (2001). Nanoparticles, proteins and nucleic acids: biotechnology melts material science. AngewChemInt Ed,40(22) ; pp 4128-58.
22. Nurmi, J. T., Tratnyek, P. G, Sarathy, V., Baer, D. R., Amonette, J. E., Pecher, K., Wang, C., Linehan, J. C., Matson, D. W., Penn, R. L., Driessen, M. D. (2005). Characterization and properties of metallic iron nanoparticles: spectroscopy, electrochemistry, and kinetics. Environ Sci Technol.Mar 1;39(5):1221-30.
23. Ramos, M., Yan, W., Li, X., Koel, B., Zhang, W. (2009). Simultaneous Oxidation and Reduction of Arsenic by Zero-Valent Iron Nanoparticles:Understanding the Signifance of the Core- Shell Structure. Phys. Chem. Letters.113; pp.14591-14594.
24. Sun, S. & Zeng, H. (2002). Communication Size-Controlled Synthesis of Magnetite Nanoparticle.J. Am. Chem. Soc. 124; 8204.
25. Schweiger, C., Pietzonka, C., Heverhagen, J., Kissel, T. (2011). Novel magnetic iron oxide nanoparticles coated with poly(ethylene imine)-g-poly(ethylene glycol) for potential biomedical application: Synthesis, stability, cytotoxicity and MRimaging.International Journal of Pharmaceutics, 408, (1–2), 15 pp.130-137.
26. Schleich, N., Sibret, P., Danhier, P., Ucakar, B., Laurent, S., Muller, R. N., Jerome, C., Gallez, B., Preat, V., Danhie, F. (2013). Dual anticancer drug/ super paramagnetic iron oxide-loaded PLGA-based nanoparticles for cancer therapy and magnetic resonance imagingInternational Journal of Pharmaceutics, 447, 1–2(15) pp. 94-101.
27. Tang, Y., Chu, L., Sun, N., Liu, R., Ge, G. (2013). Research progress in magnetic separation with iron oxide magnetic nanoparticles.Chinese Science Bulletin , 58(24):pp 2377- 2384.
28. Trantyek, P. & Johnson, R. (2006). Nanotechnologies for environmental cleanup Nanotoday, 2; pp. 44-48.
29. Ullmann, M., Friedlander, S. K., Schmidt-Ott, A. (2002). Nanoparticle formation by laser ablation.Journal of Nanoparticle Research 4, pp. 499–509.
30. Vitta, Y., Piscitelli, V., Fernandez, A., González, F., Castillo, J. α-Fe nanoparticles produced by laser ablation: Optical and magnetic properties. Chemical Physics Letters 512 (2011) 96–98.
31. Wilcoxon, J. & Provencio, P. (1999). Use of Surfactant Micelles to Control the Structural Phase of Nanosize Iron Clusters.J.Phys. Chem. B, 103 (45), pp 9809–9812.
32. Wang, Z., Li, X., Gao, M., Zeng, X. (2012). One Preparation of amorphous iron nanoparticles by laser ablation. Powder Technology. 215-216,PP.147-150.
33. Yilmaz, A., Rösch, S., Klingel, K., Kandolf, R., Helluy, X., Hiller, K., Jakob, P. (2013). Magnetic resonance imaging (MRI) of inflamed myocardium using iron oxide nanoparticles in patients with acute myocardial infarction Preliminary results.International Journal of Cardiology, 163, 2, pp.175-182.
34. Zeng, X., Wang, Z., Liu, Y. Ji, M. (2005). γ-Fe2O3 nanoparticles prepared by laser ablation of a tiny wire. Appl. Phys. A 80, 581–584.
35. Zhang, W. (2003). Nano scale iron particles for environmental remediation: an overview. J. Nanopart. Res. 5; pp.323-332.