Boletín de Malariología y Salud Ambiental
versión impresa ISSN 1690-4648
Bol Mal Salud Amb vol.53 no.1 Maracay ene. 2013
Farmacocinética de la ulamina administrada en perros como prueba aguda intravenosa e intramuscular
Laura Cristina Vásquez P.1*, José Vicente Scorza Dagert2, Herminia Bendezú2, Nelson Vicuña-Fernández1, Yaneira Petit3, Sabrina López3 & Elis Pirela1
1 Laboratorio de Farmacología. Escuela de Medicina Extensión Valera. Facultad de Medicina. Universidad de Los Andes. Valera-Venezuela CP 3101.
2 Instituto Experimental ¨José Witremundo Torrealba¨, Núcleo Universitario Rafael Rangel Universidad de Los Andes. Trujillo- Venezuela.
3 Laboratorio de Espectrometría Molecular. Facultad de Ciencias. Universidad de Los Andes. Mérida -Venezuela.
*Autor de correspondencia: lavasquez60@hotmail.com
RESUMEN
Se realizó una investigación con el objeto de describir la disposición farmacocinética del antimonial pentavalente genérico ulamina en 8 perros sanos, como prueba aguda intravenosa e intramuscular, después de administrar una dosis de 25 mg/kg. Las curvas obtenidas para ambas vías muestran un descenso de las concentraciones plasmáticas de 184,91± 86,06 μg/mL a 86,06±39,24 μg/mL y 164,61 ± 23,80 μg/mL a 100,94 ± 45,3 μg/mL, hasta la hora 4,0 para las vía IV e IM, respectivamente, que corresponden a la fase alfa de distribución. Seguidamente se aprecia un descenso lento, con antimonio detectable más allá de la hora 24 para ambas vías, denominada fase beta o de eliminación. La droga se absorbe rápidamente y mostró alta biodisponibilidad. La vida media (t1/2β) IV fue de 8,1 horas y t1/2 β IM fue 13,35 horas. El volumen de distribución (Vd) IV fue de 0,17 L/Kg e IM fue de 0,23 L/Kg. No se encontraron diferencias significativas al comparar AUC y t1/2β, después de administrar ulamina IV e IM, proponiéndose esta última como ruta de administración por resultar más práctica y segura. La ulamina constituiría una opción terapéutica para el tratamiento de la leishmaniasis humana y canina, por lo que se sugiere la aplicación de ensayos con dosis múltiples para evaluar la fase de eliminación y determinar si hay acumulación de antimonio, lo cual justificaría una disminución de la dosis.
Palabras clave: Farmacocinética, ulamina, perros, prueba aguda.
Pharmacokinetic disposition of ulamina in dogs administered as intravenous and intramuscular acute test
SUMMARY
A study was carried out to describe the pharmacokinetic disposition of pentavalent antimony generic ulamina in 8 healthy dogs in acute intravenous and intramuscular test after a dose of 25mg/Kg. The curves obtained for both routes show a decrease in plasma concentrations of 184.91 ± 86.06 μ g / mL to 86.06 ± 39.24 μ g / mL and 164.61 ± 23.80 μ g / mL to 100.94 ± 45.3, μ g / mL to 4.0 hours for the IM and IV, respectively, corresponding to the alpha phase distribution. There was a decrease slowly, with antimony detectable beyond 24.0 hours for both routes, called beta or disposal. The drug is rapidly absorbed and showed high bioavailability. The half life (t1/2β) IV was 8.1 hours and t1/2β IM was 13.35 hours. The volume of distribution (Vd) IV was 0.17 L /Kg and MI was 0.23 L /Kg. No significant differences were found when comparing AUC, and t1/2β, after IV and IM administration ulamina, proposing the latter as a more practical and safe administration route. The ulamina may be a therapeutic option for the treatment of human and canine leishmaniasis, as it is suggested by the application of multiple dose trials to evaluate the phase of removal and to determine if there is an accumulation of antimony, which would warrant a dose reduction.
Key words: Pharmacokinetics, ulamina, dogs, acute test.
Recibido el 17/02/2013
Aceptado el 16/05/2013INTRODUCCIÓN
La leishmaniasis visceral (LV) es una enfermedad zoonótica causada por el protozoario Leishmania (L.) infantum, el parásito es trasmitido a los humanos por la picadura de insectos dípteros del género Lutzomyia, tratándose de una zoonosis su ciclo epidemiológico involucra, entre otros, mamíferos de la Familia Canidae (Cerdocyon thous, Canis familiaris, Spheotos venaticus, y Lycalopex vetulus) como sus principales reservorios (Reyes & Arrivillaga, 2009; Vásquez et al., 2010). Por lo tanto,una vía para prevenir la transmisión en humanos, debe ser erradicar la enfermedad canina. Los antimoniales pentavalentes continúan siendo las drogas de primera escogencia para el tratamiento de la leishmaniasis humana y canina. Los preparados más empleados son el estibogluconato de sodio (Pentostam®) y el antimoniato de N-metilglucamina (Glucantime®), a pesar de sus conocidas limitaciones en el ámbito terapéutico: necesidad de administración diaria parenteral, falta de respuesta o respuesta con reacciones secundarias y efectos adversos, así como resistencia aparente acompañada de recaídas. Algunos autores sugieren que parte de la falla en la terapéutica con estos compuestos podría residir en la carencia de correlación entre los protocolos de administración y el comportamiento farmacocinético del antimonio (Nieto et al., 2003; Schettini et al., 2005; Vásquez et al., 2006; Gradoni et al., 2008; Arrivillaga et al., 2008; Frezard et al., 2009; Gómez et al., 2011).
Se realizó un ensayo experimental con un preparado de antimonio pentavalente denominado ulamina después de administrar una dosis única de 25 mg/ kg por vía intravenosa e intramuscular a perros sanos, con el objeto de conocer sus parámetros farmacocinéticos. El compuesto se ha sintetizado en el Laboratorio de Quimioterapia y Control del Instituto Experimental "José Witremundo Torrealba" de la Universidad de Los Andes (Vásquez et al., 2005; Scorza Dagert et al., 2006). Al igual que en otros países, su manufactura como preparación genérica, responde a la necesidad de enfrentar con soluciones la crisis económica, al reducir los costos globales del tratamiento (Sundar et al., 1998; Veeken et al., 2000; Vásquez et al., 2006). La definición del perfil farmacocinetico del compuesto en el perro, podría sugerir un modelo de protocolo terapéutico para la dosis, su intervalo de administración, duración de la terapia en esta especie y brindaría información valiosa para su aplicabilidad en humanos.
MATERIALES Y MÉTODOS
Animales
Se emplearon 8 perros (Canis familiaris) mestizos sanos de ambos sexos, con edad y peso promedio de 2 años y 30 kilogramos respectivamente, procedentes de un criadero canino de la localidad.Los criterios de exclusión fueron anemia, tiempo de protrombina anormal y deterioro de la función renal o hepática. Los animales seleccionados en función de su maniobrabilidad y docilidad, fueron evaluados clínica y ponderalmente por un médico veterinario, posteriormente fueron desparasitados y suplementados nutricionalmente, con alimento concentrado enriquecido, durante un mes previo al ensayo. Tres días previos al inicio del ensayo, se procedió a practicar pruebas hematológicas y de química sanguínea con el fin de determinar los valores hematimétricos habituales, funcionalismo hepático, renal y glicemia. A los animales se les suministró dieta convencional a base de alimento concentrado y agua ad libitum mientras se realizaron las pruebas.
Material farmacológico y dosificación
Ulamina (pentacloruro de antimonio + N - metil - glucamina), sintetizada en el Laboratorio de Quimioterapia y Control del Instituto Experimental "José Witremundo Torrealba" de la Universidad de Los Andes, con una concentración aproximada de 0,3 g/mL Sb V (Scorza Dagert et al., 2006), a una dosis de antimonio de 25 mg/Kg/día, a cuatro animales se les administró la dosis por vía intravenosa y a cuatro animales se les administró por vía intramuscular.
Diseño experimental
A cuatro animales experimentales se les cateterizaron ambas venas safenas, a través de una se administró el compuesto y de la otra se obtuvo el muestreo, a los cuatro animales restantes se les administró el fármaco mediante inyección intramuscular profunda. Se colectaron muestras de sangre completa en cada animal, previa a la administración del antimonial. Inmediatamente después, se procedió a la administración de la dosis correspondiente de fármaco. Se colectaron muestras de sangre a las 0,25 -0,75 - 1,0 - 2,0 - 4,0 - 8,0 - 12,0 y 24,0 horas, de de 2 mL. Las muestras se mantuvieron congeladas (4ºC) hasta el momento de su procesamiento, en cada una de ellas se determinó el antimonio orgánico total y sus especies.
Métodos analíticos
La concentración de antimonio total y sus especies (SbIII y SbV) fue determinada utilizando un espectofotómetro de Absorción Atómica Varian- Techtron modelo AA-1475, acoplado con generación de hidruros. Los límites de detección (tomando 3 veces la desviación estándar relativa del blanco) obtenidos, fueron de 1,02 y 0,58 μg-L para antimonio III (SbIII) y antimonio V (SbV) respectivamente, el antimonio total fue calculado mediante la suma de las concentraciones de ambas especies (Petit de Peña et al., 2001). Análisis farmacocinético Para cada animal se elaboraron curvas de concentración plasmática versus tiempo, analizándose por un modelo no compartimental basado en la teoría de momento estadístico (Wagner, 1993) utilizando el programa computarizado PK Solutions (Farrier, 2003). Los parámetros farmacocinéticos calculados para la administración intravenosa fueron: el área bajo la curva de concentración versus tiempo (AUC0-t), calculada usando la regla trapezoidal en el intervalo 0-24h, el tiempo medio de residencia (TMR=AUMC/AUC), la vida media (t1/2 β) determinada como ln2/β, β fue calculada a partir de la pendiente de la línea de regresión, constante de eliminación (Kel), el volumen aparente de distribución (Vdárea= Dosis / AUC xβ), el volumen de distribución en el estado de equilibrio (Vdss= TMR/ CL) y el clearance o depuración (CL= Dosis/AUC). Los valores calculados a partir de la vía intramuscular fueron: AUC, t1/2 β y la biodisponibilidad intramuscular (F (%)= (AUCi.m/AUCi.v) x 100). La máxima concentración observada (Cmax) y el tiempo (Tmax) fueron obtenidos directamente desde las curvas individuales. Análisis estadístico Para el análisis se calcularon los datos estadísticos descriptivos, medias y desviación estándar. Las diferencias entre AUC, TMR y t1/2βentre las dos vías de administración fue analizada estadísticamente empleando el Test de Wilcoxon (se consideró significativo todo valor de P< 0,05). Consideraciones éticas El Comité de Bioética del Instituto Experimental "José Witremundo Torrealba" de la Universidad de Los Andes avaló los procedimientos desarrollados en la investigación.
RESULTADOS
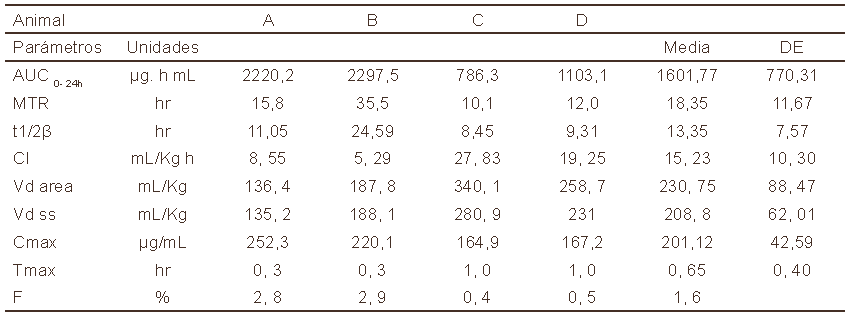
Las curvas de concentración plasmática medias de antimonio total en función del tiempo para ambas vías de administración se muestran en la Fig. 1. Los parámetros farmacocinéticos promedio para la ulamina obtenidos desde el análisis de la curva para cada animal se muestra en las Tablas I y IITabla_II. Después de la administración intravenosa de la ulamina se observa un descenso del antimonio total en dos fases, una fase de eliminación rápida con una caída de la concentración plasmática de 184,91± 86,06 a 86,06±39,24 hasta la hora 4,0, indicando rápida distribución de la droga. En la segunda fase de eliminación más lenta, las concentraciones plasmáticas descendieron más paulatinamente y la droga fue detectable más allá de las 24,0 hs. La vida media (t1/2 β) fue de 8,1 hs. La ulamina mostró un volumen de distribución de (Vd) de 178,9 mL/ kg (0,17 L/Kg), con un volumen de distribución en estado de equilibrio de (Vdss) de 197,3 mL/kg (0,19 L/Kg) y una depuración de 20,47 mL/Kg/h. Después de la administración intramuscular una Cmax de 201,12 μg/mL se alcanzó en 0,65 horas, posteriormente se aprecia una caída en dos fases, un descenso marcado hasta la hora 4,0 de 164,61 ± 23,80 a 100,94 ± 45,3 y un segundo descenso más lento con droga detectable más allá de las 24 horas. La vida media (t1/2 β) fue 13,35 h. La ulamina mostró un volumen de distribución (Vd) de 230,75 mL/kg (0,23 L/Kg), con un volumen de distribución en estado de equilibrio de (Vdss) de 208,8 mL/kg (0,20 L/Kg) y una depuración de 15,23 mL/Kg/h.
Fig. 1. Concentraciones plasmáticas promedio después de la administración de 25 mg/kg de ulamina por vía intravenosa e intramuscular en perros (n=4).
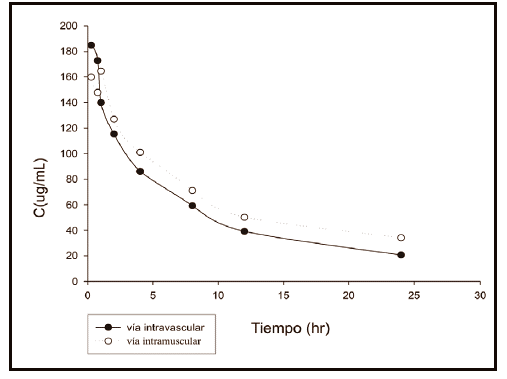
Tabla I. Parámetros farmacocinéticos de la ulamina después de la administración intravenosa (25mg/ Kg) en perros.
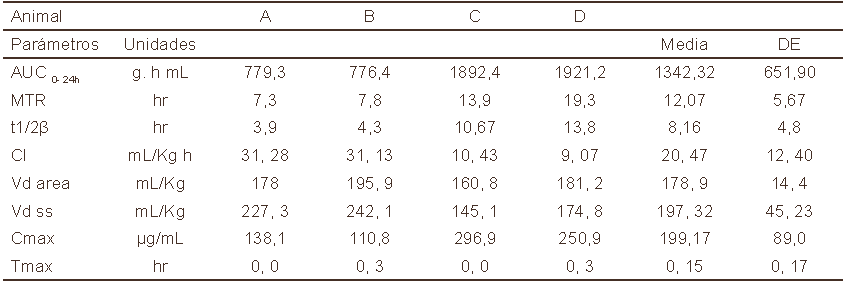
Tabla II. Parámetros farmacocinéticos de la ulamina después de la administración intramuscular (25mg/ Kg) en perros.
No se encontraron diferencias significativas al comparar AUC, y t1/2 β, después de administrar ulamina por vía intravenosa o intramuscular.
DISCUSIÓN
La farmacocinética de los compuestos antimoniales empleados usualmente en medicina humana y veterinaria es compleja e impredecible, modificando la respuesta individual (Vásquez et al., 2008). Adicionalmente, los datos cinéticos han mostrado diferencias relevantes en el comportamiento cinético de la droga en perros en comparación con los humanos, de allí que el análisis de los datos experimentales podría ayudar a clarificar el comportamiento de la ulamina cuando se administre para el tratamiento de la leishmaniasis canina o humana. La disposición cinética de las curvas de concentración plasmática versus tiempo obtenidas después de la administración del compuesto genérico ulamina por vía intravenosa e intramuscular, se caracteriza por dos fases claramente definidas. La fase inicial muestra un descenso rápido de las concentraciones plasmáticas de antimonio que corresponde a la fase de distribución (fase alfa), la cual es seguida por una segunda fase de eliminación de la droga que describe el periodo de eliminación (fase beta), así después de la administración intravenosa (IV) de la ulamina la fase alfa muestra una caída de la concentración plasmática de 184,91± 86,06 g/mL a 86,06±39,24 μg/mL hasta la hora 4,0 y después de la administración por vía IM de 164,61 ± 23,80 μg/mL a 100,94 ± 45,3 μg/mL, lo cual confirma una distribución rápida de la droga. Posteriormente, aparece la fase beta y muestra el descenso mas lento de la ulamina detectable más allá de la hora 24,0 para ambas vías. Lo anterior es comparable con el patrón mostrado por el preparado comercial (Glucantime®) pero este último a concentraciones plasmáticas mucho mas bajas, atribuible muy probablemente a la vía de administración empleada en el ensayo (vía subcutánea) (Valladares et al., 2001; Vásquez et al., 2008).
La droga se absorbe rápidamente, a la dosis empleada en este ensayo (25mg/Kg), alcanzando un Tmax de 0,6 horas y una biodisponibilidad intramuscular muy amplia, con lo que podría sugerirse esquemas de administración por esta vía. Valladares et al. (1996), encontraron que la biodisponibilidad después de la administración intramuscular y subcutánea fue 91,7 (±7,1) y 92,2 (±7,1)%, respectivamente, mientras que Tassi et al. (1994) encontraron que la biodisponibilidad aparente del antimonio fue mayor de 100% para la vía intramuscular y del 100% para la vía subcutánea; confirmándose diferencias relevantes en comparación con los humanos, y plantean la vía subcutánea como la más conveniente, dado que la concentración sérica obtenida por vía intramuscular o subcutánea es similar, pero hay mayor persistencia de antimonio en sangre empleando esta última.
La vida media (t1/2β) de la ulamina administrada por vía IV fue de 8,1 horas y la vida media (t1/2β) por vía IM fue 13,35 horas; muy similar a la t1/2β reportada para el Glucantime® de 10,02 horas cuando se empleó por vía subcutánea (Vásquez et al., 2008). Es conocido que el metal se excreta rápidamente del cuerpo, con una t1/2β corta que confirma una depuración rápida (Nieto et al., 2003). Tassi et al., (1994) también describieron el comportamiento cinético del antimonio después de emplear las mismas dosis y las mismas vías de administración, reportando una diferencia para la vida media en las tres vías: 20,5; 42,1 y 121,6 minutos para la vía intravenosa, intramuscular y subcutánea respectivamente, obviamente menores que las reportada para el Glucatime® y las encontradas para la ulamina. La ulamina mostró un volumen de distribución de (Vd) IV de 178,9 mL/kg (0,17 L/ Kg), un (Vd) IM de 230,75 mL/kg (0,23 L/Kg), el Vd de la ulamina en el perro tanto vía IV e IM es casi equivalente (0,178 y 0,230 L/Kg), pero mucho menor que el reportado para el Glucantime Vd ß 5.54 por vía subcutánea (Vásquez et al., 2006). Por el contrario en humanos el volumen de distribución de la ulamina mostró una diferencia grande con otros antimoniales Vd 6,66 L/Kg (Vásquez et al., 2006), lo que podría indicar penetración y fijación tisular.
En vista de que no se encontraron diferencias significativas al comparar AUC y t1/2β, después de administrar ulamina por vía intravenosa o intramuscular y la biodisponibilidad alcanzada, se podría sugerir esta última como ruta de administración por resultar más práctica y segura. Recientemente se ha despertado el interés por confirmar la eficacia de los antimoniales genéricos, estos preparados son un tratamiento alternativo en países con alta morbi-mortalidad por leishmaniasis, la ulamina es un antimonial pentavalente experimental, cuya síntesis química local permitirá ofrecer a los pacientes con leishmaniasis humana y canina, una opción más económica que los preparados convencionales (Vásquez et al., 2006) aunque, se sugiere la realización de ensayos con aplicación de dosis múltiples para evaluar la fase de eliminación y determinar si hay acumulación de antimonio, lo cual justificaría una disminución de la dosis. Conflictos de intereses Los Autores manifestamos que no ha habido conflictos de intereses en la realización de este trabajo.
AGRADECIMIENTOS
Al Dr. Romer Rubio Villasmil+ por el apoyo logístico prestado para la realización del presente trabajo en las instalaciones de la Escuela de Medicina Extensión Valera Universidad de Los Andes.
REFERENCIAS
1.Arrivillaga J., Rodriguez J. & Oviedo M. (2008). Evaluación preliminar en un modelo animal de la terapia con larvas de Lucilia sericata para el tratamiento de la leishmaniasis cutánea. Biomédica. 28: 305-10. [ Links ]
2.Farrier D. (2003). PKSolutions 2.0. Noncompartmental pharmacokinetics data analysis. Ashland (USA), Summit Research Services. [ Links ]
3. Frezard F., Demicheli C. & Ribeiro R. (2009). Pentavalent antimonials: New perspective for old drugs. Molecules. 14: 2317-2336. [ Links ]
4.Gómez M., Chávez N. & Delgado G. (2011). Evaluación "in vitro" e "in vivo" del efecto del aceite esencial de Elettaria cardamomun sobre parásitos de Leishmania (Viannia) panamensis. Biomédica. 31(Supl. 3): 23-205. [ Links ]
5.Gradoni L., Soteriadou K., Louzir H., Ozensoy S., Jaffe C., Dedet P. et al. (2008). Drugs regimens for visceral leishmaniasis in Mediterranean countries. Trop. Med. Int. Health. 13: 1272-1276. [ Links ]
6.Nieto J., Alvar J., Mullen A., Carter K., Rodriguez C., San Andres M., et al. (2003). Pharmacokinetics, toxicities and efficacies of sodium stibogluconate formulations after intravenous administration in animal. Antimicrob. Agents Chemother. 47: 2781- 2787. [ Links ]
7.Petit de Peña Y., Vielma O., Burguera J., Burguera M., Rondón C. & Carrero P. (2001). On line determination of antimony three (III) and antimony five (V) in liver tissue and whole blood by flow - injection hydride generation - atomic absortion spectrometry. Talanta. 55: 743-754. [ Links ]
8.Reyes A. & Arrivillaga J. (2009). Fauna Mammalia asociada a los focos de leishmaniasis neotropical. Situación en Venezuela. Bol. Mal. Salud Amb. 49: 135-152. [ Links ]
9.Schettini D., Costa A., Sousa L., Demicheli C., Rocha O., Melo M., et al. (2005). Pharmacokinetic and parasitological evaluation of the bone marrow of dogs with visceral leishmaniasis submitted to multiple dose treatment with liposomeencapsulated meglumina antimoniate. Braz. J. Med. Biol. Res. 38(12): 1879-1883. [ Links ]
10.Scorza Dagert J., Morales C., Petit de Peña Y., Vásquez L., Rojas E. & Scorza J. V. (2006). Sintesis de un complejo antimonial pentavalente (Ulamina) y su aplicación experimental para el tratamiento de leishmaniasis cutánea localizada en Venezuela. Bol. Mal. Salud Amb. 46: 59-65. [ Links ]
11.Sundar S., Sinha P., Agrawal N., Srivastava R., Rainey P., Berman J., et al. (1998). A cluster of cases of severe cardiotoxicity among Kala-Azar patients treated with a high-osmolarity lot of sodium antimony gluconate. Am. J. Trop. Med. Hyg. 59: 139-143. [ Links ]
12.Tassi P., Ormas P., Madonna M., Belloli C., Carli S., De Natale G., Ceci L. & Marcotrigiano G. (1994). Pharmacokinetics of N-methylglucamine antimoniate after intravenous, intramuscular and subcutaneous administration in the dog. Res. Vet. Sci. 56: 144-150. [ Links ]
13.Valladares J., Alberola J., Esteban M., Arboix M. (1996). Disposition of antimony after the administration of N-methylglucamine antimoniate to dogs. Vet. Rec. 138: 181-183. [ Links ]
14.Valladares J., Riera C., Gonzalez P., Diez A., Portusb M., Arboix M., et al. (2001). Long term improvement in the treatment of canine leishmaniosis using an antimony liposomal formulation. Vet. Parasitol. 97: 15-21. [ Links ]
Vásquez L., Scorza J. V., Vicuña-Fernández N., Petit Y., López S., Rojas E., et al. (2005). Comparación de tolerabilidad y físico-química entre lotes de antimonial comercial y no comercializado (Glucantime® vs. Ulamina) en el tratamiento de la leishmaniasis cutánea. MedULA. 11: 1-4.
Vásquez L., Scorza D. J., Scorza J., Vicuña- Fernandez N., Petit Y., López S., et al. (2006). Pharmacokinetic of experimental pentavalen antimony after intramuscular administration in adult volunteers. Curr. Thera. Res. 67: 193-203.
Vásquez L., Vicuña-Fernández N., Petit de Peña Y., López S., Scorza J., Scorza Dagert J., et al. (2008). Disposición farmacocinética de las especies de antimonio en perros después de una dosis de antimoniato de meglumina (Glucantime®). Bol. Mal. Salud Amb. 48: 27-33.
Vásquez L. (2009). Terapéutica antileishmania: revisando el pasado, el presente y el futuro. Gac Méd. Caracas. 117: 93-111.
Vásquez L., Vásquez L., Oviedo M., Sandoval C., Méndez Y., Bastidas G., et al. (2010). Perfil clínico y epidemiológico de la Leishmaniasis Visceral Americana en el estado Trujillo, Venezuela (1975- 2007). Bol. Mal. Salud Amb. 50: 55-64.












 uBio
uBio 
